一、 澳大利亚TGA监管信息简介
1. 监管局及简介

澳大利亚TGA负责保健品(在澳大利亚TGA的定义中叫做:补充药品)的监管,包括风险分级管理、质量、安全和功效评估等。
2. 监管法规
Therapeutic Goods Act 1989
Therapeutic Goods Regulations 1990
3. 澳大利亚保健品分类
澳大利亚将保健品归类为补充药品(Complementary Medicines),并根据原料和声称的不同,分为注册类和登记类补充药品。登记类补充药品进一步分为登记补充药品(AUST L)和评定登记补充药品(AUST L(A))。
含有草药、维生素、矿物质、营养补充剂、顺势疗法和某些芳香疗法制剂等成分的医药产品被称为“补充药物”,并根据该法案作为药物进行监管。补充药物可以列出或注册,具体取决于其成分和药物的声明。大多数补充药物都列在 ARTG 上,而注册类补充药品难度非常大。
4. 准入必要条件
GMP
授权书以及Sponsor 信息
全成分、标签与包装
测试报告(理化、微生物)及其他有效性数据
制造商与产品信息
警告
5. 注册语言
英语
二、 注册流程、周期&官费
1. 注册流程图
1)食药分类
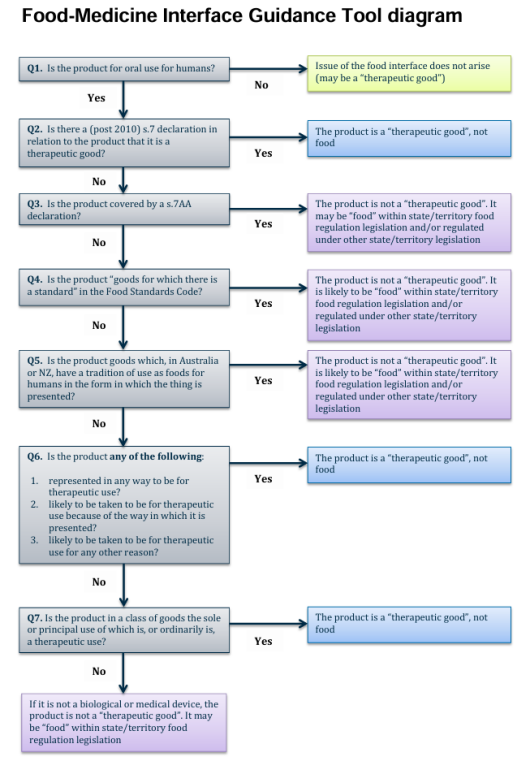
2)登记、注册路径确定

2. 注册周期及官费
1)注册周期
登记类补充药品在系统提交、付费后即可完成;而注册类补充药品预审通知为40个工作日,而评估时间会跟着风险等级升高而延长,最低风险为45个工作日,最高风险为310个工作日。
2)官费
A. 登记补充药品(AUST L)
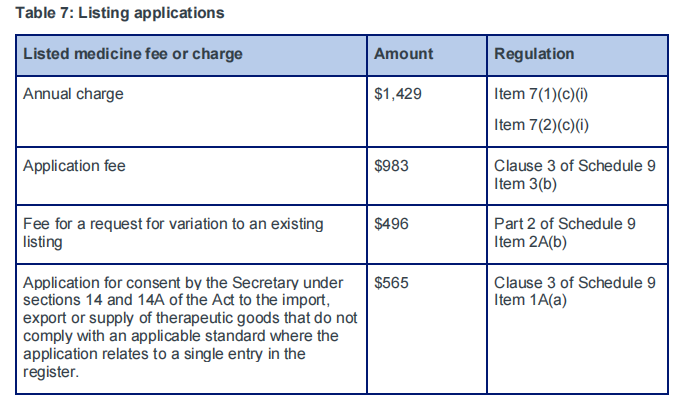

B. 评定登记补充药品(AUST L(A))
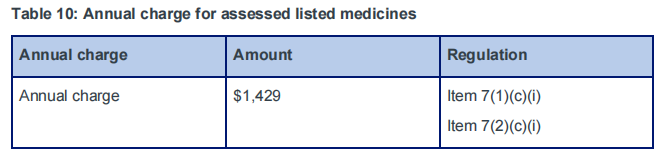

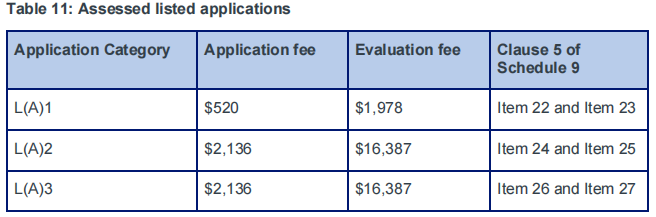
C. 注册类补充药品(AUST R)
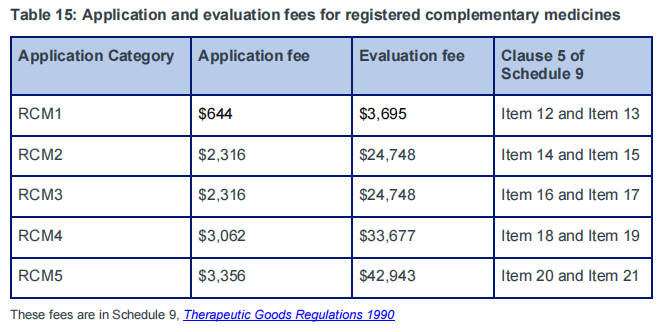
三、 FAQ
Q:澳大利亚补充药品完成注册后是否可以进行信息变更?
A:符合要求的内容可以进行变更,变更过程将产生额外费用。
Q:澳大利亚补充药品的法规定义是什么?
A:补充药物是指全部或主要由一种或多种指定活性成分组成的治疗品,每种活性成分都有明确确定的特性和传统用途。就辅助药物而言,指定有效成分是指附表14(规例)所述的一种或多种有效成分。

