A


可以。《Health Products Act 2007》规定了注册人转让相关要求,具体可参考指南《GN-24 注册人变更指南》。
可以。
产品注册阶段无需提交进口商信息;但产品销售前,需由新加坡持证人将进口商信息上传至系统。
需要,HSA认可特定机构颁发的ISO 13485证书,建议选择IAF成员组织颁发的证书。
可以。若产品发生重大变更,需向HSA提交变更申请。
可以。在泰国成为医疗器械持证人,除注册泰国公司外,还需获取TFDA颁发的医疗器械进口许可证书,同时需具备TFDA审核通过的泰国独立仓库及专业技术负责人;Wiselink Tailand泰国子公司可协助完成泰国公司成立、医疗器械进口资质申请、提供TFDA审核通过的仓库、财税合规等全流程服务。
是的。根据泰国法规要求,持证人(即进口商)需在海关系统完成申请,货物方可完成清关,参考操作流程如下: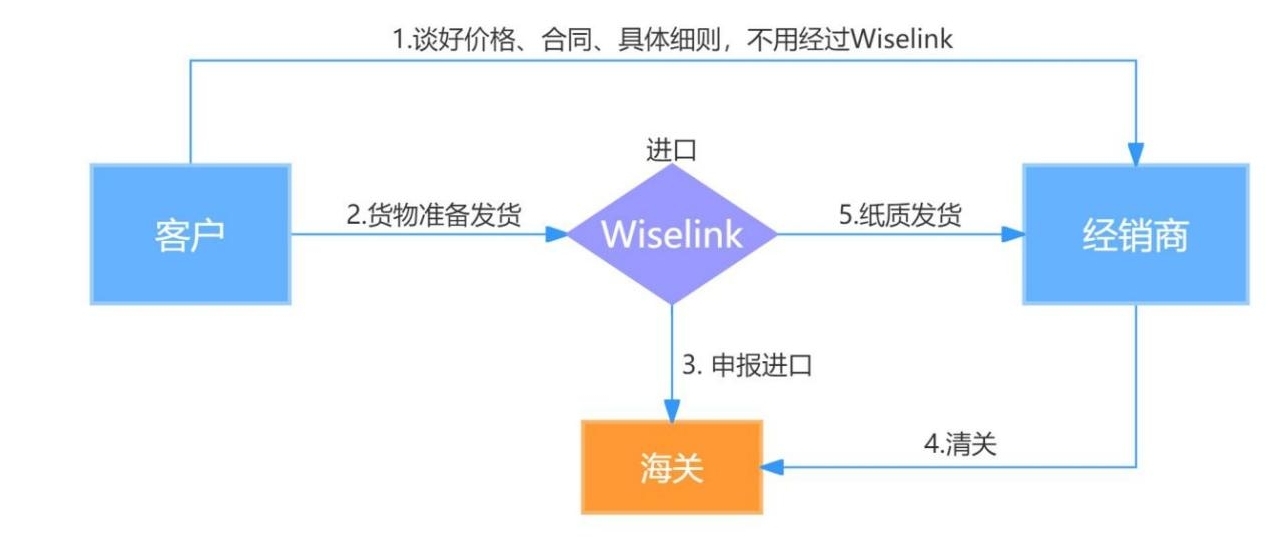
持有以下机构/国家的注册证书,申请泰国TFDA注册可实现审核加速:①欧盟(EU NB);②加拿大(HC);③日本(MHLW);④澳大利亚(TGA);⑤美国(FDA);⑥新加坡(HSA);⑦WHO体外诊断试剂预认证(WHO Prequalification of in Vitro Diagnostics,仅适用于IVD产品)。