新加坡医疗器械监管由卫生科学局(Health Science Authority,HSA)负责,核心职责是监管新加坡医疗器械的进口、制造、出口和供应,保障公众健康和安全。
医疗器械需先通过在线系统MEDICS(Medical Device Information and Communication System)提交产品文件,完成产品列名或注册后,方可合法在新加坡市场销售。
HSA风险等级分类工具官网:https://www.hsa.gov.sg/medical-devices/registration/risk-classification
新加坡对医疗器械监管要求严格,整体框架与欧美标准贴近,核心监管法规包括:
Health Products Act 2007
Health Products (Medical Devices) Regulations 2010
ASEAN Medical Devices Directive (AMDD)(东盟医疗器械指令)
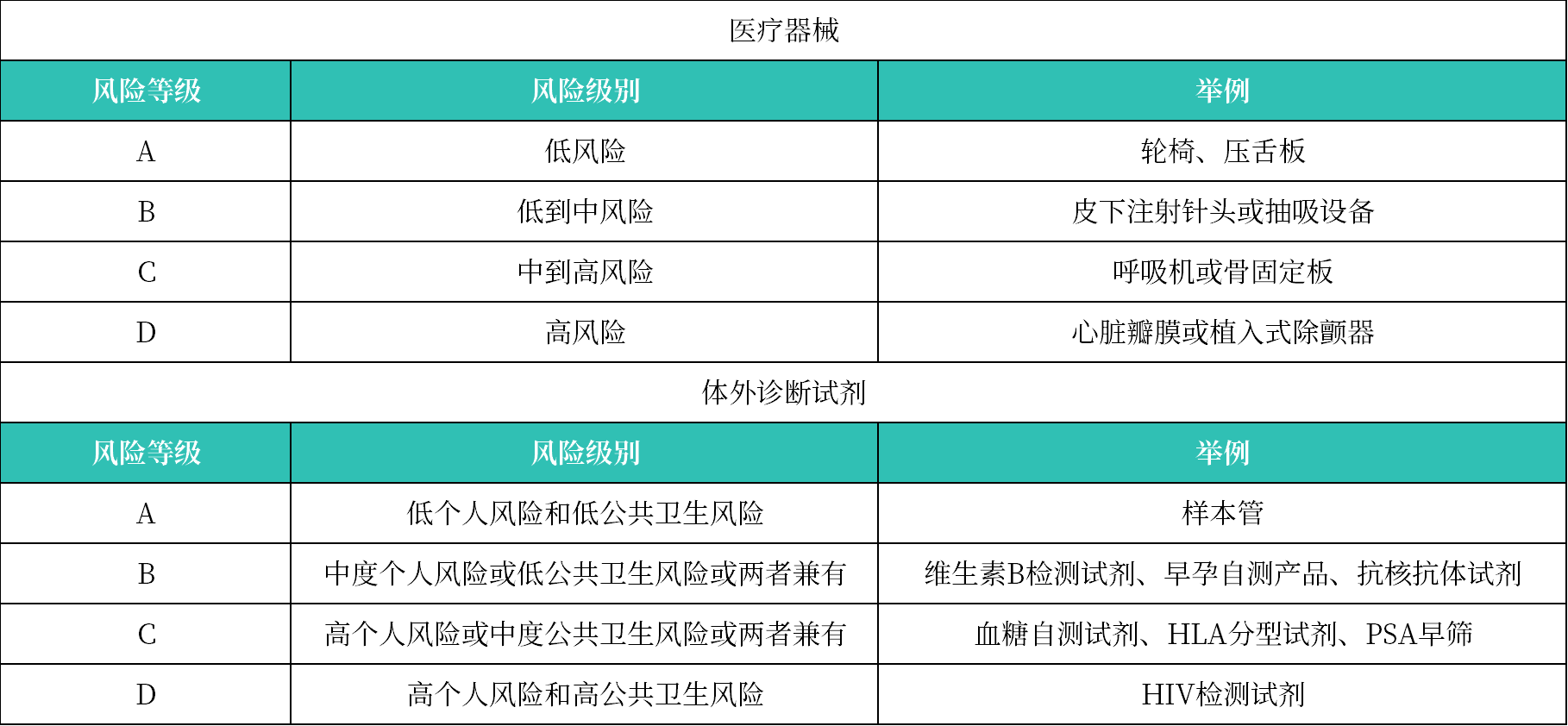
确定产品风险等级的方法如下:
① 查阅《GN-13-R2.1 普通医疗器械风险分类指南》和《GN-14-R2 体外诊断医疗器械风险分类指南》的分类规则进行判断;
② 利用HSA官网风险等级决策小工具判断(HSA | Medical device risk classification tool);
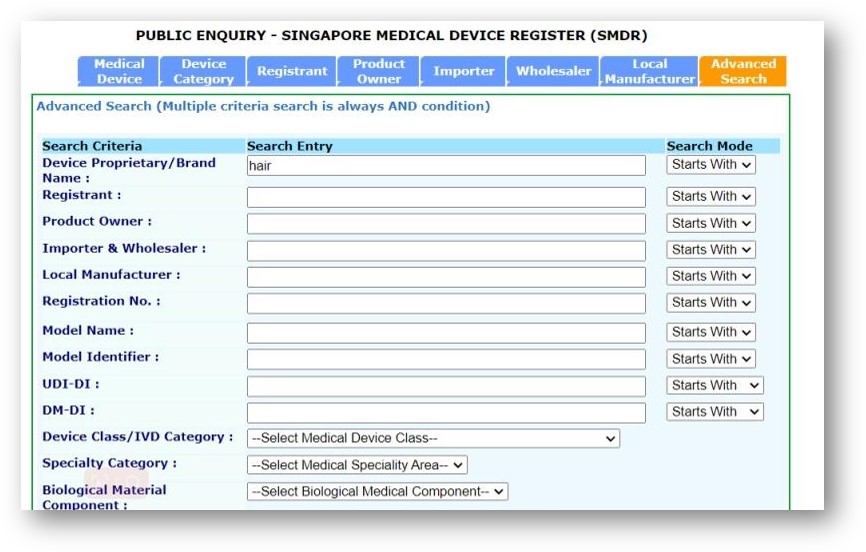
③ 利用新加坡医疗器械数据库(Public Enquiry - Singapore Medical Device Register, SMDR)查询同类产品的风险等级。
1.医疗器械和IVD产品注册,均需提供有效的ISO 13485证书;若能提供参考国注册证书,可加快注册进度,HSA认可的参考国证书包括:澳洲TGA证书、CE证书、加拿大MDL证书、日本MHLW证书、美国FDA clearance/De Novo/PMA。
2.新加坡允许将设备按类型分组申报,包括Single、Family、System、Test kit 或 Group,可通过官方工具(HSA | Medical device grouping tool)辅助判定。
3.注册资料需按照东盟共同提交档案模板 (CSDT)准备,并通过MEDICS系统在线提交;提交前,企业需申请CRIS(客户注册和识别服务)帐户并注册为CRIS管理员。
4.申请主体需为新加坡本地实体公司;非本地企业需授权当地实体公司作为授权代表(即注册人)。
5.指定的进口商和批发商,需拥有符合良好分销规范医疗器械许可证(GDPMDS)或ISO 13485的经销商许可证,其中GDPMDS认证需由新加坡认可委员会认可的机构颁发。
英语
当地代表(许可证持有人)要求
① 注册人无需HSA许可证,但必须在MEDICS系统完成注册;
② 所有医疗器械注册申请需由注册人提交,且注册人需负责产品上市后相关活动;
③ 注册人需监管制造商在新加坡的授权进口名单,若为独立第三方注册人,需授权分销商或进口商完成全流程闭环;
④ 同一设备可由多个注册人注册;若与前注册人合作终止且对方不愿转移证书,则需重新注册;
⑤ 许可进口商需具备ISO 13485证书和/或良好分销规范医疗器械–新加坡 (GDPMD-S) 许可证,并完成HSA注册。
1.注册流程

注:非无菌A类医疗器械可免除注册,但需在经销商执照申请期间,在MEDICS系统填写A类豁免清单并告知HSA;无菌A类医疗器械(含体外诊断器械)仍需完成注册。
2.注册路径
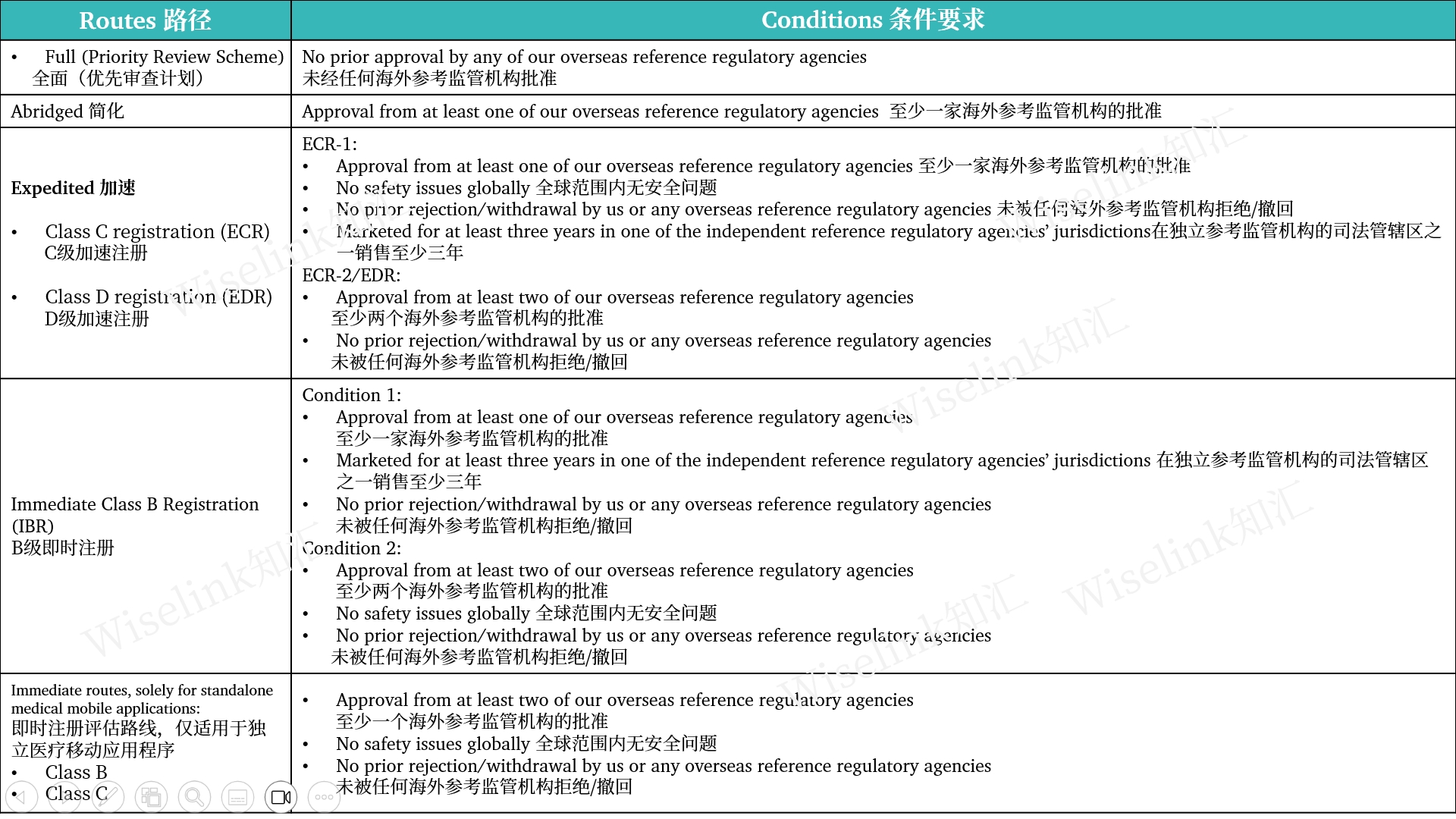
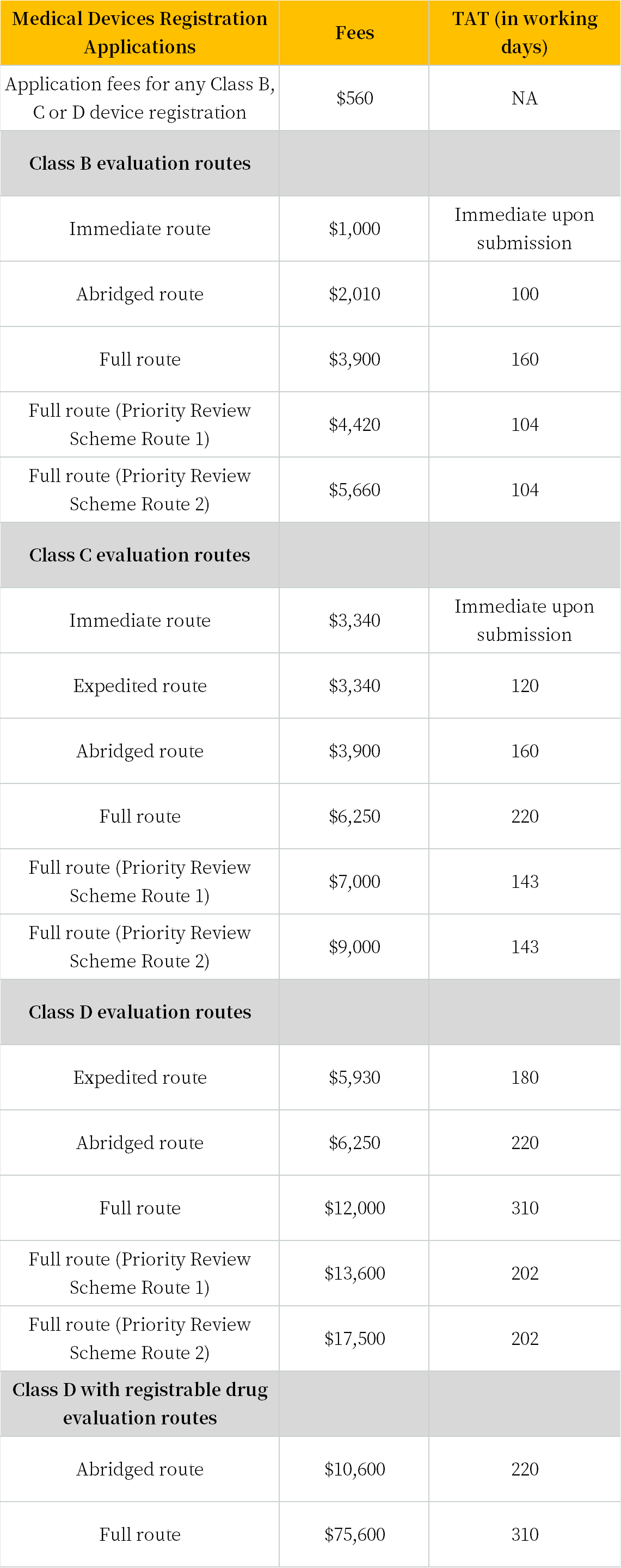
3.注册官费及周期
参考官网公示:HSA | Fees and turnaround time for medical devices
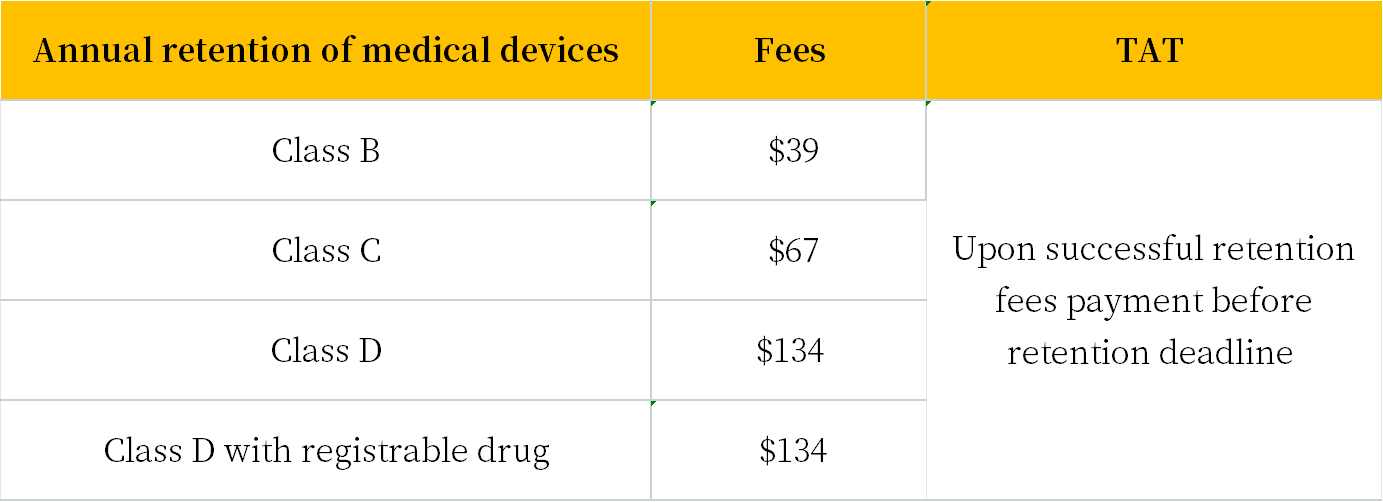
Annual retention in the Singapore Medical Device Register (SMDR)
Change of registrant
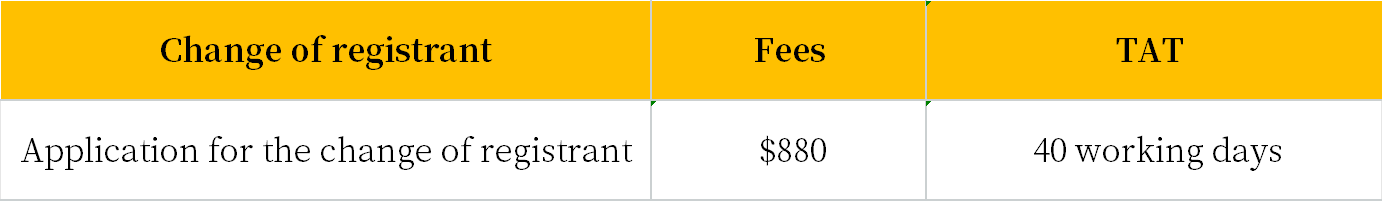
费用及周期汇总: