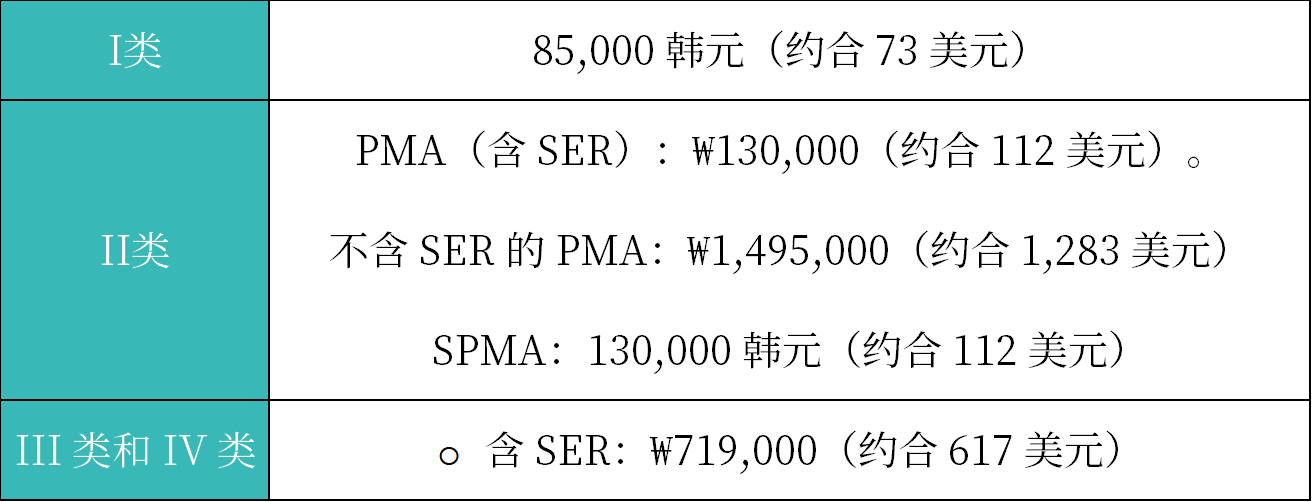
韩国医疗器械监管由卫生福利部(MHW)统筹管理食品、药品、化妆品及医疗器械相关事宜,依照《医疗器械法》,其下属的食品药品安全部(MFDS)为医疗器械具体监管执行部门,负责全流程的监管工作。
Medical Device Act [MDA](医疗器械法)
Enforcement Decree of MDA.(医疗器械法实施法令)
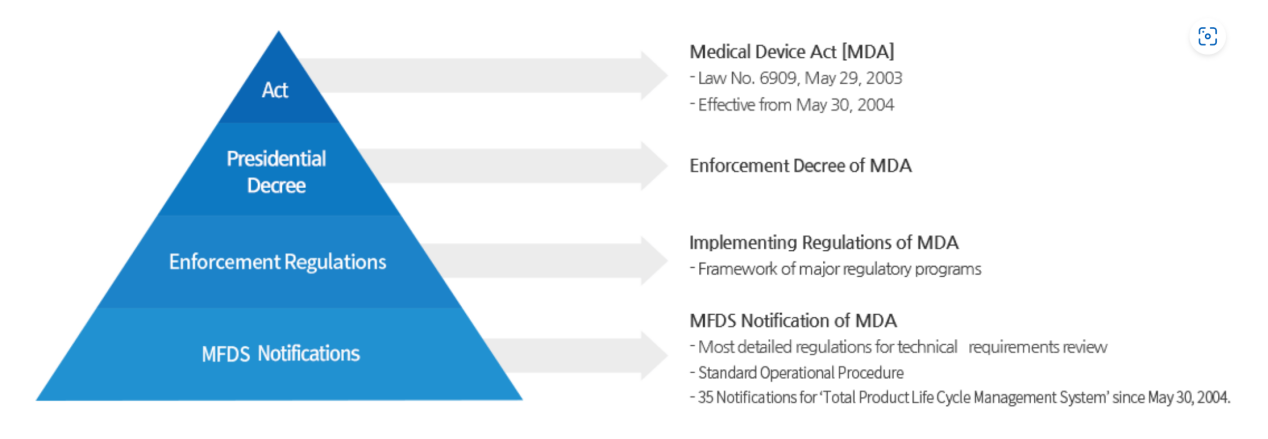
韩国将医疗器械分为普通医疗器械(不含IVD)和体外诊断医疗器械(IVD)两大类,分别按风险程度划分等级,具体分类参考如下:
【Medical Device (except IVD) 普通医疗器械】
【IVD 体外诊断医疗器械】

向MFDS申请医疗器械认证和批准,核心需提交包含产品质量、性能、安全等相关信息的技术文件,具体涵盖预期用途、作用机制(MoA)、操作(功能)结构、原材料、使用说明、测试规范等内容。
质量体系方面,除I类产品外,其余风险等级医疗器械均需获得KGMP证书。
韩语与英语
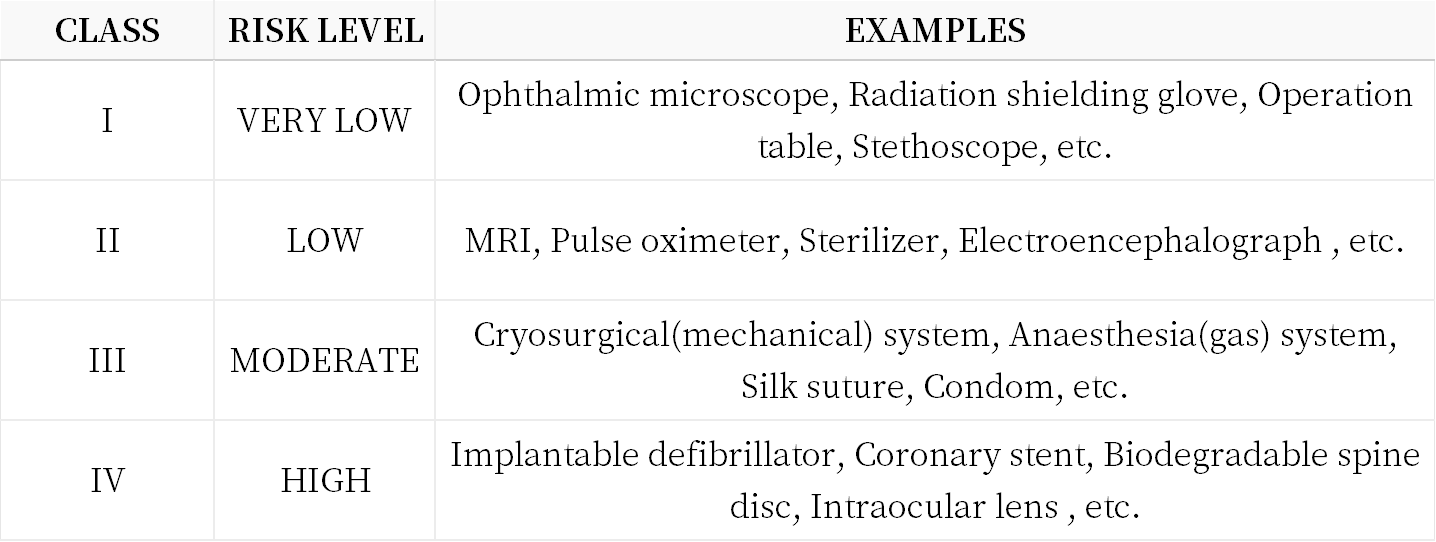
1. 注册流程图


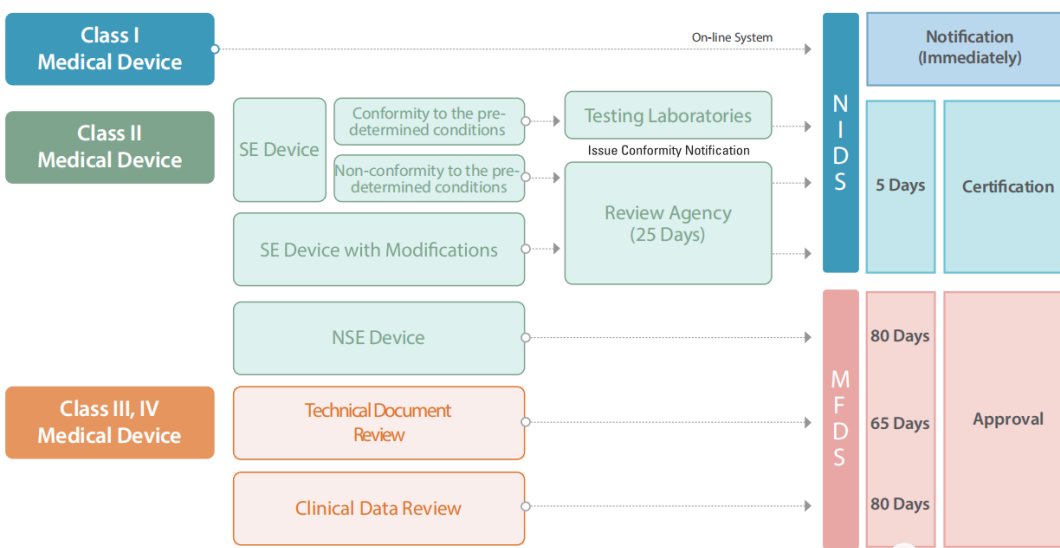
2. 注册周期及官费参考
3. 官方审核时间(Wiselink项目经验)
韩国医疗器械按风险分类对应不同市场准入途径,审核时长不同:
① I类器械:约2个月;
② II类器械:约4-7个月;
③ III、IV类器械:约145个工作日。
4. 注册费用参考