日本医疗器械监管由厚生劳动省MHLW(Ministry of Health,Labor and Welfare)和药品和医疗器械局PMDA协同负责,MHLW为核心监管部门,负责制定监管政策、最终审查注册批准、产品退市等核心管理工作;PMDA为相对独立的行政机构,与MHLW合作实施监管政策,主要承担医疗器械审核审批、QMS/GLP/GCP体系检查、不良事件报告收集分析等工作。
日本PMD法案官网:https://www.japaneselawtranslation.go.jp/ja/laws/view/3214
Pharmaceutical and Medical Device Act,简称PMD act.
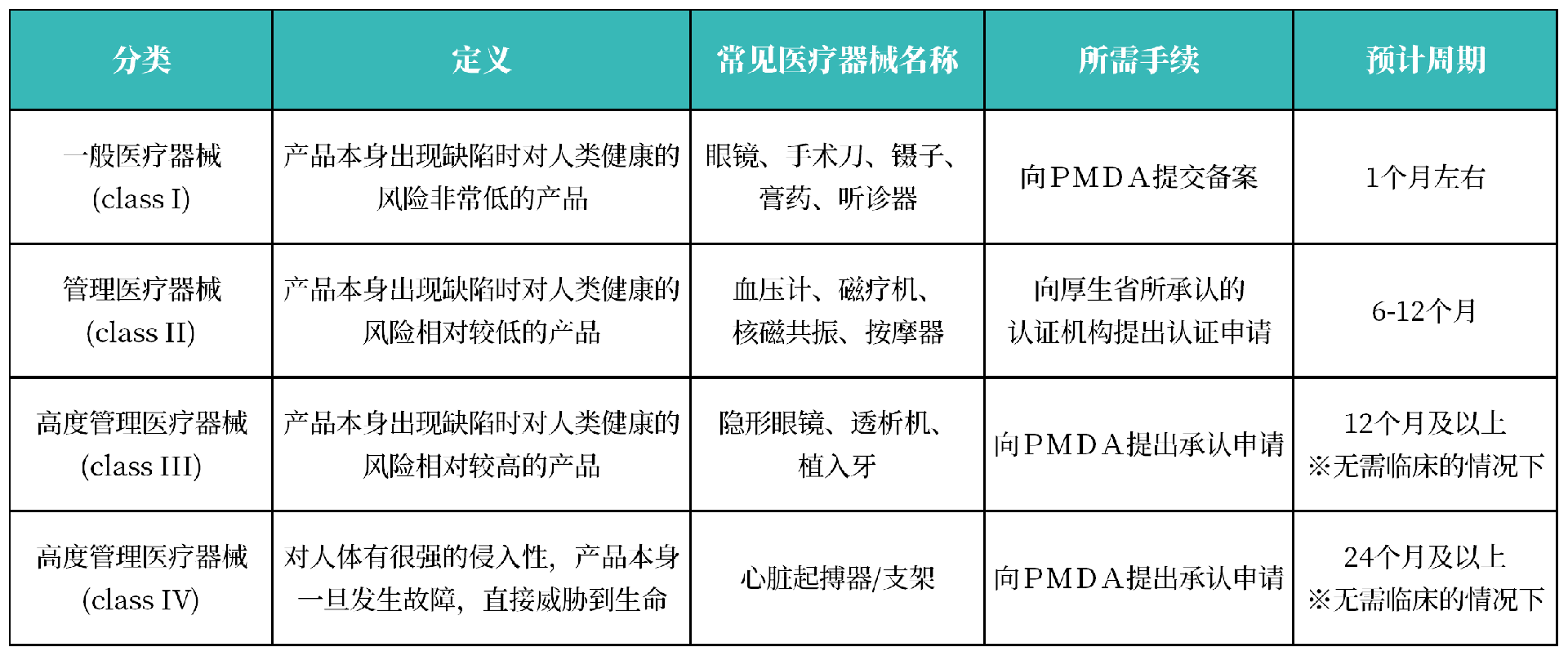
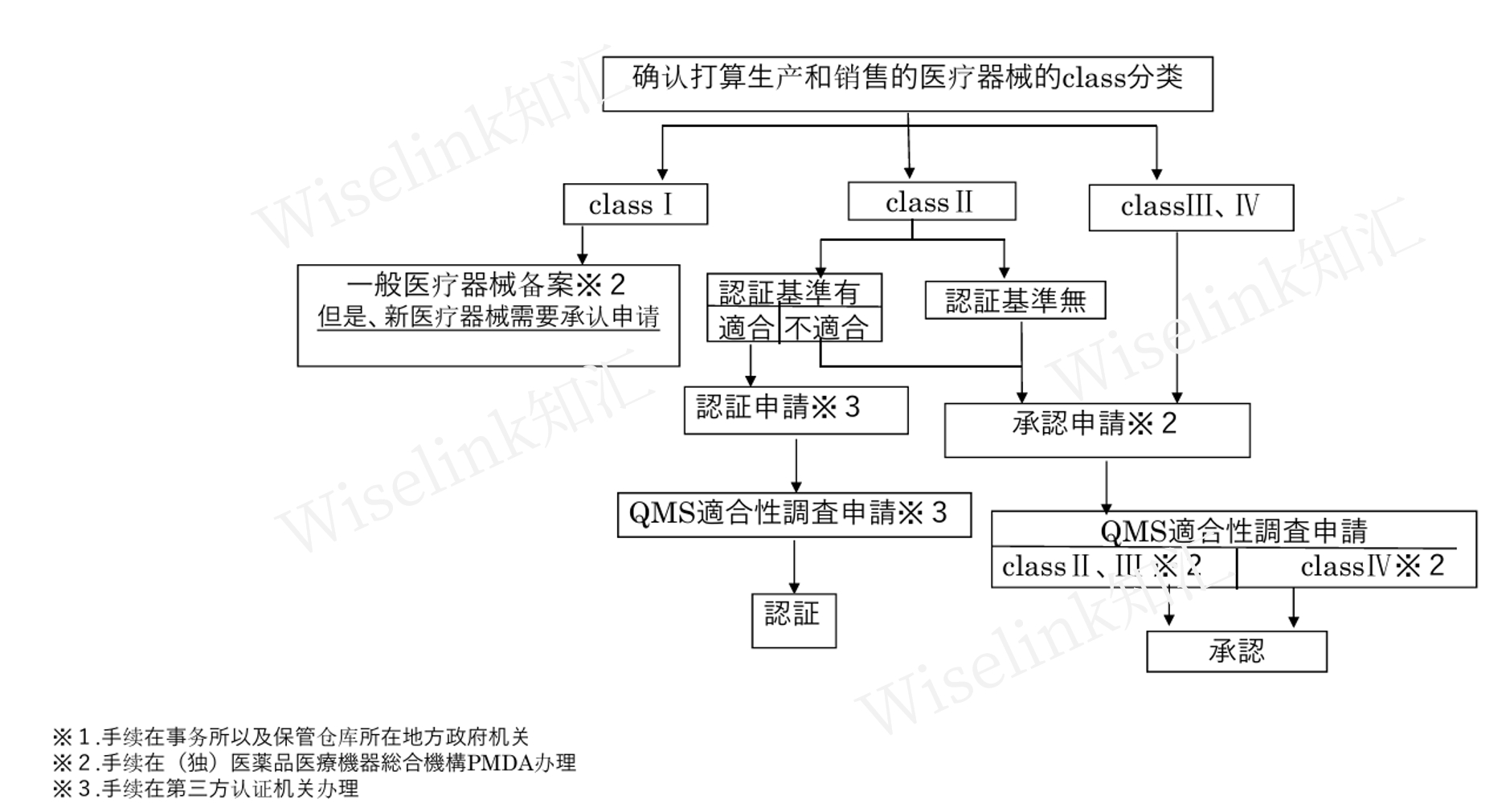
日本医疗器械分为I、II、III、IV 4个风险等级,按风险程度从低到高划分。

日语

PMD法案第63条规定医疗器械直接容器或包装需标注以下信息:
①营销授权持有人的姓名和地址
②产品名称
③制造编号或制造代码
④MHLW指定医疗器械的内容物重量、体积、数量等
⑤按相关条款规定的医疗器械标准事项
⑥MHLW指定医疗器械的有效期