


日本实行三级分工监管体系:
① **厚生劳动省(Ministry of Health, Labour and Welfare,简称MHLW)**:化妆品行业主管部门,负责制定法规、标准及最终审批。
② **药品和医疗器械局(Pharmaceuticals and Medical Devices Agency,简称PMDA)**:负责外国制造商和进口商申请的文件审查与现场核查、不良反应报告评估。
③ 各都道府县政府:负责本地企业的经营许可、日常检查与指导。
Pharmaceutical and Medical Device Law (PMDL),原《药事事务法》(Pharmaceutical Affairs Law, PAL)
普通化妆品定义:通过摩擦、喷雾或其他类似方法施用于人体,以清洁、美容、增加吸引力、改善外观或保持皮肤/头发健康为目的的物质。**医药品及医药部外品除外**。
特殊分类:医药部外品
具有特定功效的产品,如除臭剂、脱毛剂、生发治疗剂、杀菌消毒剂、美白产品等,归属PMDA按医药部外品监管,准入要求更严格。
① 提供持有有效化妆品制造销售许可证的日本进口商详细信息;
② 提交境外制造商出具的授权书;
③ 提供化妆品质量管理体系及上市后安全管理体系相关文件;
④ 提交境外制造商完整资质信息;
⑤ 提供产品基本信息、功效宣称、全成分配方表及合规标签。
日语
前置环节:外国制造商认证(必备)
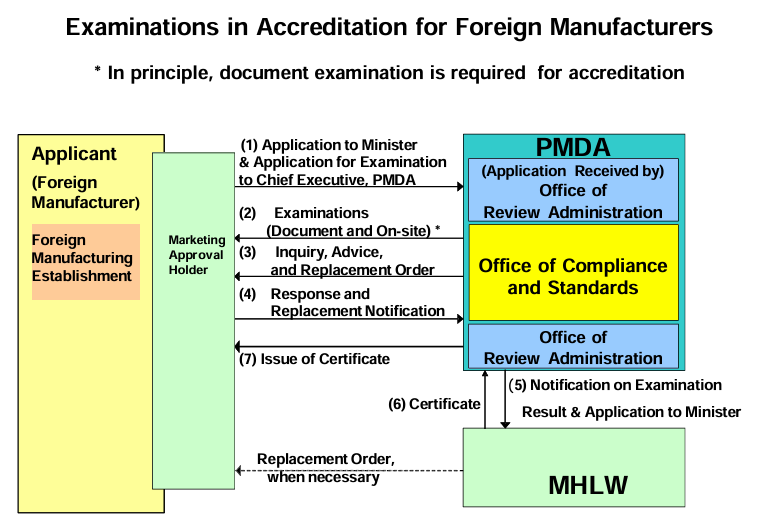
认证流程:外国制造商提交申请→向MHLW大臣递交申请→PMDA开展文件审查(原则上必备)及现场核查→合规办公室问询与回复→审查结果通知MHLW→大臣审批→颁发外国制造商认可证书
整体产品准入流程:
产品分类界定→进口商资质审核→成分与标签合规性审核→完成外国制造商认证→提交产品信息通知
| 业务类型 | 审查方式 | 官方费用 |
|---|---|---|
| 外国制造商首次认定 | 书面审查 | 62,600 |
| 实地审查 | 143,900 + 外国旅费 | |
| 外国制造商认定变更 | 书面审查 | 42,900 |
| 实地审查 | 69,700 + 外国旅费 | |
| 外国制造商认定区分变更/追加 | 书面审查 | 42,900 |
| 实地审查 | 69,700 + 外国旅费 | |
| 普通化妆品注册 | 书面审查 | 37,300 |
| 医药部外品注册 | 书面审查 | 37,300 |
| 特殊化妆品注册 | 书面审查 | 337,300 |
| 产品名称变更(代替新规申请) | 书面审查 | 37,300 |
A:根据内阁命令规定,外国制造商认可证书的有效期为5年。
A:可以续期。需在有效期内提交"认可续期申请书"及"认可审查申请书"。
① 旧PAL下证书首次续期:需额外附上旧进口许可证副本给日本进口商;
② 新PMDL下证书续期:需在续期申请表内附上原认可证书。
未按时续期的,认可证书自动失效。