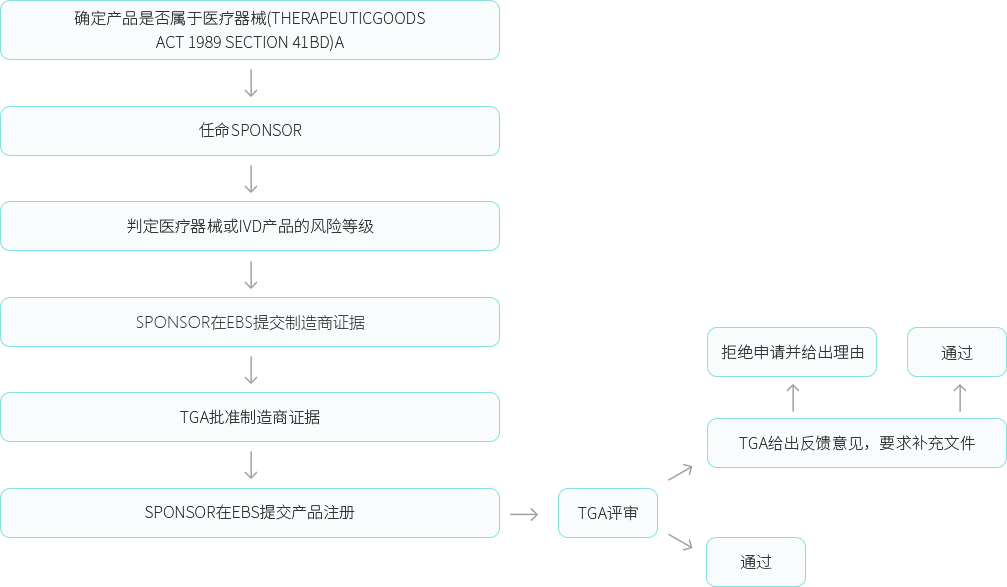
TGA(THERAPEUTIC GOODS ADMINISTRATION)是澳大利亚医疗器械的主管部门,作为澳大利亚医疗用品(含药物、医疗器械、基因科技、血液制品)的监督机构,具体负责医疗卫生用品的进口、出口、生产、供应及推广全流程管理工作。
THERAPEUTIC GOODS ACT 1989
THERAPEUTIC GOODS (MEDICAL DEVICES) REGULATIONS 2002
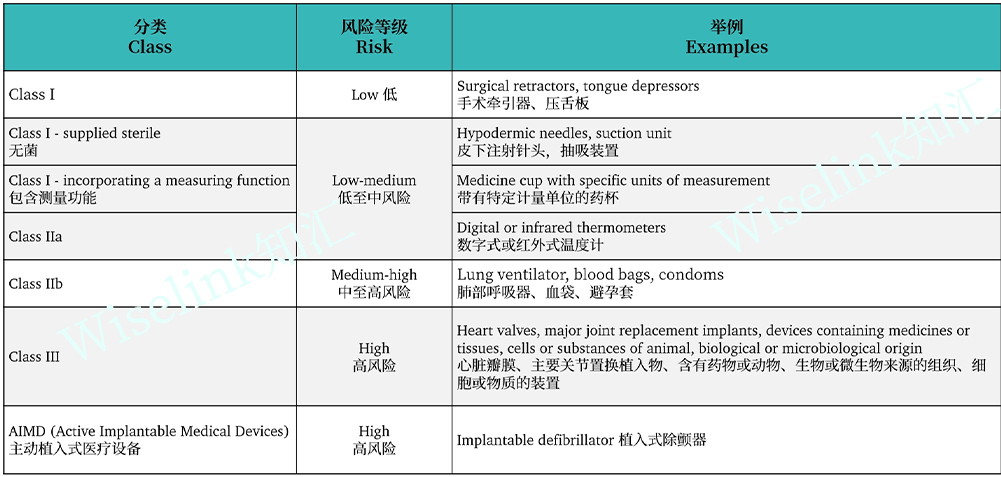
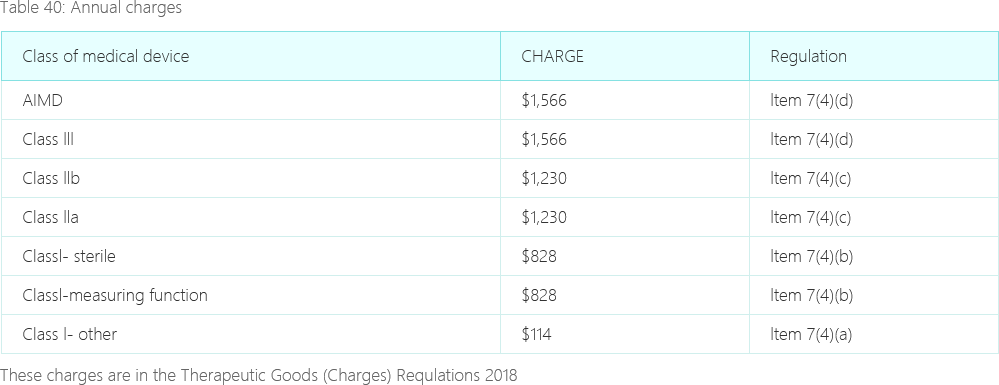
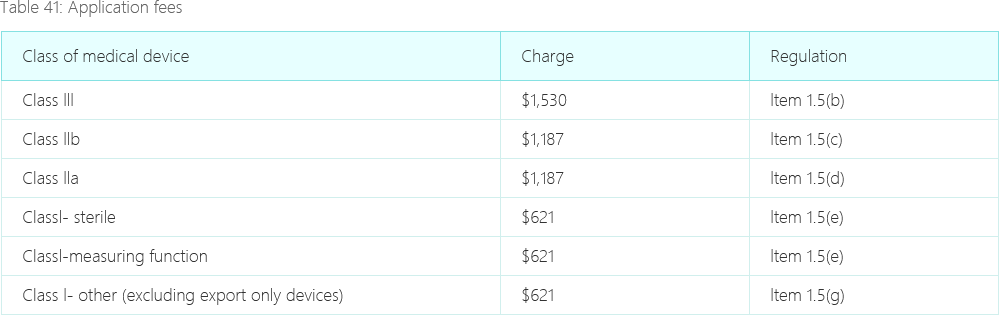
医疗器械和IVD产品提交TGA注册时,均需提供合规的制造商证据,目前TGA认可的制造商证据及注册批准文件包括:
① 澳洲本土颁发的符合性评定证书(AU CAB/ COC)
② MDSAP证书 | ISO 13485证书
③ 认可的海外注册批准文件:
• AU CAB CERTIFICATE
• TGA CONFORMITY ASSESSMENT CERTIFICATE
• EC CERTIFICATE
• HEALTH CANADA LICENCE
• JAPAN PRE MARKET CERTIFICATION/ APPROVAL
• SINGAPORE HSA CERTIFICATE
• MRA CERTIFICATE
• US FDA 510(K) DETERMINATION
• US FDA DE NOVO ORDER
• US FDA PREMARKET APPROVAL
英语
澳洲医疗器械持证人(SPONSOR)负责向TGA申请将医疗用品列入澳大利亚医疗用品登记处(ARTG),在澳大利亚市场,医疗产品必须完成ARTG列名后方可合法出售。
SPONSOR主体要求:必须为澳大利亚居民,或在澳大利亚注册成立且实际开展业务的机构,且公司指定代表需居住在澳大利亚。
上市后法定责任(器械列入ARTG后):SPONSOR需配合TGA完成上市后监测工作,履行持续报告及资料留存义务,具体包括:
• 及时向TGA报告产品不良事件
• 及时向TGA报告海外监管机构针对该产品采取的监管行动
• 提交制造商开展的相关调查结果(如后续临床研究、不良事件审查报告等)
• 从制造商处获取TGA要求的各类合规资料,并妥善留存产品分销记录
TGA会将所有收到的不良事件报告、产品投诉录入专属数据库,由内部临床医生和科学家团队进行专业风险评估,必要时启动产品调查,调查过程中可根据需求征求外部专家意见。