


香港医疗器械监管由医疗仪器科(前称医疗仪器管制办公室)负责,其建立了独特的医疗器械监管体系,即MDACS (Medical Device Administrative Control System)(医疗器械行政控制系统),专门用于医疗器械的监管事宜。
International Medical Device Regulators Forum,简称IMDRF(国际医疗器械监管机构论坛)
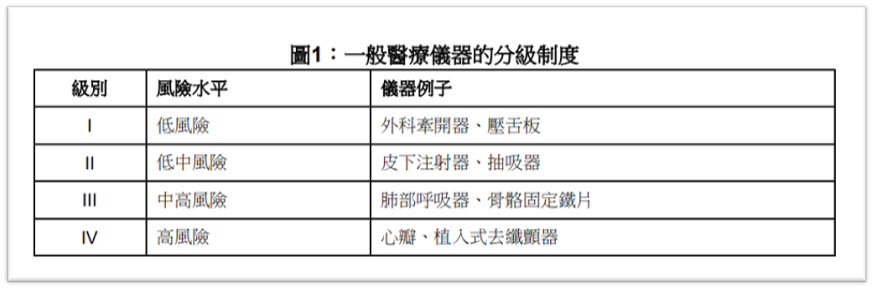
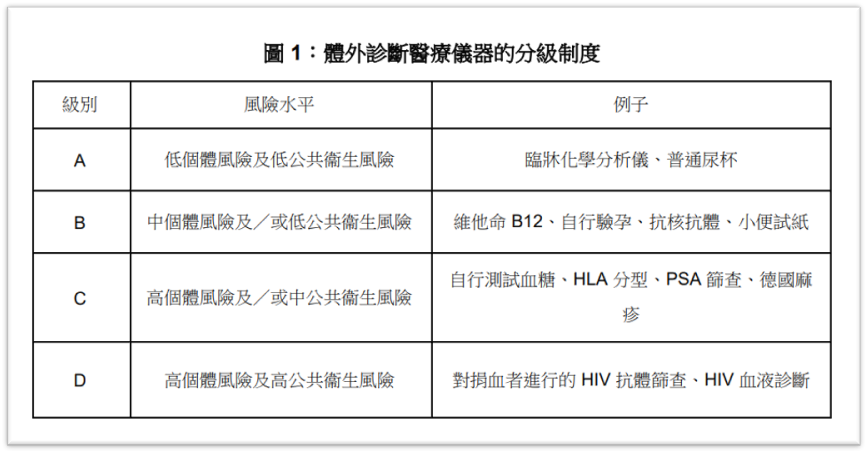
香港参考国际医疗器械监管机构论坛(IMDRF)的分类原则,将医疗器械(含普通医疗器械和体外诊断医疗器械(IVDMDs))按预期用途相关风险水平划分等级:
1. 普通医疗器械(MD)分为4类,风险从低到高为第I、II、III、IV类;
2. 体外诊断医疗器械(IVD)分为4类,风险从低到高为第A、B、C、D类。
仅第II、III、IV类普通医疗器械和第B、C、D类体外诊断医疗器械可申请香港表列,第I类普通医疗器械和第A类体外诊断医疗器械因风险等级最低,不接受表列申请。
确定产品风险等级的方法:
① 查阅《TR-003普通医疗器械分类》和《TR-006体外诊断分类》的分类规则判断;
② 利用官网风险等级决策小工具判断;
一般醫療儀器分級程式
體外診斷醫療儀器分級程式
③ 利用香港医疗器械表列数据库(医疗仪器列表)查询同类产品等级。
需依据《TR-002證明符合醫療儀器安全及性能基本原則的技術文件摘要》准备资料,所有申请材料均要求以中文及英文填写,向MDACS提交对应申请表格(医疗器械填MD-C2&3&4表,IVD填MD-IVD表)。
必备文件清单:
Ø CE证书或510K信函
Ø 质量管理体系符合性证明,如ISO 13485证书
Ø 标签和使用说明,需符合《TR-005醫療儀器標籤附加規定》
Ø 上市后程序
Ø 国际测试报告和临床数据(如适用)
Ø 按照TR-004编写基本原则检查表(IVDs需额外提供性能评估报告)
具体可参考指南:《GN-02第II III IV级一般医疗仪器表列指南》和《GN-06第B,C及D级体外诊断医疗仪器表列指南》。
英语或繁体中文
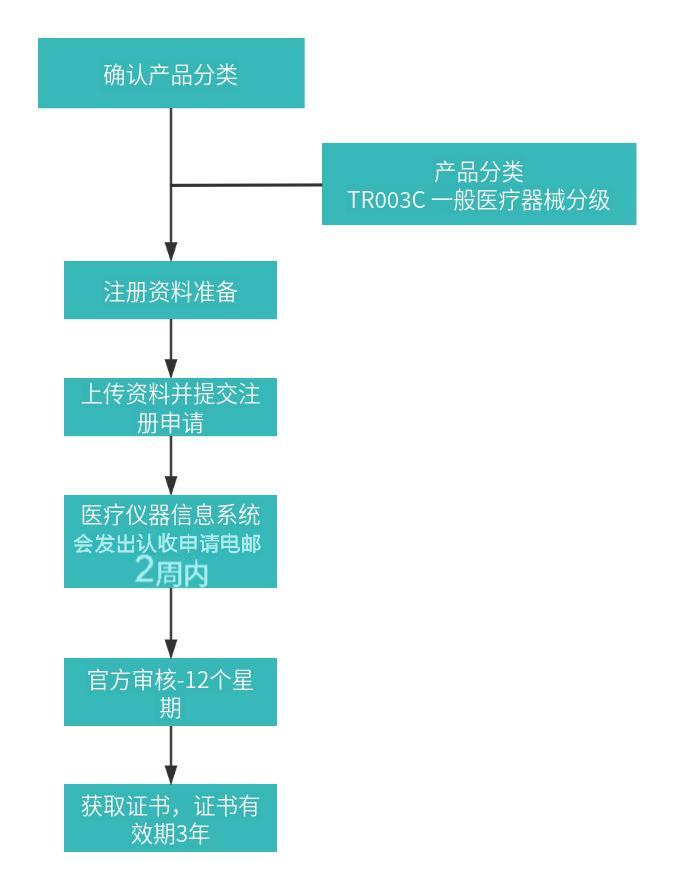
注册周期:递交申请及全部所需证明资料 (包括标签样本)后,12个星期内完成表列。