

新西兰MEDSAFE(Medicines and Medical Devices Safety Authority),是新西兰政府负责监管和管理医疗器械和其他医疗产品的机构。该机构负责新西兰医疗产品的注册审核、法规制定、市场监管。
Medicines Act 1981
Medicines Regulations 1984
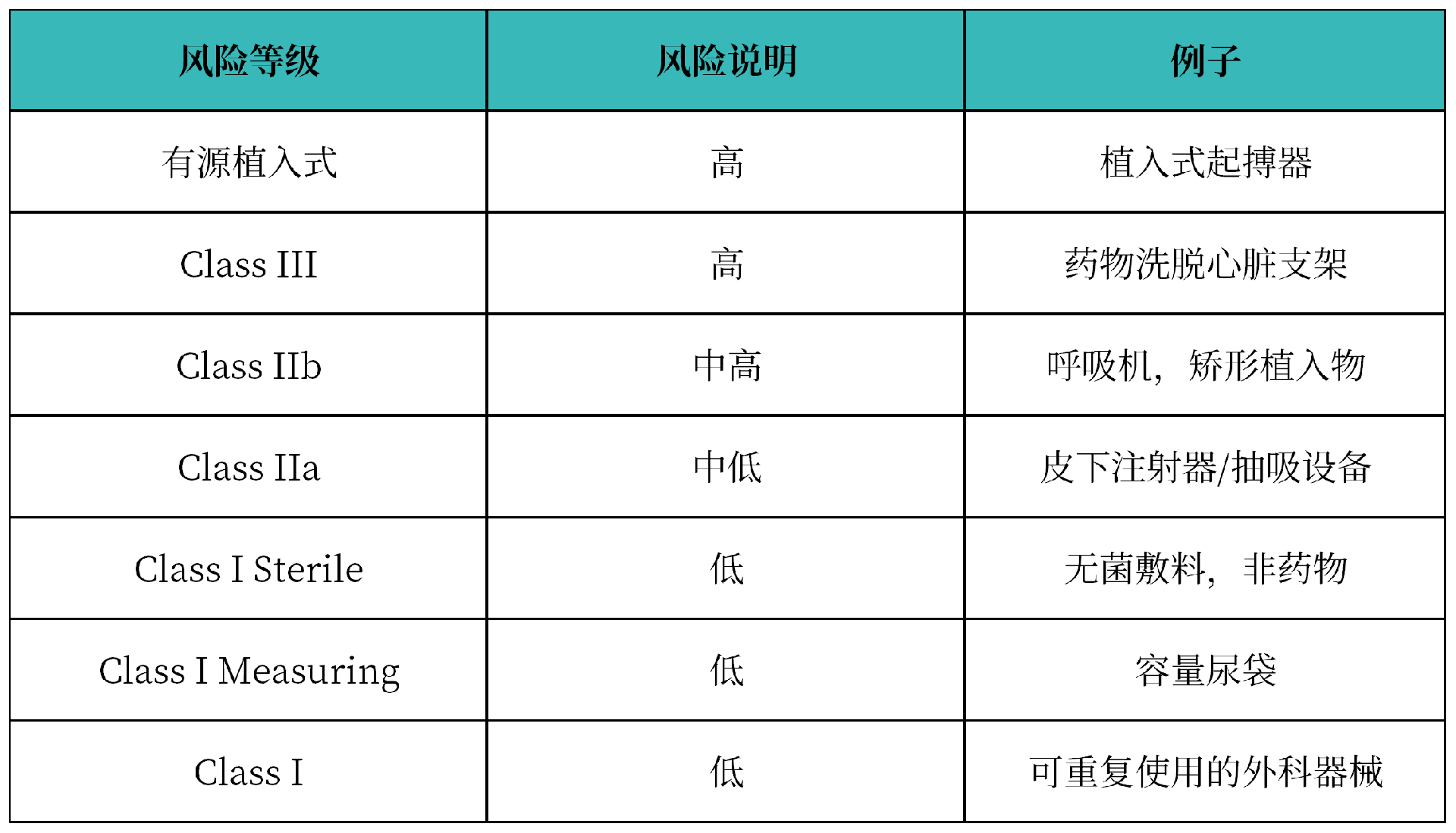
所有医疗器械都是按照与欧盟和美国FDA分类系统类似的基于风险的方法进行分类的,范围从I类(基本/灭菌/测量)、IIa、IIb和III类。
ISO 13485
技术文件:制造商必须提交详尽的技术文档,包括产品规格、质量标准、制造流程、风险评估报告等,以证明产品的安全性和有效性。
英语
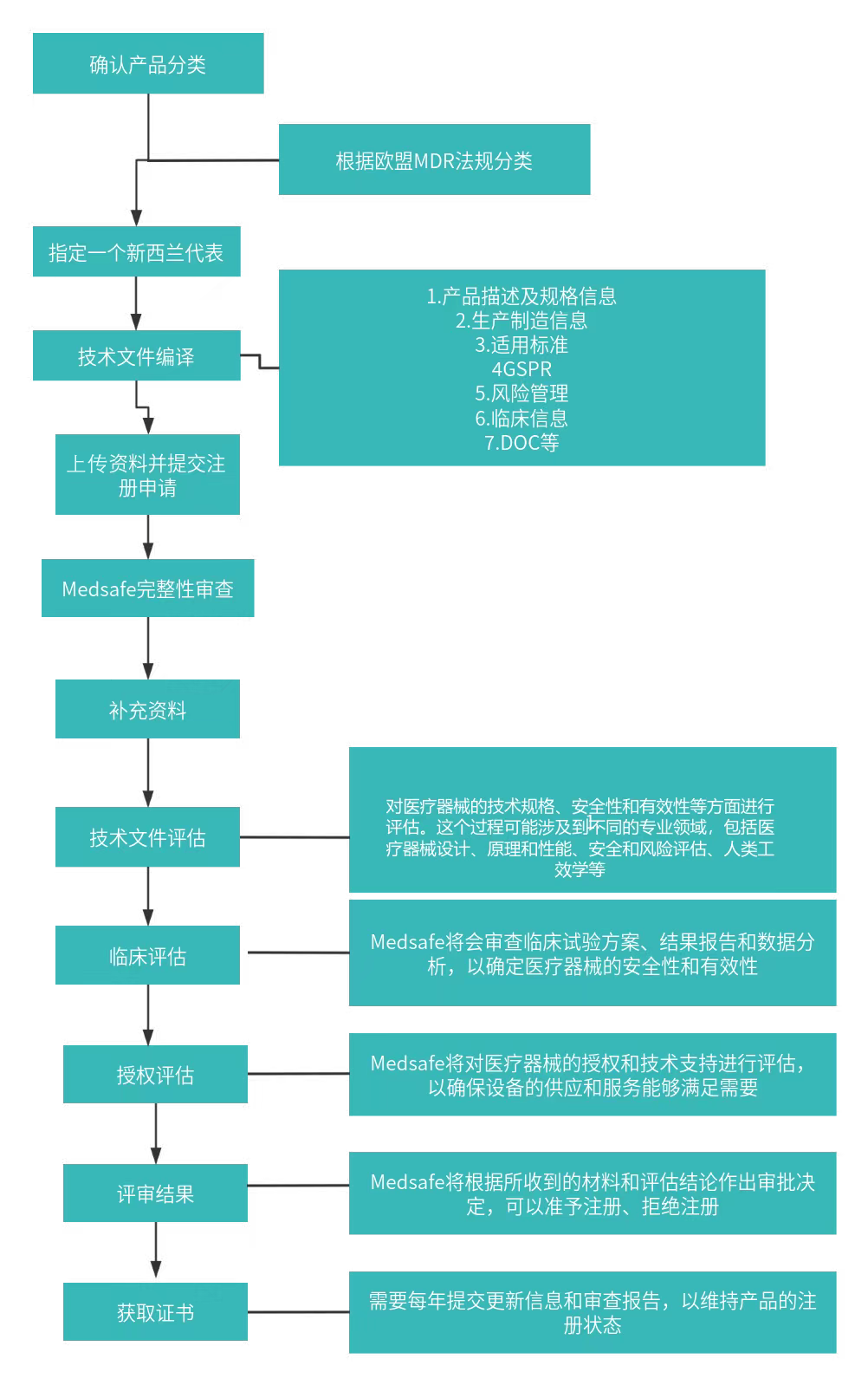
Medsafe在收到所有必要文件和信息后,通常需要1个月左右可以完成医疗产品的注册。
注册周期可能会因为产品类型、复杂性和其他因素而有所差异。
新西兰MEDSAFE目前不收取官方费用。