泰国医疗器械监管由泰国食品药品监管局(Thai Food and Drug Administration,TFDA)全权负责,核心职责为监管和审批泰国市场销售的医疗器械,保障产品的安全性、有效性和质量,具体包括:审批医疗器械注册申请、制定并执行相关法规标准、监督医疗器械市场流通与使用并开展相关检查。
官方信息:
Address:Food and Drug Administration, Ministry of Public Health88/24 Tiwanon Road, Mueang District, Nonthaburi 11000 THAILAND
Open:Monday-Friday 08.30-16.30 hrs.
Medical Devices Act, B.E.2551 (2008) and (No. 2), B.E. 2562 (2019)
ASEAN Medical Device Directive(东盟医疗器械指令AMDD)
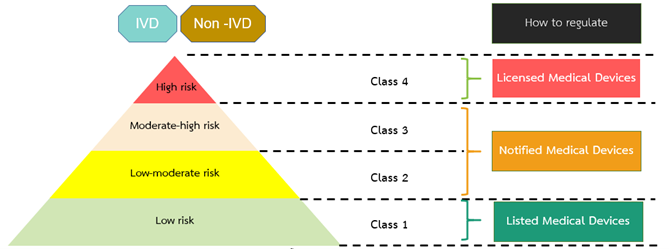
泰国医疗器械风险等级分类严格遵循东盟医疗器械指令AMDD附录3,依据泰国法规 RISK CLASSIFICATION OF MEDICAL DEVICES,Β.Ε. 2562 (2019),将医疗器械分为普通医疗器械(Non-IVD)和体外诊断试剂(IVD)两大类,均按风险由低到高分为四个等级:Class 1、Class 2、Class 3、Class 4。
需提供ISO 13485质量管理体系证书
【供专业人士使用】:英语
【供非专业人士使用】:标签、说明书需提供英文和泰语版本;除标签、说明书外的其他资料,可仅提供英文版。
1.注册途径

①Full evaluation 全流程审批路径:无任何国家注册历史的产品可申请;
②Concise pathway 简化审核路径:适用于Class 2~Class 4医疗设备;产品需在欧盟(EU NB)、加拿大(HC)、日本(MHLW)、澳大利亚(TGA)、美国(FDA)、WHO组织6个参考监管机构中任意一个获得注册认证(全面评估)并上市一年以上,且无严重不良事件;
③Reliance program 依赖审核路径:适用于Class 2~Class 4医疗设备;产品需在新加坡(HSA)获得批准。
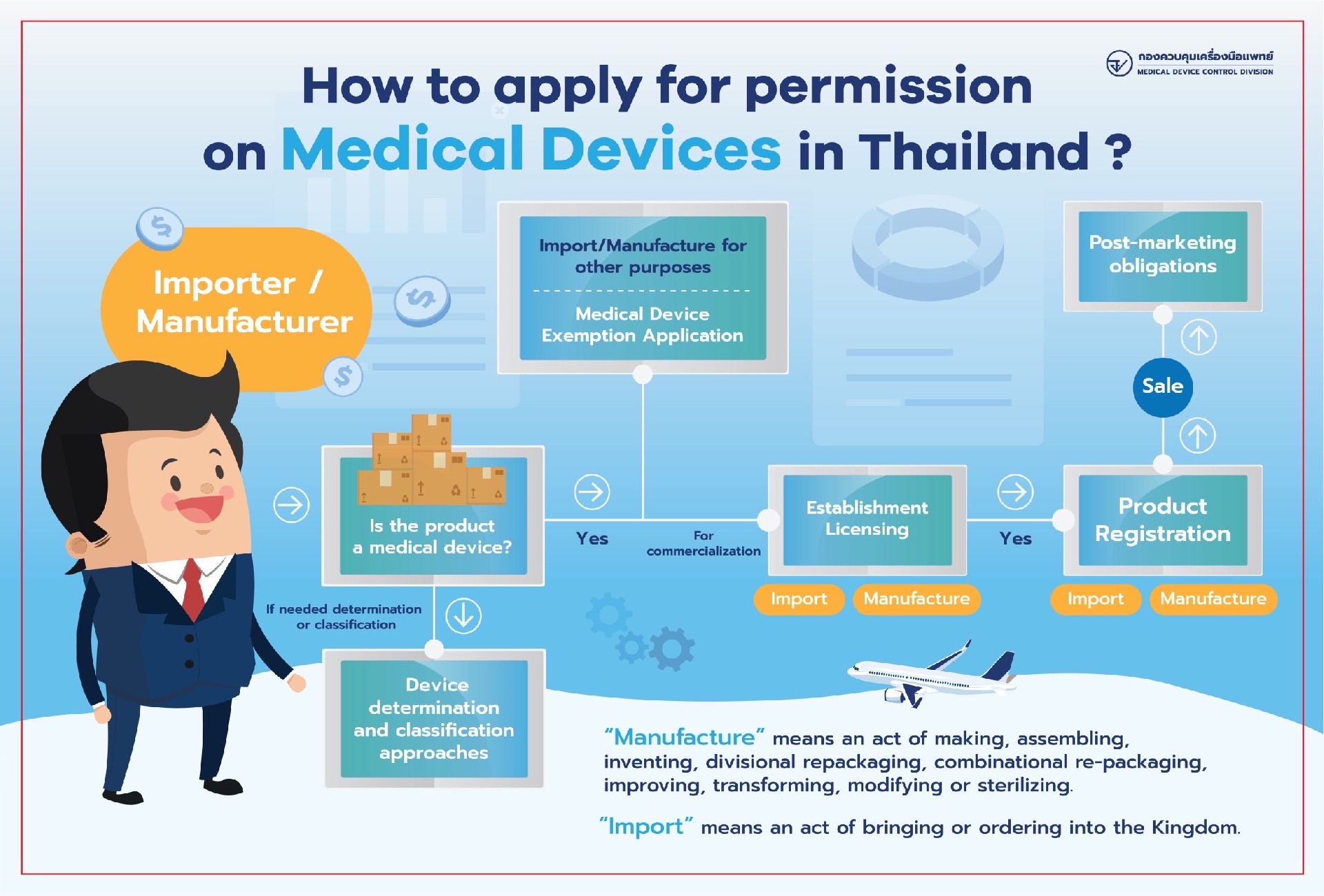
2.注册流程
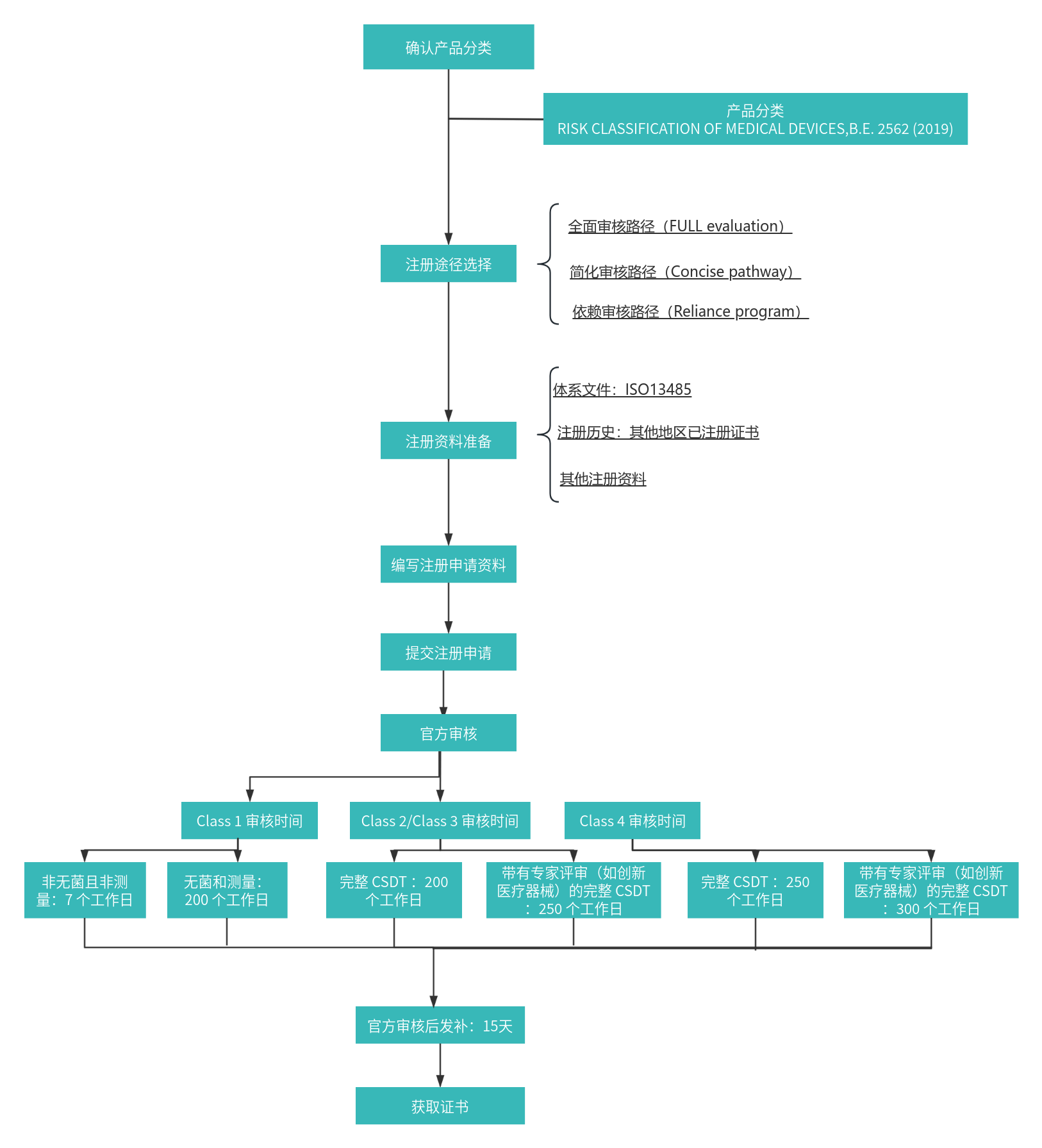
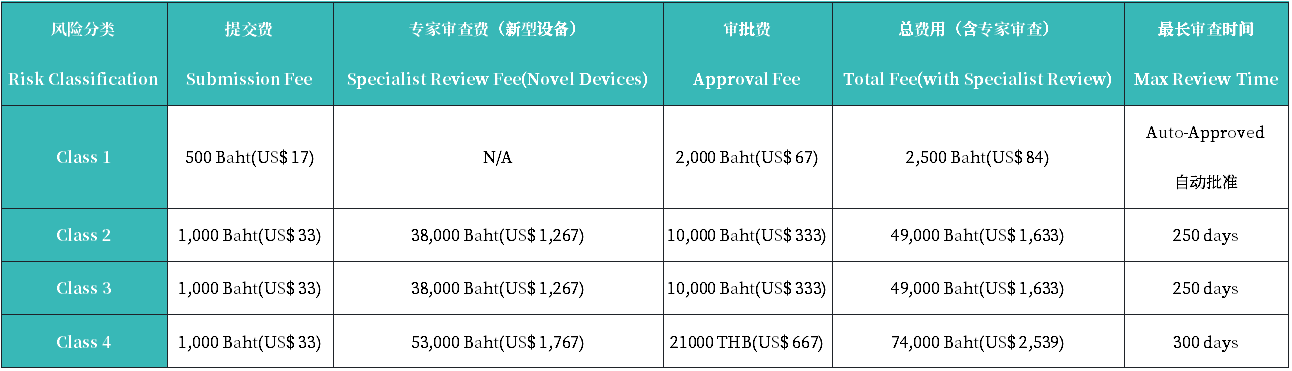
3.注册周期及官费