


肯尼亚医疗器械由药房和毒药委员会(Pharmacy and Poisons Board,简称PPB)统一监管,核心职责包括:医疗器械市场准入审批、产品合规性评估、生产与进口环节监督、上市后质量监测及不良事件管理。
Pharmacy and Poisons Act
医疗器械按风险等级分为Class A、Class B、Class C和Class D四类,风险等级依次升高:
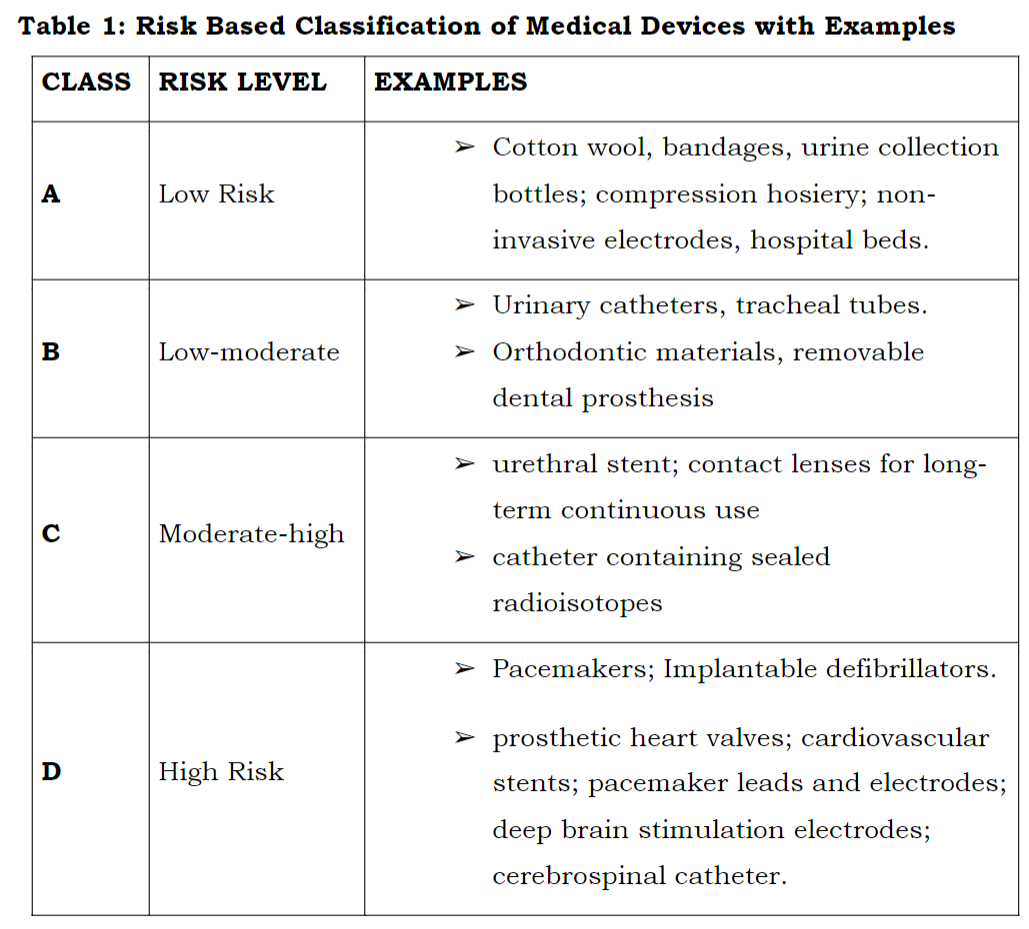
体外诊断试剂(IVD)产品同样按风险等级分为Class A、Class B、Class C和Class D四类:
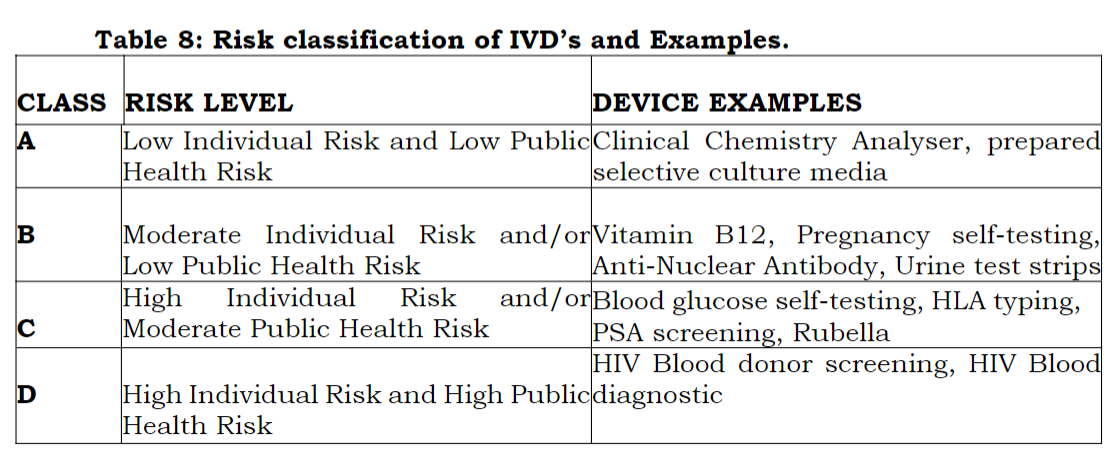
① 提供有效的ISO 13485质量管理体系证书;
② 委任一位肯尼亚当地授权代表(LAR);
③ 提交完整注册文件:行政信息、产品分类信息、符合性声明草案、风险管理报告、临床评估报告、上市后监督(PMS)及上市后临床随访(PMCF)计划等。
英语
肯尼亚境外制造商必须指定一位当地授权代表(LAR),负责与PPB进行所有注册相关的沟通。制造商需提供书面授权书明确授权代表的权利与职责。
一个制造商在肯尼亚针对同一产品线或产品组合只能指定一个授权代表。
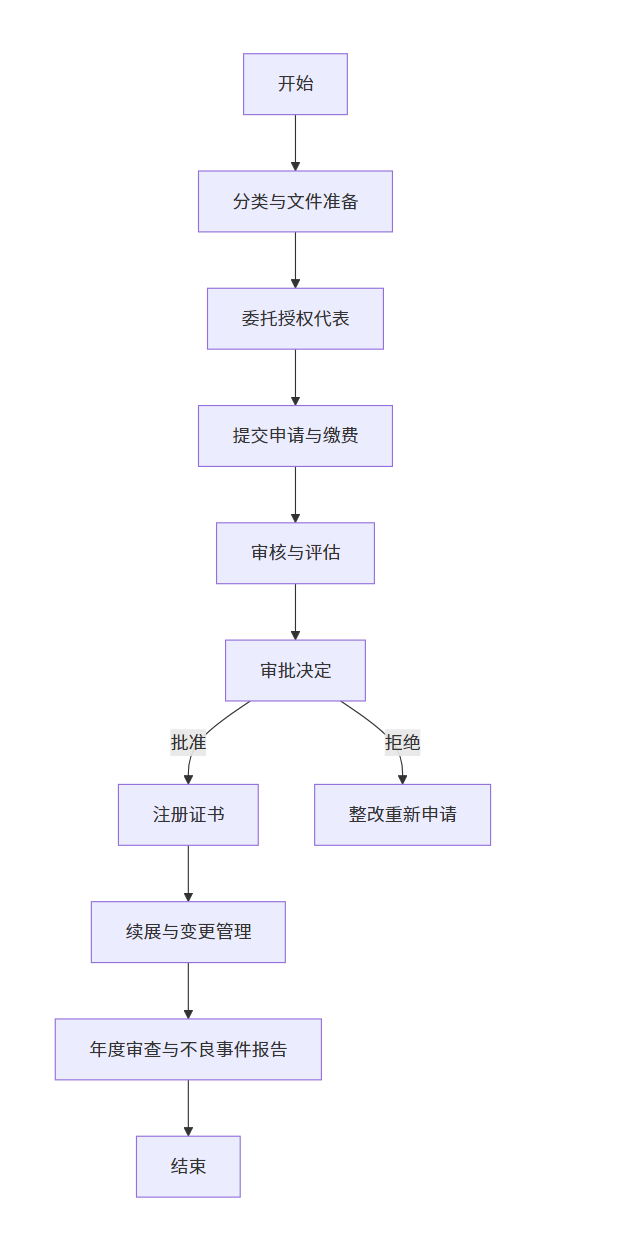
标准流程:产品风险分类与注册文件准备→委托肯尼亚当地授权代表→通过CSDT模板提交注册申请并缴纳官费→PPB开展技术审核与评估→作出审批决定(批准颁发注册证书/拒绝并说明理由)→注册后进行续展与变更管理,同时履行年度审查与不良事件报告义务。
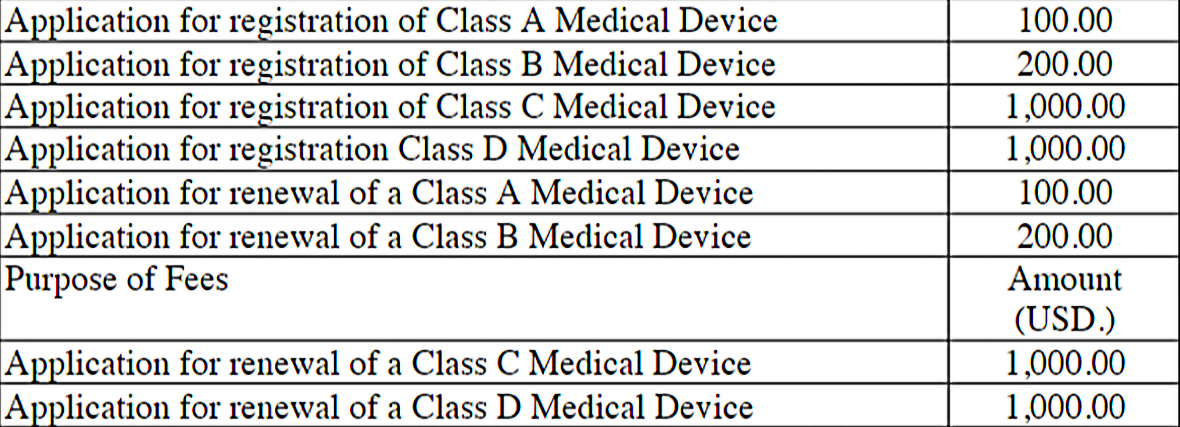
| 业务类型 | Class A | Class B | Class C | Class D |
|---|---|---|---|---|
| 首次注册申请 | 100.00 | 200.00 | 1,000.00 | 1,000.00 |
| 注册续展申请 | 100.00 | 200.00 | 1,000.00 | 1,000.00 |
新注册(含完整评估和简化评估流程)常规周期约12个月(基于Wiselink实际项目经验)。