2025年8月22日,墨西哥卫生部通过联邦健康风险防护委员会(COFEPRIS)发布《关于简化联邦健康风险防范委员会程序的协议》(刊登于墨西哥《联邦官方公报》DOF ),该协议对医疗器械、药品等相关产品办理注册的流程、优化材料、压缩审评时限做出系统性调整,并设置明确的过渡期与信息化要求。本文将简单为您介绍协议的核心内容。
https://www.dof.gob.mx/nota_detalle.php?codigo=5766390&fecha=22/08/2025#gsc.tab=0
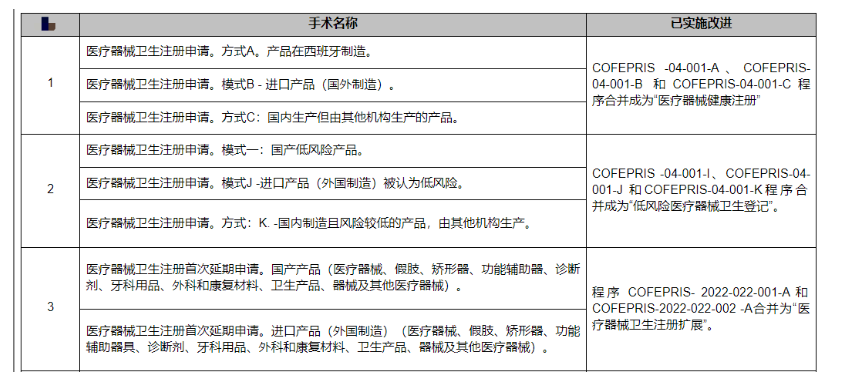
将COFEPRIS-04-001-A、COFEPRIS-04-001-B和COFEPRIS-04-001-C流程合并为“医疗器械卫生注册”。将COFEPRIS-04-001-I、COFEPRIS-04-001-J和COFEPRIS-04-001-K流程合并为“低风险医疗器械卫生登记”。将COFEPRIS-2022-022-001-A和COFEPRIS-2022-022-002-A流程合并为“医疗器械卫生注册延期”。
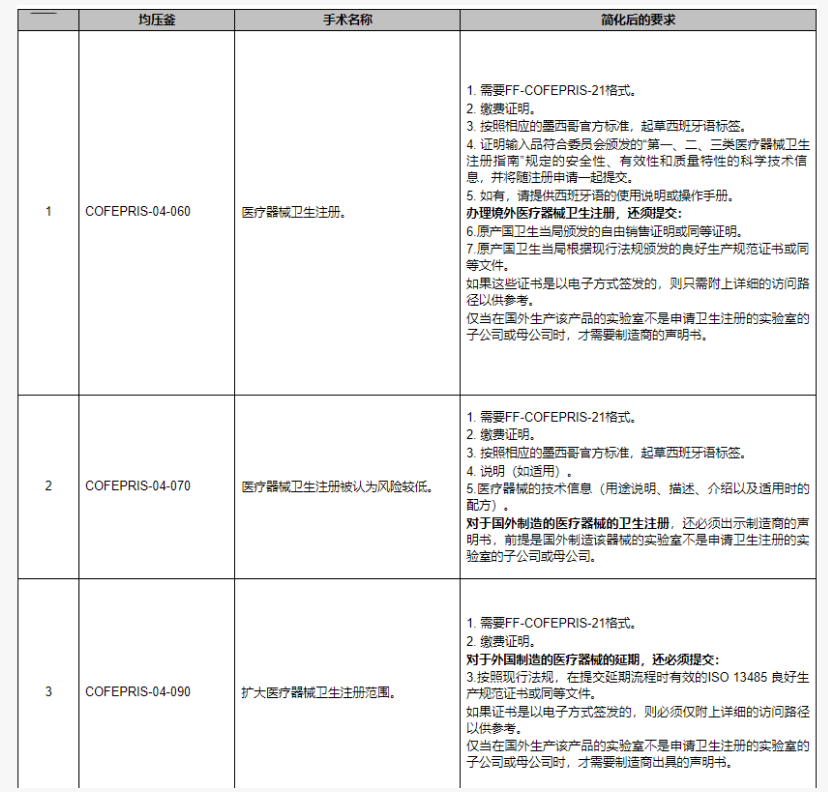
(1)统一使用 FF-COFEPRIS-21(器械相关)/ FF-COFEPRIS-22(药品相关)等表格与缴费凭证;(2)提交墨西哥官方标准的西班牙语标签/说明书草案及必要的技术资料(安全、质量与有效性信息);(3)GMP/ISO 等合规证书如由原产国当局或认可机构以电子方式签发,可仅提交可核查的访问路径或等效参照;(4)境外制造时,仅当境外工厂与申请实验室不存在母子公司关系时,才需提交制造商代表函(carta de representación);(5)COFEPRIS不得要求其自身签发文件、简单复印件或本协议之外的额外材料;首次证明法人资格或变更法定代表人时,才需提交法律授权与身份证明;(6)申请人须完整填报必填字段,表格由COFEPRIS官网发布。
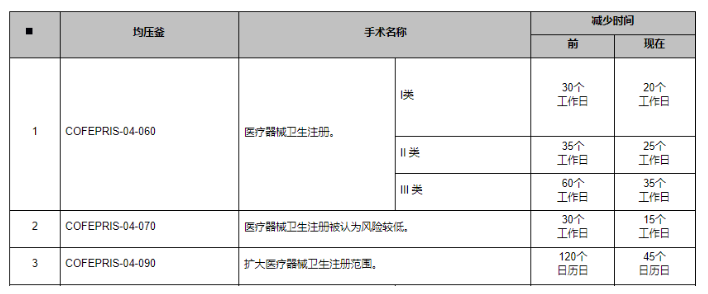
(1)COFEPRIS-04-060 医疗器械卫生注册(2)COFEPRIS-04-070 低风险医疗器械卫生登记
生效时间:自DOF刊登之日起30个工作日后生效并按本协议办理。以上四类自刊登之日起180个工作日后生效,须等待COFEPRIS系统与平台完成调整。
本次COFEPRIS改革以“流程合并 + 材料减负 + 时限压缩”为主线,既提升办事确定性,也显著缩短上市周期。对企业而言,最直接的收益是审批周期显著缩短、重复资料大幅减少。未来在墨西哥的市场准入将更加高效和透明。
- 跨境注册战略的重新布局(尤其是依赖FDA等通道的企业)
可以说,本次COFEPRIS简化协议既是挑战,也是机遇。谁能率先适应新规,谁就能抢占墨西哥乃至拉美市场的先机。