2025年8月,美国FDA正式发布了《Animal Studies for Dental Bone Grafting Material Devices - Premarket Notification (510(k)) Submissions》(牙科骨移植材料器械的动物研究 - 上市前通知 (510(k)) 提交),为制造商在510(k)注册中如何设计和提交动物实验数据提供了最新指引。本次指南适用于牙科骨移植材料类器械,旨在帮助相关企业提升申报合规性和效率。
https://www.fda.gov/regulatory-information/search-fda-guidance-documents/animal-studies-dental-bone-grafting-material-devices-premarket-notification-510k-submissions
监管基础:根据《联邦食品药品与化妆品法》(FD&C Act),FDA将部分牙科骨修复材料从III类(需PMA批准)重新分类为II类(特殊管制),如羟基磷灰石、磷酸三钙、聚乳酸/聚乙醇酸及胶原材料。特殊管制要求:2005年FDA已发布《Dental Bone Grafting Guidance》,明确了材料表征及体内性能验证要求。此次新指南进一步细化了动物实验的推荐设计与实施规范。
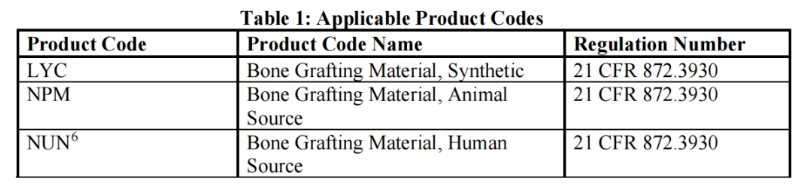
本指南适用于 21 CFR 872.3930 下的牙科骨移植材料,具体产品代码包括:
- 去矿化骨基质(DBM,最小处理或含防腐剂等添加剂的情况除外)
(1)推荐模型:成体犬或猪,更接近人类牙槽骨解剖结构;不推荐啮齿类(骨持续生长、模型局限性大)。(2)应用场景:必须与拟申报适应症匹配,例如用于牙槽嵴增量、囊肿切除后缺损填充等,需在口腔颌面部模型中验证。(1)样本量与分组:每组至少3只动物,随机化设置;需包括测试材料、对照材料(同类已上市产品或自体骨移植)及空白对照。(2)最坏情况测试:选择临床最严苛的缺损模型(如1壁/2壁关键缺损),以及材料形态中的“最不利条件”(最大尺寸、最低密度等)。(3)关键缺损模型(Critical Size Defect):缺损应保证在无处理条件下不会自发愈合,用于验证材料的真实骨生成能力。(4)愈合周期:拔牙模型需先愈合3-6个月再造缺损;实验持续至少12周,建议设多个时间点(如4、8、12周),必要时延长至26周。
- 组织学:HE染色、Masson染色,确认新骨形成与炎症反应
- 组织形态学定量:测量新骨比例、材料残留量、纤维组织比例
动物实验可同时覆盖 ISO 10993-6 植入局部效应试验,减少动物使用。但需区分数据呈现,将“器械性能评价”与“生物相容性评价”分别列出。
3R原则:FDA鼓励替代、减少和优化动物使用,若拟采用非动物方法,应通过Q-Submission程序提前沟通。数据质量:需提交完整的实验设计、动物信息、影像与组织学图像(彩色、带标注),确保可重复和无偏差。申报建议:制造商可通过Pre-Submission机制提前与FDA确认实验设计,避免因模型或方案不符合要求而导致补充材料。
提前规划注册路径:尤其是涉及创新材料(如复合骨移植材料)的企业,应结合FDA要求设计动物实验。关注模型科学性:不再接受单纯引用对照产品数据或啮齿类模型,必须有口腔颌面部相关的动物研究。提升研发效率:通过结合ISO 10993-6等试验,减少重复试验,降低成本和周期。合规数据积累:完整的影像、组织学和定量分析数据,将成为FDA审查的关键证据。
本指南标志着FDA对牙科骨移植材料的监管要求更加精细化和临床相关化。制造商在510(k)申报过程中,需高度重视动物实验的科学性与合规性,提前布局研发与注册策略,才能顺利应对监管审查,加快产品上市。