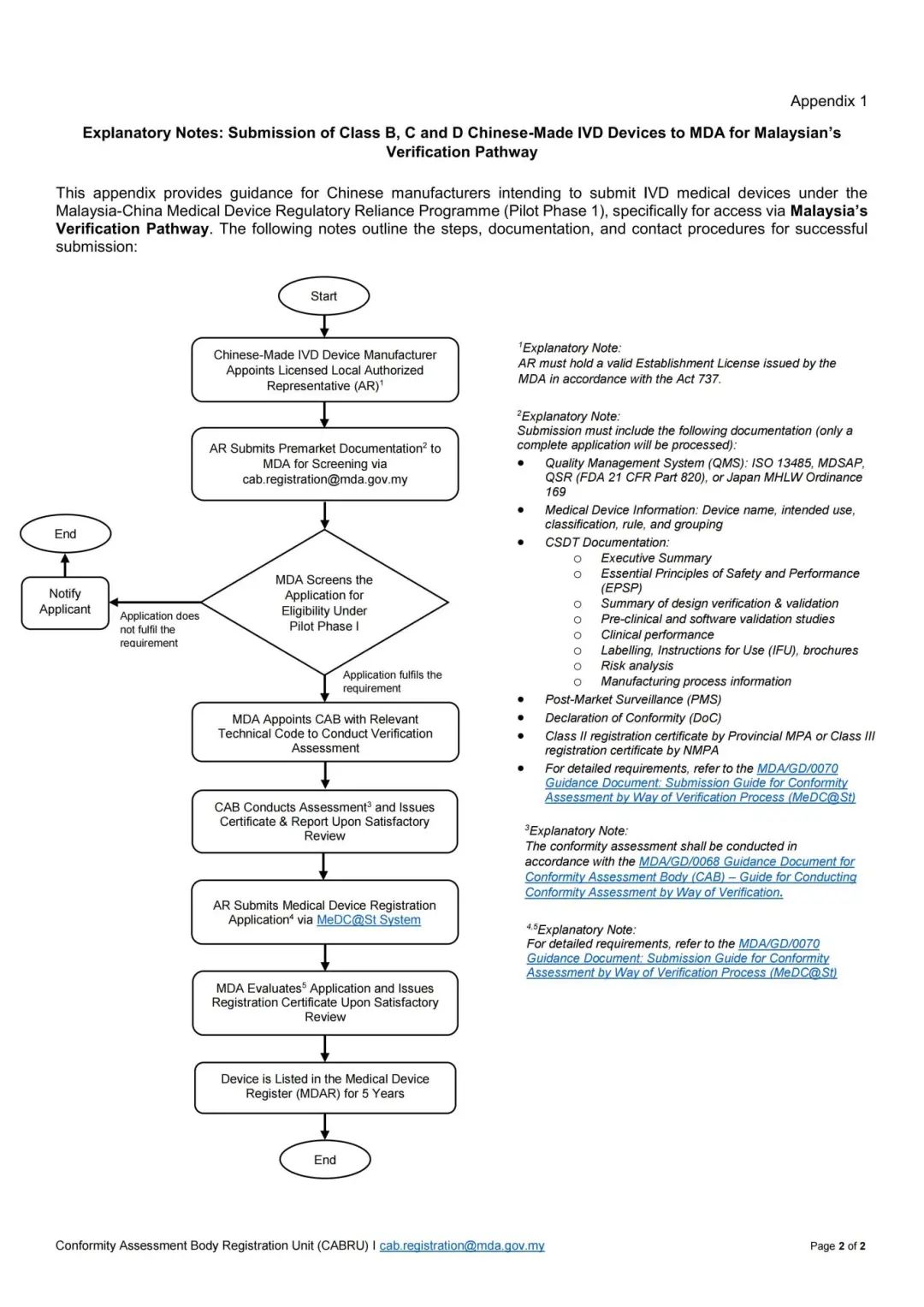
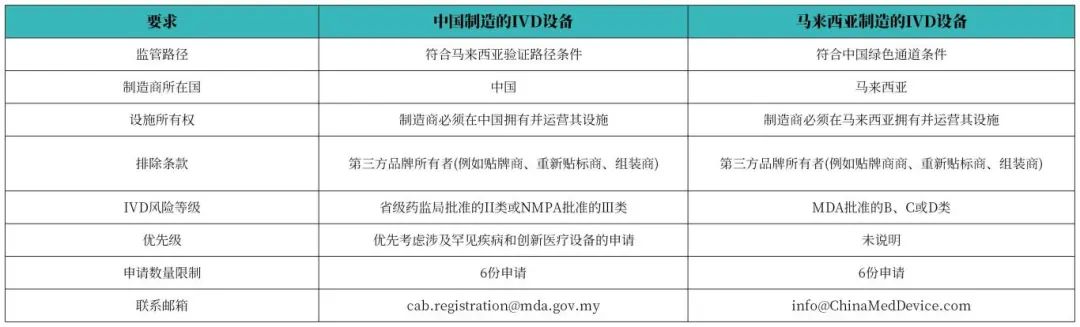
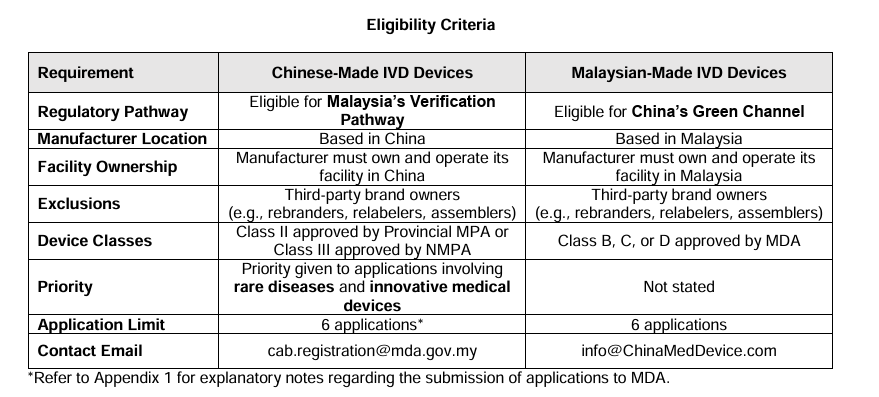
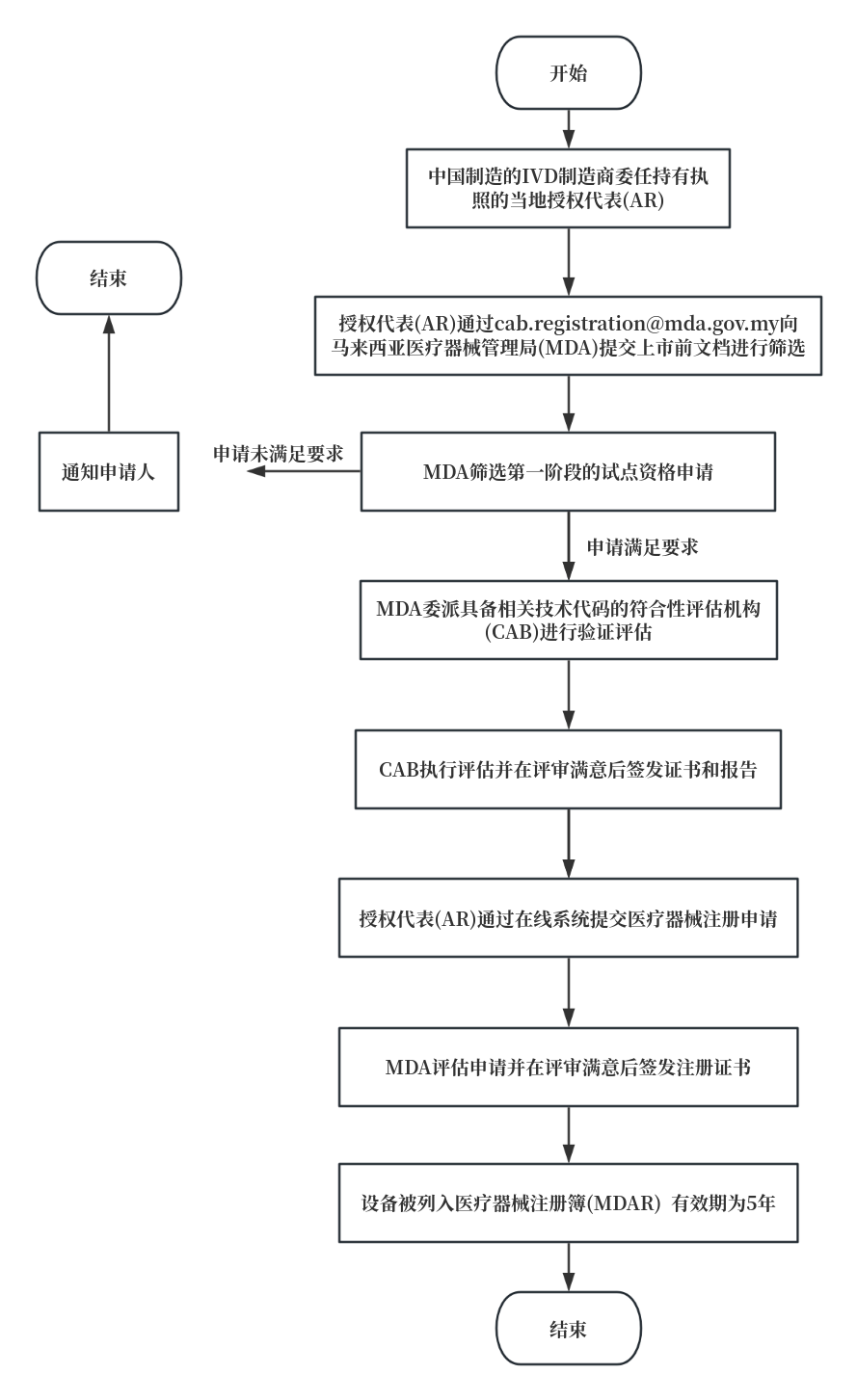
2025年7月30日,中国NMPA与马来西亚MDA正式启动了医疗器械监管互认计划试点阶段。 该计划的试点阶段一将于2025年7月30日至9月30日开展,仅60天!聚焦于IVD产品,旨在通过双方监管合作,提升审评效率,推动相关产品更快速进入中马两国市场。本文知汇将为您带来此公告的详细内容介绍。 https://portal.mda.gov.my/index.php/documents/ukk/3707-implementation-of-the-malaysia-china-medical-device-regulatory-reliance-programme-pilot-phase-i-30072025-2/file 该计划的试点阶段一将于2025年7月30日至9月30日开展,仅60天! 授权代表(AR)必须持有马来西亚医疗器械管理局(MDA)根据《Act 737》签发的有效机构许可证(Establishment License)。同时提交时必须包含以下文件(仅完整的申请才会被受理): 质量管理体系(QMS)文件:ISO 13485、MDSAP、QSR(美国 FDA 21 CFR 第820部分),或日本 MHLW Ordinance 169 医疗器械信息:包括器械名称、预期用途、分类、法规条款及分组信息 CSDT 技术文档,包括: 上市后监测(PMS)计划 符合性声明(DoC) 中国省级药监局签发的 Class II 注册证书或国家药监局(NMPA)签发的 Class III 注册证书 中马IVD医疗器械监管互认计划试点阶段一已正式启动,企业可借助该机制加速获证、节省成本,抢占马来西亚市场先机!但请注意,本次试点仅开放60天,时间紧迫,建议有注册需求的企业尽快行动。如需马来西亚注册支持,欢迎联系Wiselink知汇团队。 Wiselink拥有包括原澳大利亚药品监督管理局局长Dr. Derrick Beech为首席顾问的国际专业团队,秉承源于澳洲、扎根中国、服务世界的精神,信守专业、真诚、开放的核心价值观,致力于为医疗器械、化妆品、食品、保健品和中药制造商提供全球合规认证和临床试验服务。
○ 执行摘要
○ 安全与性能基本原则(EPSP)
○ 设计验证与确认的总结
○ 软件和临床验证研究
○ 临床性能资料
○ 标签、使用说明书(IFU)、宣传册等
○ 风险分析
○ 生产工艺信息