


FDA最新发布关于2026财年(2025年10月1日-2026年9月30日)医疗器械注册各项收费标准,大家最为关心的具体费用变化信息如下文所示:
https://www.fda.gov/industry/fda-user-fee-programs/medical-device-user-fee-amendments-mdufa-fees
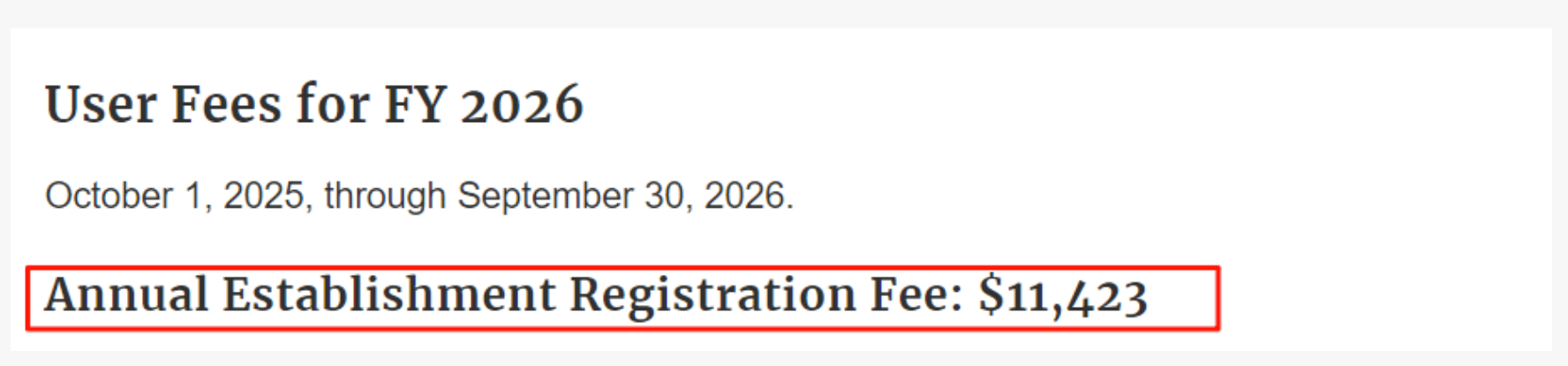
2026财年企业注册的年费为11,423美元,2025财年为9,280美元,涨幅为23.1%。
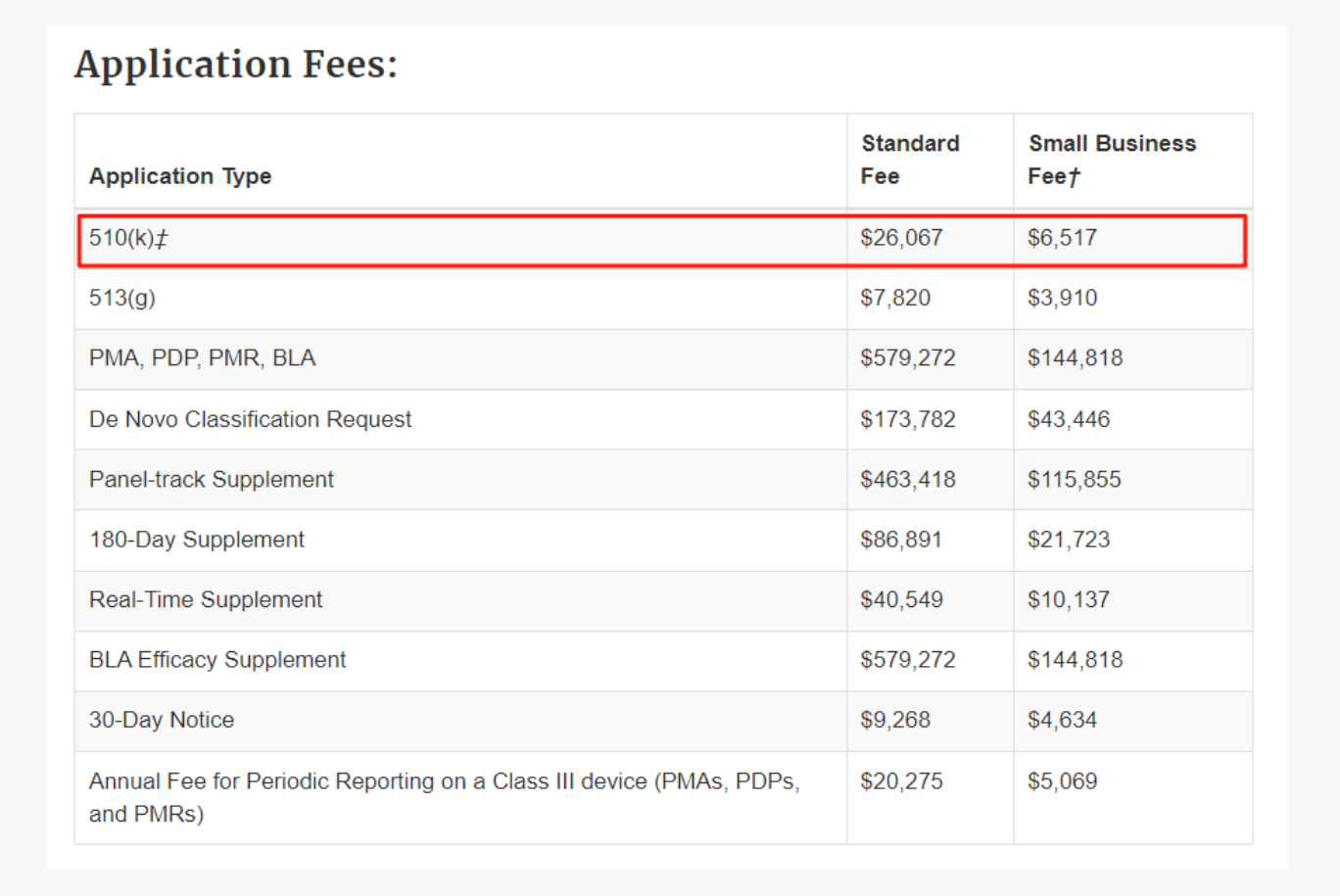
2026财年510(k)审批费为26,067美元,2025财年为24,335美元,涨幅为7.1%。
2026财年申请了小企业资质的510(k)的费用是6,517美元。
原文内容:
2026财年,FDA可能会对符合小型企业认定 (SBD) 计划条件的某些小型企业免除年度企业注册费(不包括首次注册费),前提是这些小型企业能够证明缴纳该费用会导致FDA认定的财务困难。
提交小型企业申请 (SBR): CDRH 的 SBD 项目负责确定企业是否符合“小型企业”的资格,并确定某些类型的 CDRH 申请是否有资格享受费用减免。
降低费用:通过 SBD 计划获得资格的小型企业,如果总收入或销售额不超过 1 亿美元,则有资格享受以下方面的降低费用:
上市前通知(510(k));
De Novo 请求;
上市前申请(上市前批准申请(PMA);
生物制品许可申请(BLA);
产品开发协议(PDP);
上市前报告(PMR);
PMA/BLA 补充;
PMA 年度报告;
513(g)分类信息请求。
申请豁免:通过 SBD 计划获得资格的小型企业,如果总收入或销售额为 3000 万美元或以下,则有资格免除其首次上市前批准申请 (PMA)、产品开发协议 (PDP)、上市前报告 (PMR) 或生物制品许可申请 (BLA) 的费用。
Wiselink拥有包括原澳大利亚药品监督管理局局长Dr. Derrick Beech为首席顾问的国际专业团队,秉承源于澳洲、扎根中国、服务世界的精神,信守专业、真诚、开放的核心价值观,致力于为医疗器械、化妆品、食品、保健品和中药制造商提供全球合规认证和临床试验服务。


