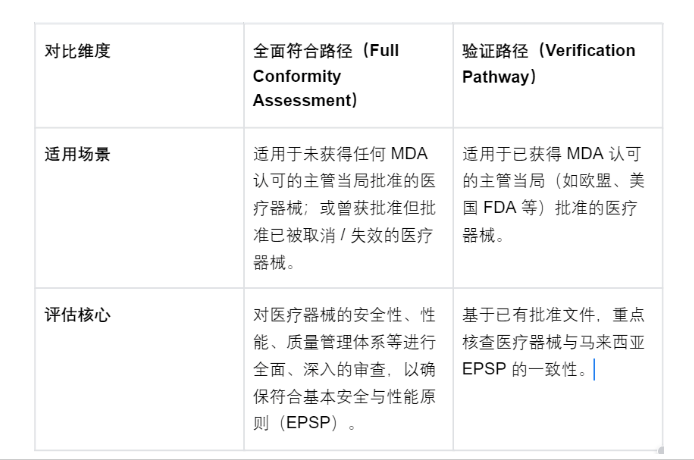
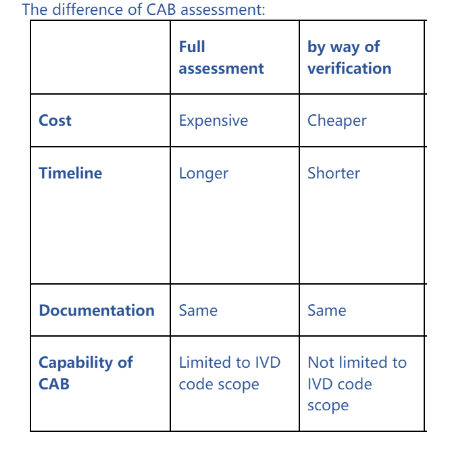
相信大家最近的朋友圈都被一条关于中马医疗器械互认协议的资讯刷屏了吧?知汇也不例外,发布了一篇文章《IVD重大利好!中马医疗器械监管互认协议:7月30日生效,审批时间降至30个工作日!》。文章发布后,许多业内人士和客户朋友纷纷向知汇咨询相关问题。大家最关心的一个问题,莫过于:这项协议是否仅适用于体外诊断(IVD)产品,还是涵盖了普通医疗器械? 看到如此多的朋友前来咨询,小编虽然相信自己内容的准确性,但为了给广大客户和读者们提供准确的答案,知汇团队特地与马来西亚MDA官方进行了电话沟通。经确认,7月30日生效的中马医疗器械互认协议,对双方而言,都仅限于体外诊断(IVD)产品,不包括普通医疗器械。正如知汇在上一篇的文章所写: 关于是否会在未来涵盖普通医疗器械,知汇将继续关注马来西亚官方发布的最新信息,并及时为大家更新。 本篇文章,知汇将针对原文中提到的“Chinese devices may use Malaysia's Verification Pathway”,从“全面符合路径”(FulI Conformity Assessment))和“验证路径”(Verification Pathway)两个方面为大家介绍关于马来西亚医疗器械注册的知识。 以下是CAB机构对于两种路径的评估: 接下来,知汇将给大家分享关于这两种不同路径的FAQ: 1. 什么是验证路径的符合性评估? 验证路径是马来西亚医疗器械管理局(MDA)为已获得 MDA 认可主管当局上市批准的医疗器械设立的简化符合性评估流程。其目的是精简注册流程并缩短符合性评估时间,这一流程在 2025 年第 1 号 MDA 通函中有相关规定。该路径通过核查器械是否符合安全与性能基本原理(EPSP),基于其在认可地区已有的批准文件开展评估。 2. 哪些医疗器械符合验证路径的要求? 初始认证评估的合格条件包括: 已获得至少一个 MDA 认可主管当局的批准(本次互认原则,就是将中国纳入参考国); 在马来西亚的设计和预期用途与获批版本一致。 重新认证评估的合格条件包括: 该器械此前已通过全面评估或验证路径在 MDA 完成注册; 重新认证前持有有效的注册证书; 未发生设计、规格或注册相关信息的变更(除非已通知 MDA); 注册未被 MDA 驳回或撤销。 3. 验证路径需要提交哪些符合性证据? 证据需证明符合 EPSP,包括四大核心要素: 质量管理体系(QMS)文件; 上市后监督(PMS)系统记录; 技术文档; 符合性声明(DoC)。 这些材料需按照《通用提交档案模板(CSDT)》整理。 4. 符合性评估机构(CAB)在验证路径中扮演什么角色? 机构(制造商或授权代表)必须委托具有相关医疗器械技术领域专业知识的注册 CAB 开展验证评估。CAB 会审核符合性证据,核查是否符合 EPSP,并出具评估报告和符合性证书,这些是后续注册申请的必要材料。 5. 验证路径与全面符合性评估路径有何区别? 验证路径:适用于已获 MDA 认可机构批准的器械,重点核查与 EPSP 的一致性,CAB 评估时间约为 1.5 个月。 全面评估路径:适用于未获认可机构批准的器械,需对安全性和性能进行更全面的评估。 6. 哪些医疗器械不适用验证路径? 通过特殊紧急或同情使用计划授权的器械(如欧盟 “Exceptional Use Authorization”、美国 FDA EUA、澳大利亚 SAS)不适用。这些计划为危急情况下的未获批器械提供临时市场准入,不符合验证要求。 7. 验证路径的时间周期是多久? CAB 完成验证评估的总时间约为 1.5 个月,涵盖文件审核、认证决定和证书发放等阶段(详见附件 2)。CAB 批准后,通过 MeDC@St 提交申请及 MDA 审核还需额外时间(B/C/D 类为 30 个工作日)。 8. 验证路径可用于重新注册吗? 可以。重新注册需满足:器械此前通过全面评估或验证路径注册、持有有效注册证书、无未通知的变更。重新注册申请通过 MeDC@St 提交,系统会在注册证书到期前 1 年显示 “重新注册” 按钮。 9. 完成验证路径后会怎样? CAB 确认器械符合 EPSP 后,需通过 MeDC@St 提交注册或重新注册申请。若 MDA 确认器械满足《2012 年医疗器械法》及相关法规的所有要求,将予以注册或重新注册,有效期为 5 年,并列入 MDAR(马来西亚医疗器械注册簿)。 1. 什么是全面符合性评估路径? 全面符合性评估路径是马来西亚医疗器械管理局(MDA)规定的一种符合性评估方式,适用于未获得 MDA 认可的主管当局上市批准的医疗器械。该路径通过全面评估器械的安全性、性能及对法规要求的符合性,确保其满足《2012 年医疗器械法》(Act 737)及相关条例的要求,是器械注册前的必要环节。 2. 哪些医疗器械需要通过全面符合性评估路径? 需适用全面评估的医疗器械包括: 未获得任何 MDA 认可的主管当局(如欧盟、美国 FDA、澳大利亚 TGA 等,详见附件 1)上市批准的器械; 虽曾获认可主管当局批准,但该批准已被取消或失效的器械。 3. 全面符合性评估与验证评估(Verification)的核心区别是什么? 两者的核心区别体现在适用场景和评估范围上: 适用场景:全面评估适用于未获认可当局批准的器械;验证评估适用于已获认可当局批准、满足上市时间及安全要求的器械。 评估范围:全面评估需对器械的安全性、性能、质量管理体系等进行更全面、深入的审查;验证评估则基于已有批准文件,重点核查与马来西亚基本安全与性能原则(EPSP)的一致性。 4. 全面符合性评估需提交哪些材料? 需提交的核心材料包括证明器械符合基本安全与性能原则(EPSP)的完整证据,具体涵盖: 质量管理体系(QMS)相关文件(如 ISO 13485 证书); 上市后监督体系(PMS)记录; 详细技术文档(包括设计验证与确认数据、临床证据、风险分析等); 符合性声明(DoC); 按《通用提交档案模板(CSDT)》整理的所有材料 5. 全面符合性评估的流程是怎样的? 流程主要包括以下阶段: 委托 CAB:制造商或授权代表需委托具有相关医疗器械技术领域资质的注册符合性评估机构(CAB)开展评估; 材料提交与审查:向 CAB 提交完整的符合性证据,CAB 对材料进行全面审查与评估; 出具评估报告与证书:CAB 完成评估后,向申请方出具符合性评估报告及证书; 提交注册申请:凭 CAB 报告及证书,通过 MeDC@St 系统向 MDA 提交注册申请,进入后续审核流程。 6. 全面符合性评估的时间周期是多久? 由注册的 CAB 开展的全面符合性评估整体周期约为 2 个月(不包含申请方准备材料的时间)。完成评估后,向 MDA 提交注册申请的审核时间为 30 个工作日(适用于 Class B、C、D)。 7. 哪些医疗器械必须通过全面符合性评估路径? 主要包括两类: 未获得任何 MDA 认可的主管当局(如欧盟、美国 FDA、澳大利亚 TGA 等,详见附件 1)上市批准的医疗器械; 虽曾获认可主管当局批准,但该批准已被取消或失效的医疗器械。 8. 全面符合性评估适用于重新注册吗? 通常情况下,全面符合性评估主要适用于初始注册阶段。重新注册的器械若此前通过全面评估或验证路径注册,且满足无设计 / 规格变更、注册证书有效的条件,可通过验证路径进行重新注册评估,而非再次进行全面评估。 9. 全面符合性评估与 CAB 的关系是什么? 全面符合性评估必须由 MDA 注册的符合性评估机构(CAB)执行。CAB 需具备相关医疗器械技术领域的专业能力,按照 MDA 规定的流程和标准开展评估,确保评估结果的客观性和合规性。评估完成后,CAB 出具的报告及符合性证书是向 MDA 提交注册申请的必要材料。 10. 全面符合性评估的结果如何影响注册? 只有通过全面符合性评估,且 CAB 确认器械符合 EPSP 及相关法规要求后,申请方可向 MDA 提交注册申请。若评估未通过,需根据 CAB 意见补充材料或整改,否则注册申请将被拒绝。