

随着欧盟《医疗器械法规》(MDR 2017/745)实施,欧洲市场的医疗器械行业正在推动实施唯一设备标识(UDI)系统。
该系统旨在确保医疗器械的足够识别性和可追溯性。根据MDR第27条规定,除定制设备外,所有医疗器械在投放市场前必须分配并注册唯一设备标识(UDI)。为进一步增强UDI的追溯性,制造商需在欧洲医疗器械数据库(Eudamed)中注册基本UDI-DI和UDI-DI。
https://health.ec.europa.eu/document/download/ad6ae143-baa2-451a-8c5e-0c5d22983e88_en?filename=mdcg_2025-7_en.pdf
“高度个性化设备”是指那些具有特定个性化设计,且不属于常规设备范畴的产品。例如:
隐形眼镜
眼镜框
眼镜镜片
现成老花镜
欧盟为这些设备提供了“Master UDI-DI”技术方案,允许将设计参数相似的设备组合在一起,共用一个UDI标识。这不仅能简化产品的追溯过程,还能减轻制造商、分销商以及Eudamed数据库的负担,避免了为每个相似产品单独分配UDI的繁琐程序。

根据欧盟最新法规,针对这些设备,以下是实施的关键时间节点:
UDI标签要求:
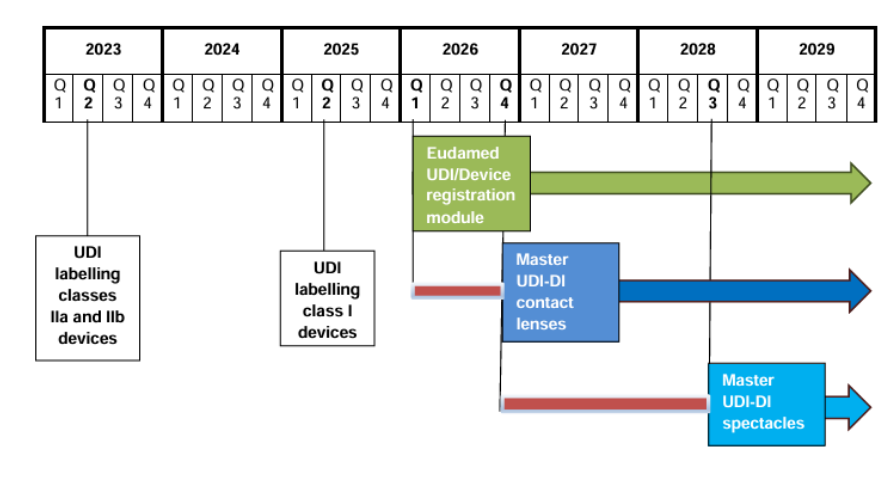
IIa和IIb类设备:从2023年5月26日起,必须在设备及其所有包装上进行UDI标签标识。
I类设备:自2025年5月26日起,UDI标签要求生效。
Eudamed设备注册模块强制启用:
根据MDR第29条和第123条,Eudamed的UDI/设备注册模块将在2026年第一季度强制启用。制造商必须在此后使用该模块进行设备的注册和管理。
隐形眼镜的Master UDI-DI实施:
根据《委员会授权法规(EU)2023/2197》,隐形眼镜的Master UDI-DI解决方案要求制造商从2026年11月9日起开始实施。自该日期起,所有新生产的隐形眼镜必须在标签上标明Master UDI-DI。
眼镜框、眼镜镜片和现成老花镜的Master UDI-DI实施:
对于眼镜框、眼镜镜片和现成老花镜,Master UDI-DI解决方案的实施要求制造商从2028年9月起开始实施。
时间节点图:
在规定的强制实施日期前,欧盟允许制造商自愿实施Master UDI-DI。制造商应尽早在设备上标注Master UDI-DI并进行Eudamed注册。这样做将有助于:
提早适应新规,确保合规性;
利用Master UDI-DI所带来的便利,例如简化的追溯和报告功能。
特别是对于隐形眼镜、眼镜框等设备,建议制造商在法定强制要求前,尽早开始分配并实施Master UDI-DI。这不仅有助于满足监管要求,还能帮助企业在市场竞争中抢占先机。
Eudamed(欧洲医疗器械数据库)是欧盟在医疗器械监管中至关重要的平台。制造商需要通过该平台提交其设备的UDI信息,确保设备的可追溯性。
自2026年起,所有设备(包括高度个性化设备)都必须通过Eudamed进行注册。随着系统逐步完善,Eudamed将成为设备生命周期管理的核心工具,包括但不限于:
设备注册
警戒和市场后监管(vigilance)报告
临床数据提交
随着欧盟逐步推进UDI系统,隐形眼镜、眼镜框等高度个性化设备将面临更加严格的监管要求。制造商应密切关注相关法规的实施时间表,提前准备并采取行动。为了避免延误并降低合规风险,Wiselink知汇建议相关医疗器械制造商:
提前在设备上标注Master UDI-DI;
积极注册并使用Eudamed的UDI/设备注册模块;
关注法规实施的具体要求与时间节点,确保符合监管要求。
通过这些举措,制造商不仅能符合欧盟的合规要求,还能在市场上赢得更多的信任与机会。