

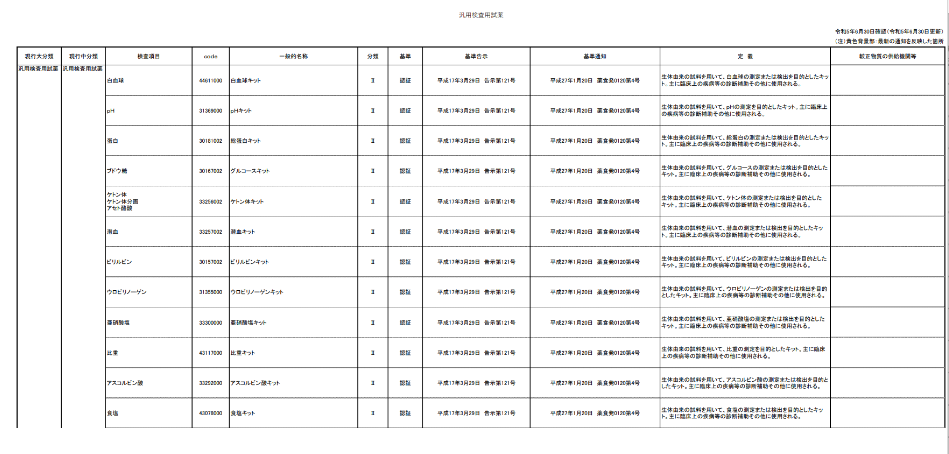
在全球医疗市场中,日本作为发达国家之一,一直以丰厚的利润和高监管要求而著称。因此,日本对体外诊断用医药品(IVD)的注册和管理有着严格且细致的规定,对于希望进入日本市场的IVD企业而言,了解和遵循这些流程和要求至关重要。本文知汇将详细为您解析日本IVD的注册流程、分类和具体要求,帮助您顺利进入这一市场。 想要出口IVD产品到日本,首先您需要有一个在日本取得相应资质的合规代理人。Wiselink Group日本子公司【Wiselink JP株式会社】已经取得了“体外診断用医薬品製造販売業許可証”和“体外診断用医薬品製造業登録証”两项重要资质,正是IVD制造商选择日本合规代理人的完美选择! “体外診断用医薬品製造販売業許可証”:这项许可证赋予了Wiselink JP株式会社在日本进口体外诊断用医药品和产品上市的合法资格。它是公司在日本开展IVD产品销售和市场推广的基础。 “体外診断用医薬品製造業登録証”:这张注册证是Wiselink JP株式会社在日本制造和保管体外诊断用医药品的合法认证,确保产品符合严格的质量管理和安全标准。 这两项资质不仅是Wiselink在日本本地合规运营的体现,也是我们为全球客户提供更好服务的标志。 IVD在日本注册所需要的流程和医疗器械注册流程一样。 1. 外国制造商登录 作为注册流程的第一步,厂家首先需要在日本进行外国制造商的正式登陆,确保企业的基本信息在日本监管机构中备案。 2. 获得进口商资质 进口商需要获得“体外診断用医薬品製造販売業許可”,并配置相应的专业人员,包括至少1位药剂师作为总括责任人,1位具有3年品管经验的品质管理人,以及1位安全管理人员。 3. 进行制造业登记 涉及IVD产品的保管与验货环节,需进行“体外診断用医薬品製造業登録”,并需要1位药剂师作为管理人。 4. 产品分类及审查 体外诊断用医药品是指专门用于疾病诊断的药品,并且这些药品不直接用于人体或动物体内。根据这一定义,体外诊断用医药品被分类为不同的“I” 类“II”类 “III”类,并根据类别进行制造和销售的规制。简而言之,则是: “I” 类 IVD需要“备案” “II”类 IVD需要“认证” “III”类 IVD需要“承认” 类别 I 1. 判断方式: 用于疾病诊断时,其诊断信息风险较小,信息准确性对生命维持的影响相对于类别Ⅲ的项目较小,并且具有校准标准物质或标准测量方法,且自检较为容易。注意,不包括一般用检测试剂(OTC)。 2. 审查方式: 自我认证(制造和销售报告),对于类别 I ,符合不需要批准或认证标准(根据《药品、医疗器械等质量、安全性及有效性保证法》第23-2-5第1项制定的标准)的产品,采用报告制度。 类别 II 1. 判断方式: 用于疾病诊断时,其诊断信息风险较小,信息准确性对生命维持的影响相对于类别Ⅲ的项目较小,以及一般用检测试剂(OTC)。 2. 审查方式: 注册认证机构(制造和销售认证),对于类别 II,符合认证标准(根据《药品、医疗器械等质量、安全性及有效性保证法》第23-2-23第1项制定的标准)的产品,需通过厚生劳动大臣注册的认证机构(注册认证机构)进行认证。 类别 III 1. 判断方式: 用于疾病诊断时,其诊断信息风险较大,信息准确性对生命维持的影响较大。 2. 审查方式: 厚生劳动省(制造和销售承认),对于类别 III,以及不符合上述1或2的产品,由独立行政法人医药品医疗器械综合机构进行承认审查。 注意:如果产品不符合标准,则需要申请“承认”。 1. 新品项:试图检测或测量的新产品 2. 承认标准外的品项:没有承认标准的产品 3. 符合承认标准品项:有承认标准且符合承认标准的产品。根据《体外诊断用医药品向一般用检测试剂的转用》(平成26年12月25日药食发1225第1号厚生劳动省医药食品局长通知)制定的指南申请承认的符合承认标准的一般用检测试剂 4. 不符合标准品项:有承认标准、认证标准(指根据《药品、医疗器械等质量、安全性及有效性保证法》第23-2-23第1项制定的标准)或不需要承认和认证标准(指根据《药品、医疗器械等质量、安全性及有效性保证法》第23-2-5项制定的标准)的产品,但不符合上述两项标准的产品 日本医疗器械命名法 (JMDN) 由厚生劳动省官方公报公布。JMDN的优势在于,IVD企业一旦确定自己的IVD产品适用的 JMDN,IVD 注册途径、分类和适用的报告、认证、承认等标准将自动确定。由于该文件仅提供日文版本,因此您需要熟悉日语且了解JMDN中各种细微差别的专业人士的帮助才能找到正确的代码。 JMDN部分文件示例: 日本IVD注册流程虽然复杂,但遵循正确的步骤和要求,可以确保您的产品顺利进入这一重要市场。“体外診断用医薬品製造販売業許可証”与“体外診断用医薬品製造業登録証”资质的成功获取,不仅提升了Wiselink自身在日本市场的合规性,更能为广大客户提供更加高效的服务。 Wiselink将继续为全球IVD企业提供专业的合规认证等一站式服务。我们将在日本这个高监管的市场中,帮助更多企业顺利完成产品的市场准入,推动其业务发展。


Wiselink拥有包括原澳大利亚药品监督管理局局长Dr. Derrick Beech为首席顾问的国际专业团队,秉承源于澳洲、扎根中国、服务世界的精神,信守专业、真诚、开放的核心价值观,致力于为医疗器械、化妆品、食品、保健品和中药制造商提供全球合规认证和临床试验服务。