


根据英国最新的医疗器械法规要求,制造商必须提交定期安全更新报告(PSUR),以确保其设备在市场上的安全性和有效性。该报告涵盖设备的性能、市场表现以及风险评估等关键内容,确保设备持续符合监管要求。
2025年6月,英国卫生部发布文件《Standardised Format for Periodic Safety Update Report (PSUR)》,介绍了定期安全更新报告的标准格式要求。本篇文章,知汇将为您详细介绍这份文件的内容。
https://assets.publishing.service.gov.uk/media/68663d16e6557c544c74db7d/Standardised_format_for_periodic_safety.pdf
制造商的详细信息;
涉及的设备名称和基本UDI-DI(唯一设备标识符);
设备的UKCA标记或CE标记;
PSUR的版本号和参考编号;
数据收集时间范围;
目录。
这些信息有助于快速识别报告的版本和覆盖的设备,确保报告的完整性和透明度。
上次PSUR报告后采取的措施;
当前报告期内的变化或新采取的行动;
基于数据分析,是否影响了设备的利益风险比;
制造商是否采取了新的纠正措施来应对新识别的风险。
这一部分旨在为监管机构提供对设备整体受益风险的概述。
这一部分提供了详细的设备描述,包括:
设备的基本UDI-DI以及与之关联的设备名称;
设备的分类和预期用途;
设备的适应症、禁忌症和目标人群;
首次认证日期和市场投放日期;
设备是否仍在市场上销售,以及是否存在任何安全纠正措施(FSCA)。
制造商需明确说明相较于上次PSUR是否有设备变更,这对于比较和分析报告至关重要。
1. 销售量(Volume of sales):提供设备在英国(包括英格兰、苏格兰、威尔士及北爱尔兰)及全球的销售数据,按照年度和地区进行分列。这有助于评估设备在市场上的表现和使用频率。
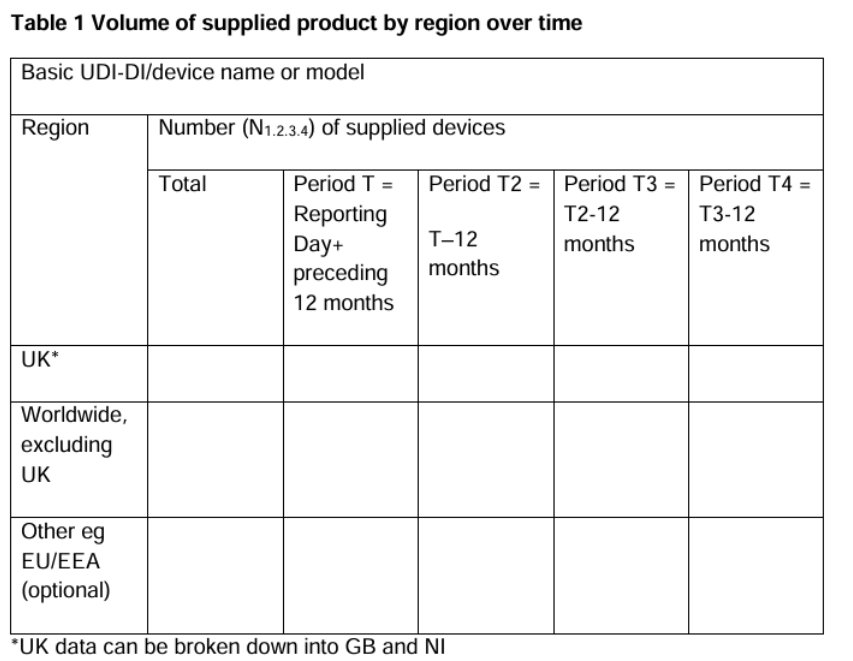
2. 使用人群的特征(Size and other characteristics of the population using the device):除了销售量,制造商还需提供关于设备实际使用情况的数据。这包括设备在特定人群(如老年患者或特殊病患群体)中的使用频率、植入设备的数量等。
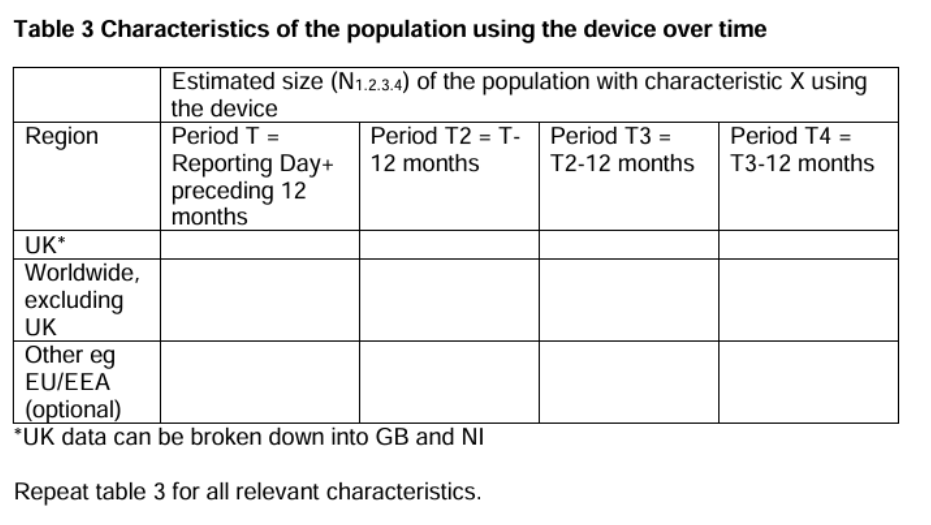
设备性能信息是PSUR的关键部分,涵盖了多方面的内容:
警示数据(Vigilance Data):包括严重事故报告、趋势数据以及现场安全纠正措施(FSCA)。需要展示设备的主要问题、根本原因和健康影响等。
主动数据分析(Proactive data analysis from defined populations):包括制造商主办的PMCF研究或注册库,独立的临床研究和文献综述,所有数据应与设备的后市场监控计划和PMCF计划相连接。
其他数据源(Data from other Sources including incidents not considered serious):这部分包括用户反馈、投诉数据和来自真实世界数据源(如电子健康记录、数字健康监测设备的数据等)。
对于任何设备存在的风险或不符合规定的情况,制造商必须提供已采取的预防与纠正措施(CAPA)。每个CAPA应包括:
受影响的设备型号;
措施的启动日期;
纠正措施的描述及根本原因分析;
当前状态(是否完成、进行中或待完成)。
在报告的最后,制造商需提供对设备的整体受益风险比的结论,并根据数据分析得出:
数据的有效性(Validity of the data):说明数据的有效性和限制因素,如销售或使用量的偏差,或PMCF研究的偏倚。
整体结论(Overall conclusions from data analysis):概述任何新的临床风险,识别的性能差异,以及设备是否实现了预期的效益。
采取的行动(Actions taken to address conclusions):如果设备的风险或性能问题发生了负面变化,制造商需详细说明已采取的纠正措施,以及实施的时间表。
Wiselink拥有包括原澳大利亚药品监督管理局局长Dr. Derrick Beech为首席顾问的国际专业团队,秉承源于澳洲、扎根中国、服务世界的精神,信守专业、真诚、开放的核心价值观,致力于为医疗器械、化妆品、食品、保健品和中药制造商提供全球合规认证和临床试验服务。