


2025年3月,随着《Therapeutic Goods Legislation Amendment (Australian Unique Device Identification Database and Other Measures) Regulations 2025》的发布,澳洲TGA宣布其唯一设备标识 (UDI) 监管框架正式生效。
链接:https://www.tga.gov.au/resources/legislation/therapeutic-goods-legislation-amendment-australian-unique-device-identification-database-and-other-measures-regulations-2025
澳大利亚政府正通过引入本国的医疗器械唯一标识(UDI)系统,进一步提升患者安全水平。该系统不仅强化了医疗器械的识别管理能力,还支持其他一系列监管改革,旨在优化整个医疗器械的监管体系,特别是在安全警示、产品召回等上市后安全管理方面的响应效率。
https://www.tga.gov.au/resources/guidance/complying-unique-device-identification-timeframes-medical-devices
从TGA认可的发证机构获取 UDI 设备标识符 (UDI-DI)
根据发行机构的要求,对 UDI 生产标识符 (UDI-PI) 进行格式化
由于医疗器械发生变化而导致医疗器械成为新型号(UDI Trigger)而需要获取新的 UDI-DI
在标签、包装和患者植入卡中纳入 UDI
在适用的情况下,对医疗器械直接标记UDI
在澳大利亚UDI数据库(AusUDID) 中提交 UDI-DI 和相关强制性数据的要求,包括提交数据的时间
澳大利亚TGA在其网站上提供了有关 UDI 标签要求的更多详细信息。TGA 的新指南《遵守医疗器械唯一设备标识要求》概述了获取和应用 UDI 的要求,以及在 AusUDID 中提交和维护 UDI 数据的要求。(如需原文资料,可以咨询小编)
除 I 类和 I (measuring) 类器械外,所有器械均须遵守这些 UDI 要求。I 类体外诊断器械 (IVD) 也不受此限制,除非其被视为仪器或软件。制造商可以选择为豁免器械分配并应用 UDI;如果这样做,TGA 建议满足所有 UDI 要求,以避免最终用户产生混淆。
UDI 合规开始日期是指您的设备必须符合澳大利亚 UDI 要求的日期。上述UDI要求的合规工作将分阶段实施,合规日期取决于取决于器械类别、该器械是否受欧盟医疗器械指令 (MDD) 或体外诊断指令 (IVDD) 支持,以及该器械是否在合规起始日期之前制造并贴标(即“现有器械”)。

TGA 发布了新指南《遵守医疗器械唯一设备标识时间表》,对这些日期进行了详细说明,具体如下:
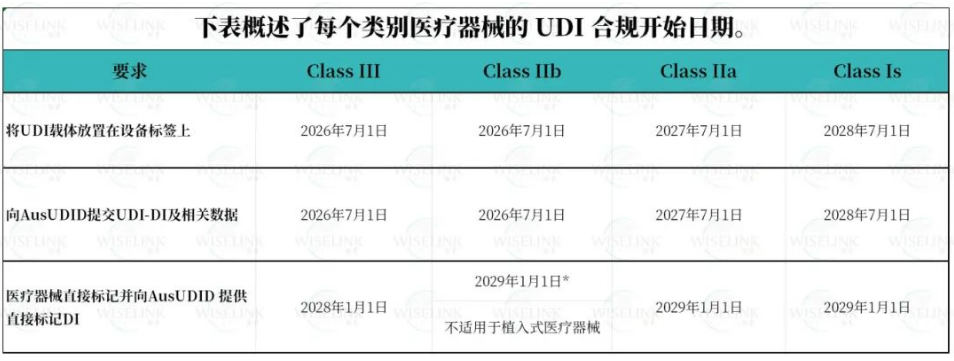
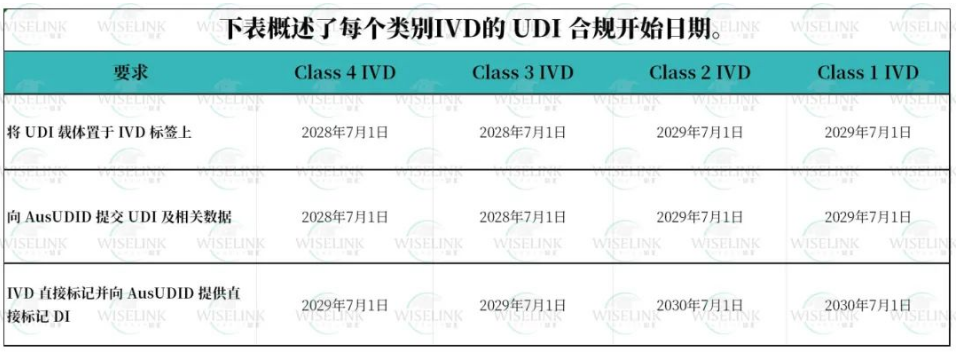
归类为 III 类或 IIb 类的“现有器械”必须在各自的合规生效日期前符合 UDI 要求,所有其他类别的“现有器械”在其整个生命周期内均可豁免。
澳大利亚TGA已建立并发布了澳大利亚唯一设备标识数据库(AusUDID),用于存储在澳大利亚供应的医疗器械的 UDI(唯一标识码)及其相关数据。该数据库中的信息会与澳大利亚治疗用品注册(ARTG)中的相应产品条目进行关联。
AusUDID 包含两个独立的使用环境:
1. 正式环境(Production Environment)
包含当前已注册的医疗器械信息;
对公众开放,任何人都可以免费访问相关数据。
2. 预发布环境(Pre-production Environment)
仅限注册人(sponsors)和制造商访问;
主要用于帮助企业熟悉 AusUDID 系统,提前测试数据提交方式(如 API、Excel 批量上传等),以便在正式提交数据前确保操作正确无误。
这一设计有助于企业在不影响正式系统的前提下完成 UDI 数据对接准备,顺利实现合规过渡。
历经多年的筹备与完善,澳大利亚的 UDI 监管框架终于落地实施,标志着TGA设备识别与可追溯性能力的全面提升,为建立更加高效和透明的监管体系奠定了基础。
当前阶段,赞助商和制造商可选择在强制实施前主动遵循 UDI 要求。但一旦启动自愿合规,就应全面遵守所有相关规定,以避免对最终用户产生混淆,确保信息一致性与患者安全。
Wiselink拥有包括原澳大利亚药品监督管理局局长Dr. Derrick Beech为首席顾问的国际专业团队,秉承源于澳洲、扎根中国、服务世界的精神,信守专业、真诚、开放的核心价值观,致力于为医疗器械、化妆品、食品、保健品和中药制造商提供全球合规认证和临床试验服务。