

2025年6月11日,墨西哥卫生部在《联邦官方公报》(DOF)正式发布了《关于医疗器械等效路径适用规则的修订协议》,这是继2021年之后,COFEPRIS再次对“国际注册认可”制度进行重大调整。此举不仅响应全球监管趋同趋势,更提升了墨西哥本土市场对国际先进医疗产品的准入效率。
对于计划进军墨西哥市场的医疗器械企业来说,这是一份不可不读的重要新规。
https://dof.gob.mx/nota_detalle.php?codigo=5759832&fecha=11/06/2025#gsc.tab=0
本协议对《健康投入条例》(Reglamento de Insumos para la Salud)中第167、170、177、177‑Bis 2、179、180条款所要求的注册技术评估与数据认证进行“等效承认”,并将国际标准视作墨西哥本土注册标准的对应依据。涵盖范围包括:
新分子创新药、仿制药、生物类似药;
医疗器械与诊断产品(依据条例第262条定义);
特别针对公共卫生事件中紧急、被忽视疾病的药械产品。
根据第22条,COFEPRIS承认以下国际权威机构的监管决策:
①IMDRF管理委员会成员国的监管机构(如美国FDA、日本PMDA、加拿大Health Canada等);
②MDSAP计划成员国的认证机构所签发的GMP证书。
这意味着,只要你的产品已经获得上述国家认可,有望走“等效路径”快速进入墨西哥。

依据第23条,制造商在提交医疗器械注册申请时,可以用下列任一文件替代传统墨西哥GMP认证:
①IMDRF成员监管机构签发的GMP证书;
②MDSAP认证机构出具的质量体系合格证书;
③ISO 13485质量体系证书(需由官方认可机构签发);
④由欧盟委员会批准的公告机构颁发的医疗器械合格评定证书 (CE);
⑤含有GMP符合性声明的自由销售证书(FSC)。
需要注意的是:文件需符合COFEPRIS后续将在DOF发布的技术指南要求,并以正式格式递交。

若来自其他IMDRF成员国(如澳大利亚、欧盟等),在新编码发布前,仍需通过上述路径之一申请。待COFEPRIS发布对新监管机构的认可公告后,方可切换为原产路径。

新规第25条规定:
COFEPRIS必须在30个工作日内针对“依赖式申请”完成注册审批。
这对过去常被诟病审批时间不定的墨西哥审批系统,是一次重大“提速”承诺。尽管现实中COFEPRIS审批效率仍需进一步提升,但法律承诺的时限将有助于企业据此主张行政效率,从而有效的助力企业快速投放市场、抢占销售窗口期。
审批效率:明确时间表(≤30个工作日),极大提速。
成本控制:减少重复认证与数据准备 。
国际对接:打通IMDRF/MDSAP与墨西哥市场。
注册策略优化:精准匹配注册路径与监管要求。
合规可预期性提升:所有标准、监管路径、可用证书均明确可查。
(一)优先定位适配认定路径
已获FDA/HC/CE/ISO 13485/MDSAP 等认证的产品最具优势;
确保产品与审批版本技术参数一致。
(二)整理关键文档准备提交
GMP/MDSAP/CE/FSC+技术对比说明;
产品对比表与“同款声明”资料不可忽略。
(三)灵活选择注册模板
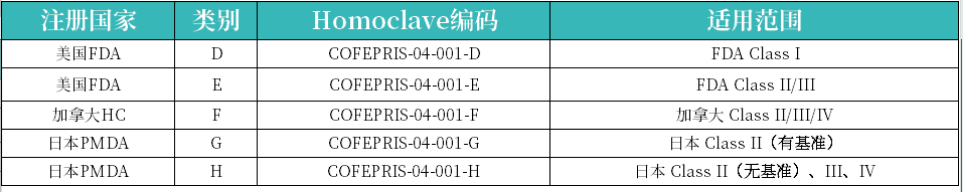
根据产品注册来源选择 D/E/F/G/H 模式;
若非这三国来源,需及时跟进COFEPRIS指南动态更新路径选择。
(四)重视时效与追踪
虽承诺 30 日仍可能延误,建议企业预设缓冲期;
同时跟进 COFEPRIS 后台审查反馈与补件通知。
新规将于2025年8月(60个工作日后)正式生效;同时废除所有此前有关“等效路径”的旧政策,包括2020年、2021年发布的相关协议。
墨西哥此次改革是拉美地区对国际医疗器械监管趋同的一大进步,将成为IMDRF与MDSAP框架下“regulatory reliance 依赖式监管”在中高风险器械注册中的试点典范。
对中国医疗器械企业而言,是拓展拉美市场的黄金窗口期。特别是已获得 美国FDA、日本PMDA、MDSAP等国际认证的企业,应尽快制定相关出海战略,抢占政策利好先机。
MDSAP认证已经获得五个国家的监管机构:美国食药品监督管理局FDA,加拿大卫生局 Health Canada,澳大利亚治疗品管理局(中文简称)TGA,巴西卫生局 ANVISA 和日本厚生劳动省 MHLW 的认可,并且2017年1月1号正式实施MDSAP并对检查结果互认。
如今墨西哥医疗器械注册也可接受MDSAP认证,对于医疗器械制造商而言,知汇建议可以将办理MDSAP认证作为企业出海的优先战略目标。一个MDSAP认证,可以适用多个国家。