


随着全球医疗器械监管环境的持续升级,泰国作为东南亚重要的医疗市场之一,其《医疗器械法案》(Medical Device Act B.E. 2551及其修正案B.E. 2562)也引入了更加严格的风险分类体系。
本文Wiselink知汇将重点为您介绍泰国对“特殊管制医疗器械(Specially Controlled Medical Devices)”的管理要求,涉及十几种高风险器械类别,帮助相关医疗器械制造商了解合规注册流程,提前布局东南亚市场。文中附官方文件与器械示例。
什么是“特殊管制医疗器械”?
根据泰国食品药品监督管理局(Thai FDA)于2020年发布的官方公告,所谓“特殊管制器械”是指高风险医疗器械,一旦投放市场需经过注册审查,并获得进口或制造许可证。
这类器械通常具有下列特征:
- 长期或永久性植入体内;
- 接触中枢神经系统或心脏循环系统;
- 具备放射性、能量释放或免疫影响;
- 属于高致死或不可治愈疾病的诊断工具(例如 HIV 检测)。
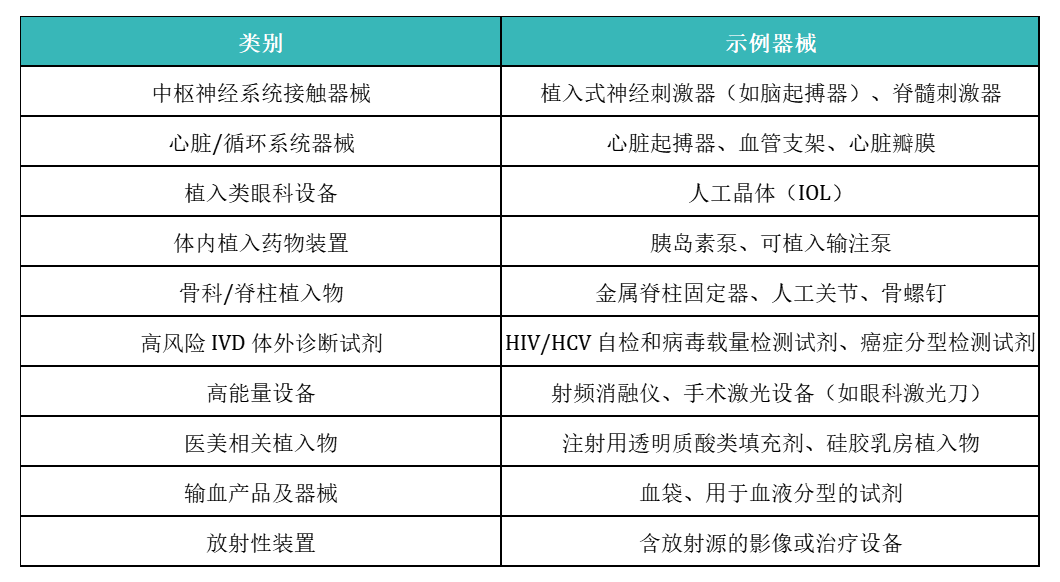
来源:https://en.fda.moph.go.th/media.php?id=482373295589695488
1. 确认产品分类:确定你的器械是否属于“特殊管制器械”范围;
2. 准备注册资料:包括技术档案、临床评价、QMS文件、标签、说明书等;
3. 选择合适代理人:非泰国本地公司必须通过具备资质的泰国代理商进行注册;
4. 注意语言要求:提交材料需含泰语标签与说明书。
提交完整注册资料
经 Thai FDA 技术审查通过
获取制造或进口许可证
无证销售/进口属于违法行为,将被处罚。
产品技术说明书(Device Description)
风险管理报告(ISO 14971)
临床评价或性能数据
ISO 13485 或 GMP 认证文件
标签(Label)和说明书(IFU)【需提供泰语版】
其他国家注册证(若需要)
建立产品追溯机制
上报不良事件(Adverse Event)
定期提交市场表现与风险评估更新报告(如适用)
Wiselink拥有包括原澳大利亚药品监督管理局局长Dr. Derrick Beech为首席顾问的国际专业团队,秉承源于澳洲、扎根中国、服务世界的精神,信守专业、真诚、开放的核心价值观,致力于为医疗器械、化妆品、食品、保健品和中药制造商提供全球合规认证和临床试验服务。