

1
香港医疗器械监管部门
1.1 香港MDACS

香港医疗仪器科(前称医疗仪器管制办公室)负责医疗器械的监管事宜,医疗器械在香港有一个独特的监管体系,即MDACS (Medical Device Administrative Control System)(医疗器械行政控制系统)。
1.2 监管法规
International Medical Device Regulators Forum, IMDRF
1.3 风险等级分类
参考国际医疗器械监管机构论坛(IMDRF)提出的医疗器械分类原则,医疗器械(包括普通医疗器械和体外诊断医疗器械(IVDMDs))根据与其预期用途相关的风险水平分为四(4)类。只有第II、III和IV类医疗器械以及第B、C和D类体外诊断医疗器械可以申请在香港表列,而对于第I类医疗器械和第A类体外诊断医疗器械的最低风险等级,MDD将不接受表列申请。
MD-医疗器械
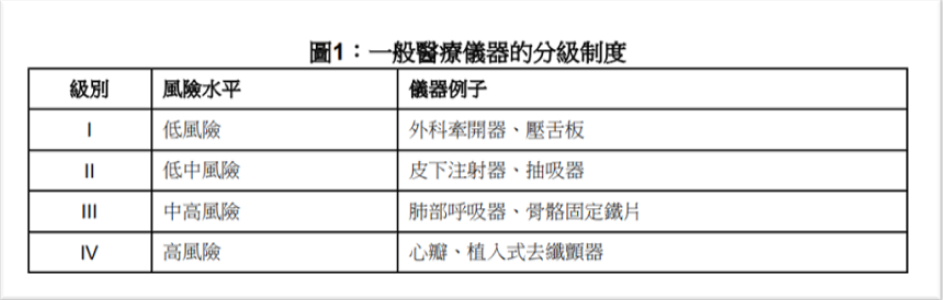
IVD-体外诊断
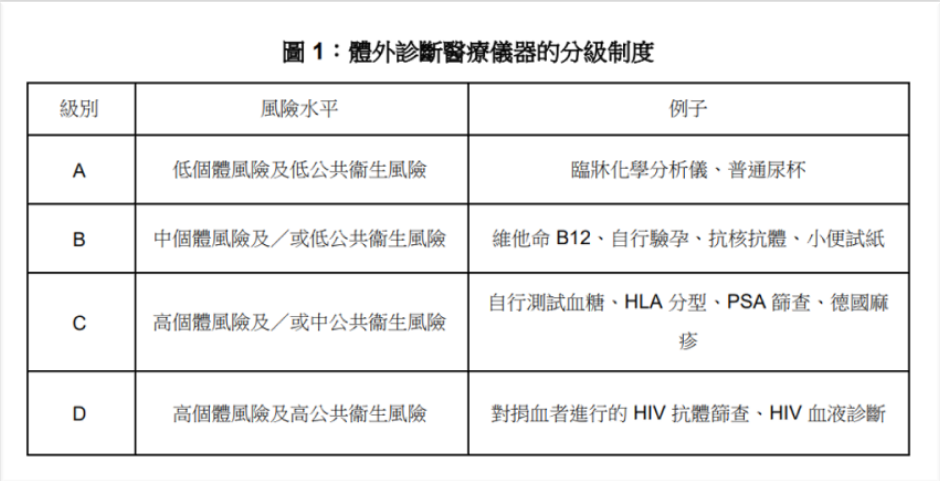
确定产品风险等级分类的方法如下:
方法一:查阅《TR-003普通医疗器械分类》和《TR-006体外诊断分类》的分类规则,依据分类规则判断产品风险等级。
方法二:利用官网上的风险等级决策小工具进行判断衞生署 | 醫療儀器科 - 一般醫療儀器分級程式
衞生署 | 醫療儀器科 - 體外診斷醫療儀器分級程式
方法三:利用香港医疗器械表列数据库卫生署 | 医疗仪器科 - 医疗仪器列表https://www.mdd.gov.hk/sc/mdacs/search-database/list-md/index.html 查询同类产品的风险等级。
1.4 注册必须具备的资料
依据《TR-002證明符合醫療儀器安全及性能基本原則的技術文件摘要》准备注册资料,所有申请材料都要求中文及英文填写。向医疗器械行政控制系统MDACS申请(医疗器械的MD-C2&3&4表,IVD的MD-IVD表)
所需文件包括:
CE证书或510K信函
质量管理体系符合性证明,如ISO 13485证书
标签和使用说明,需符合《TR-005醫療儀器標籤附加規定》
上市后程序
国际测试报告和临床数据(如适用)
按照TR-004编写基本原则检查表(加上IVDs的性能评估报告)
具体可以查看指南《GN-02第II III IV级一般医疗仪器表列指南》和《GN-06第B,C及D级体外诊断医疗仪器表列指南》。
1.5 注册语言
英语或繁体中文。
2
注册流程|周期
2.1 注册流程
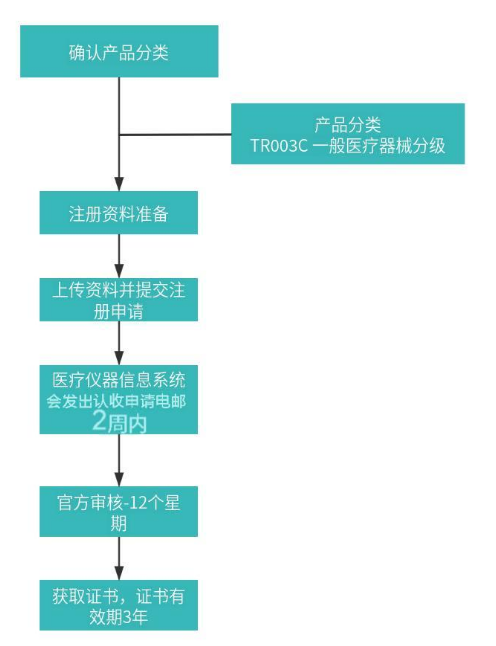
2.2 注册周期
递交申请及全部所需证明资料 (包括标签样本)后12个星期内完成表列。
3
香港医疗器械注册常见FAQ
Q:香港医疗器械表列需要在香港开展临床试验吗?
A:目前,香港并无特定法例规管医疗仪器的临床研究。但这并不意味着制造商不需要进行临床研究。
Q:医疗器械在香港一定要有本地负责人(LRP)吗?
A:有意申请把仪器纳入「医疗仪器列表」的制造商,如在本港没有注册营业地址,则须在提出申请前委任一名本地负责人 (LRP) 。
Q:香港表列医疗器械有效期是多久?如何续期?
A:本地负责人须在 5 年有效期届满前最少12周至1年内 (包括首尾两天),向医疗仪器科递交表列医疗仪器的续期申请。续期申请必须在上述期限内送达医疗仪器科,否则医疗仪器科将不会处理该续期申请。
Q:什么是被除名的医疗仪器?在什么情况下医疗仪器会被除名?
A:卫生署可在下列情况下,有权酌情把仪器从「医疗仪器列表」上永久或暂时删除:
①卫生署基于公众健康或安全考虑,认为有需要把仪器从列表上删除,如制造商或本地负责人未能处理或妥善处理仪器所构成的危险;或
②制造商或本地负责人未能符合医疗仪器行政管理制度的规定或任何批准表列条件;或
③制造商或本地负责人未能完全遵从卫生署的指示,从宣传中撤回没有充分理据的声称;或
④制造商或本地负责人已清盘或不复存在;或
⑤制造商或本地负责人要求除名。
Q:香港注册一定要原产国注册才可以吗?
A:原产国注册并不是香港注册的先决条件,但如果有全球医疗器械协调工作组(IMDRF)五个创始成员国(欧盟、澳大利亚、加拿大、日本和美国)的任意一个国家注册证,能够加速在香港的注册。