在2014年2月25日,菲律宾列出了在菲律宾分销和销售之前需要注册的体外诊断试剂清单(Philippines circular 2014-005),该法规主要涉及HIV/HBV/HCV/梅毒、伴随诊断、血型分析、抗人球蛋白诊断试剂等8类产品。但在2022年菲律宾召开了公众咨询会,提出新的IVD法规修订草案并明确实施时间表,其中明确了2023年第二季度将开始实施,2025年底将结束过渡阶段,预计在2026年将全面实施,届时符合IVD定义的产品将需要取得注册或登记才能在菲律宾市场流通。
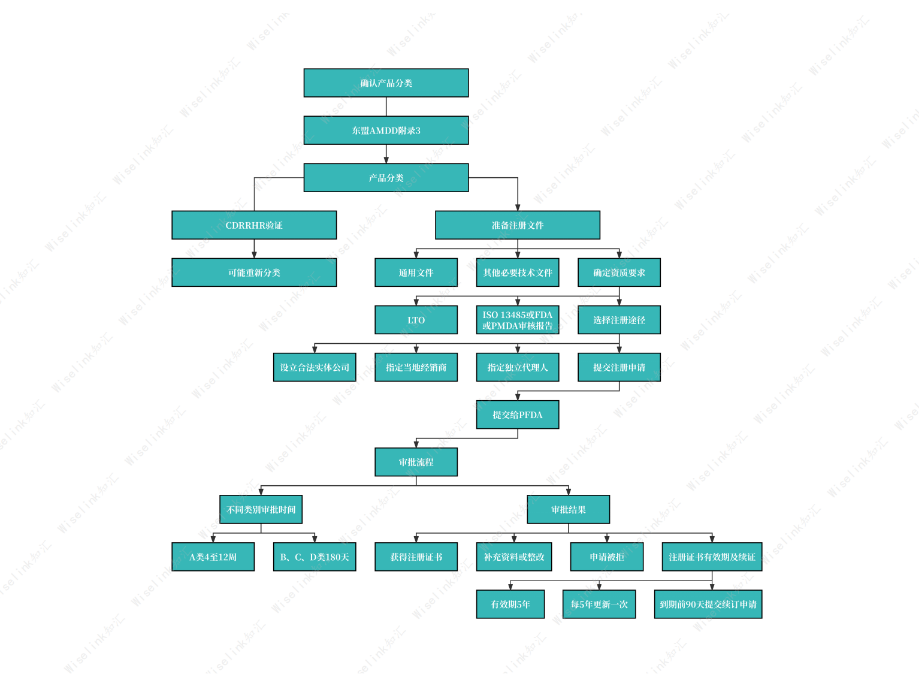
提交申请时BCD类产品需要遵守顺序原则, A-M开头的公司可以在周四提交申请,N-Z字母开头的公司可以在周五提交申请,而A类产品则无此要求,可以在工作日无限制提交产品申请。A类IVD产品通常在提交申请后20天左右给出反馈意见,批准或要求补充文件,BCD类产品则要求6-9个月甚至更长的时间才能获批。如果涉及菲律宾本地实验室测试则需要更长的时间。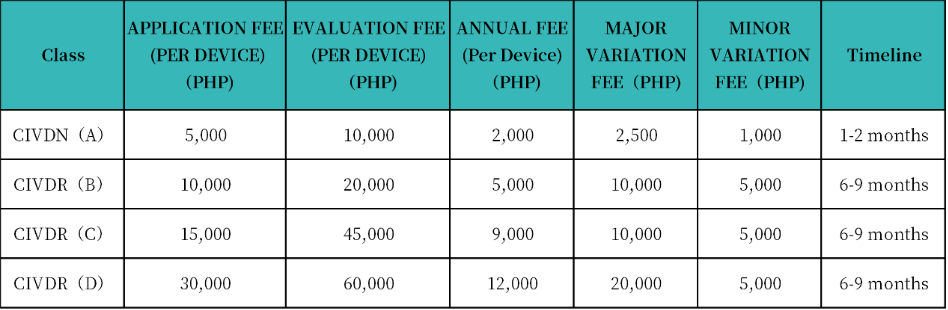
注:以上费用不包括国家参考实验室(NRL)测试费用.产品注册证有效期为5年,证书需要每5年续期一次并且需要提前发起申请,之后提供官方所要求的资料即可。Wiselink拥有包括原澳大利亚药品监督管理局局长Dr. Derrick Beech为首席顾问的国际专业团队,秉承源于澳洲、扎根中国、服务世界的精神,信守专业、真诚、开放的核心价值观,致力于为医疗器械、化妆品、食品、保健品和中药制造商提供全球合规认证和临床试验服务。







