

一. 背景
2024年11月11日,欧盟更新了关于MDR法规和IVDR法规中关于警戒术语和概念的公告。

该文件中的部分定义借鉴了《医疗器械警戒系统指南》,并依据MDR和IVDR进行了必要的修订。除非直接从法律文本中引用或另有特别说明,本文中“器械”一词泛指医疗器械、医疗器械附件、MDR附件XVI所列产品、体外诊断医疗器械及体外诊断医疗器械附件。此外,本文件应与其他相关法规、标准及MDCG指导文件结合使用,以获取全面理解。
二. 警戒术语和概念的核心FAQ
Q1:MDR & IVDR法规中“事故”和“严重事故”有什么区别?
A1:“事故 ”与 “严重事故 ”的主要区别在于与市场上销售的器械问题相关的健康或公共卫生结果(或潜在结果)的严重性。详细情况可见下表:
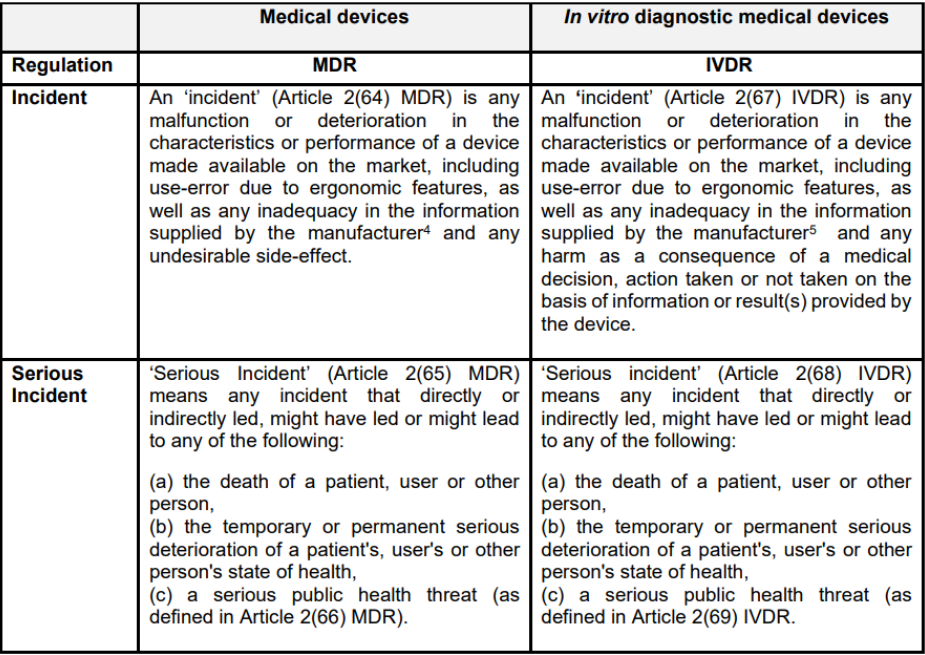
Q2:判断“需要报告的严重事故”的基本标准是什么?
A2:任何符合以下三项基本报告标准的事故均被视为严重事故,必须向相关主管当局报告。
(1)已发生事故
(2)事故直接或间接导致、或可能导致严重事故的任何结果
(3)严重事故与制造商设备之间的因果关系已确定、或有合理的可能或怀疑
Q3:根据 MDR 第 2(64)条 & IVDR 第 2(67)条,“器械特性和性能的故障或恶化 ”具体指的是什么?
A3:医疗器械特性和性能的故障或退化"可描述为:器械在按照信息使用时,未能达到或无法维持制造商所声明的性能 "(MDR Article II(22) )
对于 IVD,器械的性能包括分析性能,以及支持其预期用途的临床性能,制造商必须在技术文件中证实器械的性能。(IVDR Article II(39) )
Q7:如何解释“器械事故间接导致个人健康状况出现恶化”?
A7:有些器械由于其预期用途,可能不会对人造成直接伤害或健康恶化,但可能会造成间接伤害。在大多数情况下,如果医疗决定、采取的行动或没有采取的行动是基于设备提供的不正确信息或结果,那么所造成的伤害或健康恶化就是间接伤害。
三. 总结
本文件旨在详细解释和阐明欧盟医疗器械法规(MDR)(EU)2017/745及体外诊断医疗器械法规(IVDR)(EU)2017/746 Chapter VII Section 2所提及的关键术语和概念,这些术语和概念的共同理解对于确保上述法规下警戒要求的有效和一致执行至关重要。如果您对指南有更多疑问,欢迎咨询Wiselink知汇的小伙伴!
添加小编咨询可获取PDF原文件!
Wiselink拥有包括原澳大利亚药品监督管理局局长Dr. Derrick Beech为首席顾问的国际专业团队,秉承源于澳洲、扎根中国、服务世界的精神,信守专业、真诚、开放的核心价值观,致力于为医疗器械、化妆品、食品、保健品和中药制造商提供全球合规认证和临床试验服务。