

背景

当地时间11月5日,欧盟委员会发布了截至2024年6月30日的最新第十轮公告机构MDR/IVDR申请与发证调查报告。该报告对于把握医疗器械过渡阶段的状况、预见并规范欧盟医疗器械市场具有重要意义。
此次调查于2024年7月1日至8月6日期间进行,全面覆盖了欧盟现有的50家公告机构(NB),并实现了100%的回复率,充分展现了其全面性和权威性。
截止到2024年6月底的申请与发证情况
MD
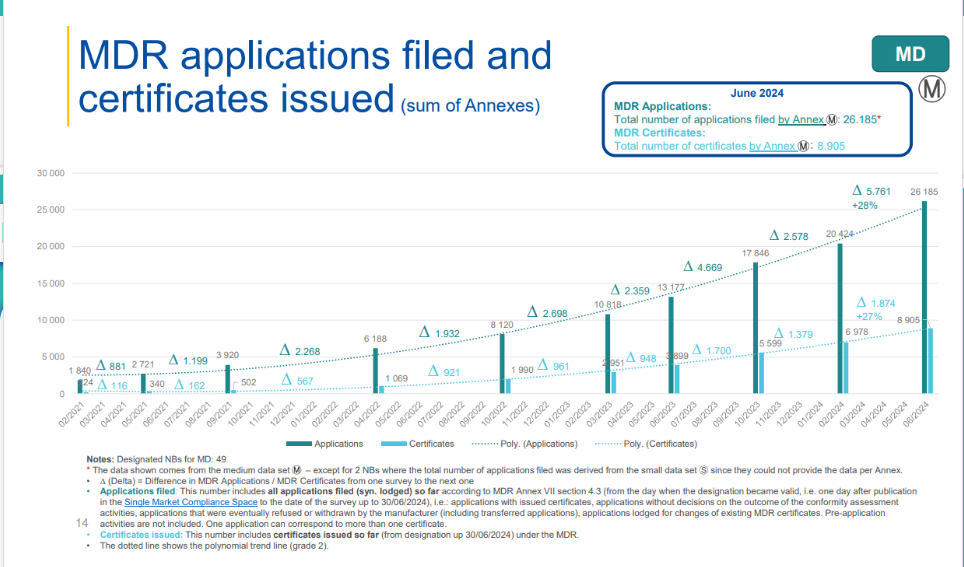
MDR调查报告核心数据(截止2024年6月底):
申请总数为26185份,发证数量为8905份,发证比例为34%
与2024年2月相比:
(1)MDR申请:由20424份增长到26185份,共计增加5761份,增幅比例达到28%(上期增幅比例为14%)
(2)MDR证书:由6978份增长到8905份,共计增加1927份,增幅比例达到27%(上期增幅比例为25%)
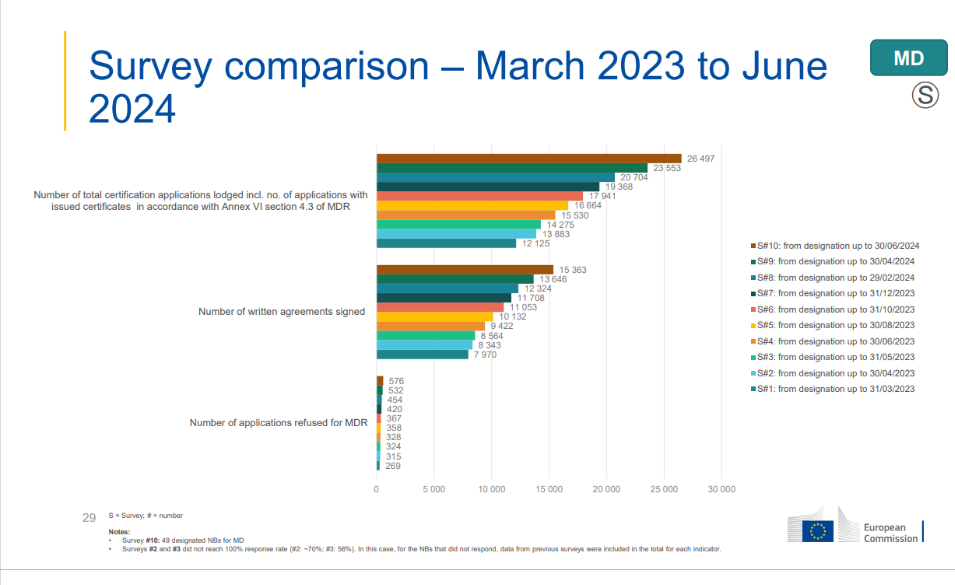
与2024年2月相比:
(1)提交申请数量增长28%
(2)书面协议签署数量增长25%
IVD
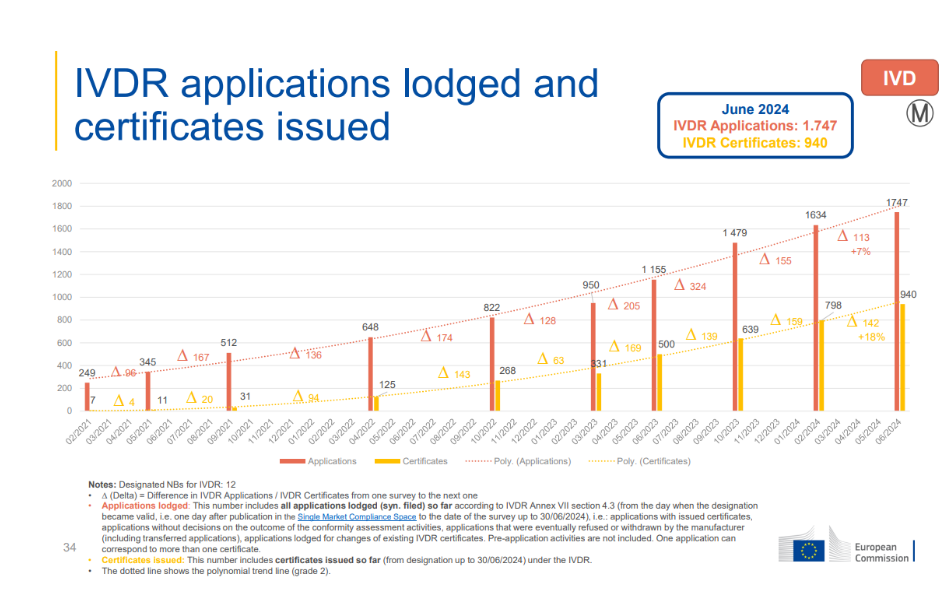
IVDR调查报告核心数据(截止2024年6月底):
申请总数为1747份,发证数量为940份,发证比例为53.8%
与2024年2月相比:
(1)IVDR申请:由1634份增长到1747份,共计增加113份,增幅比例为7%
(2)IVDR证书:由798份增长到940份,共计增加142份,增幅比例为18%
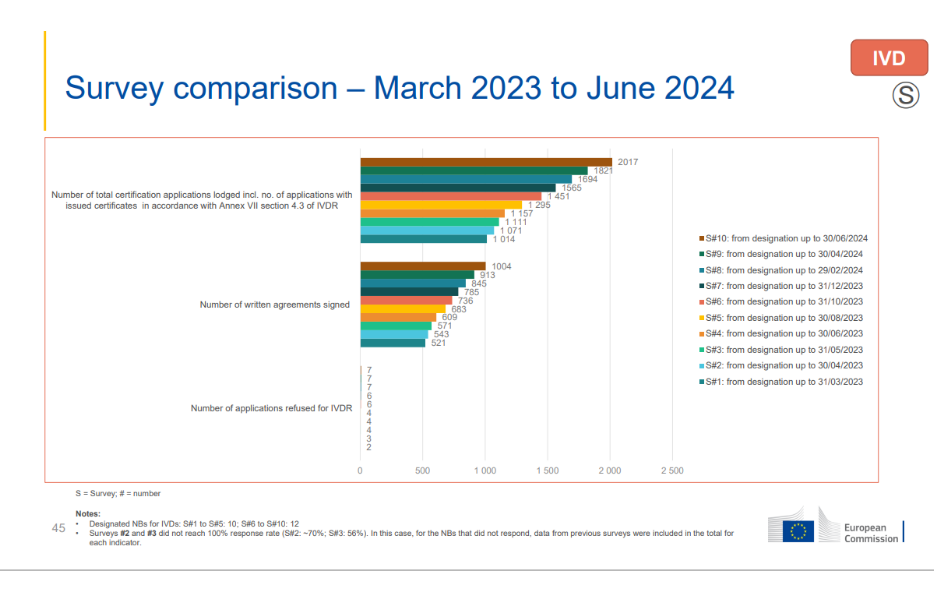
与2024年2月相比:
(1)提交申请数量增长19%
(2)书面协议签署数量增长19%
MDR & IVDR申请被拒原因分析
MD
IVD
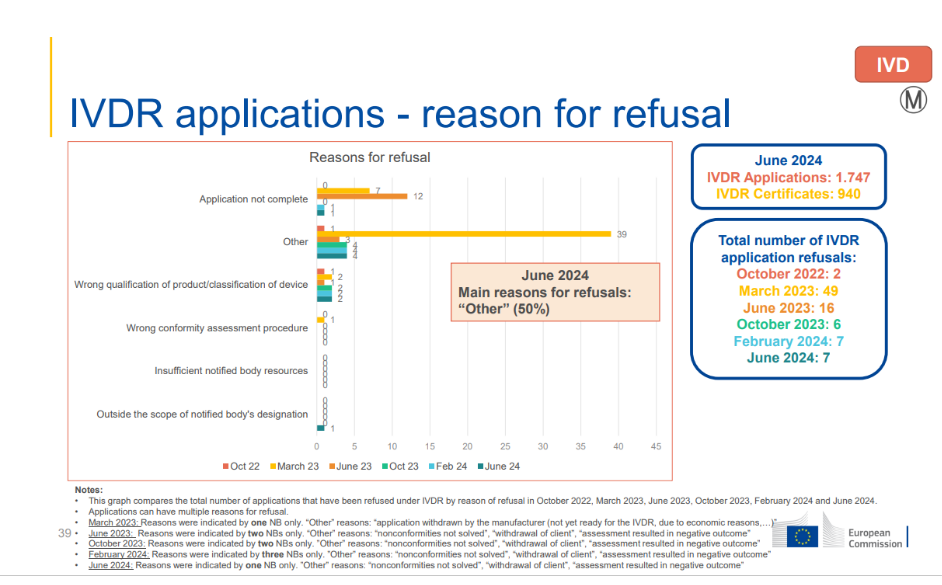
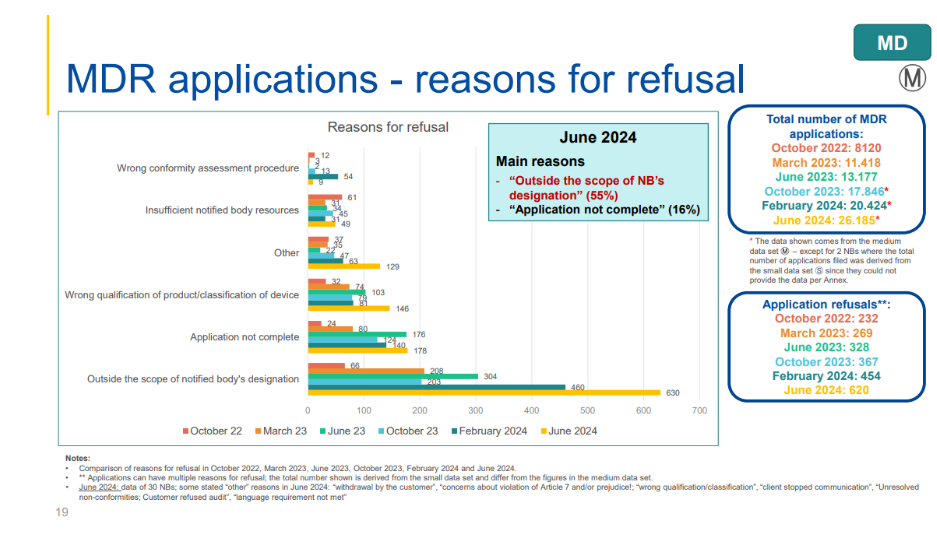
MDR & IVDR申请被拒主要原因:
(1)超出公告机构的认证范围
(2)申请资料不完整
(3)产品资质不符/医疗器械风险等级分类有误
(4)其他原因
MDR申请被拒首要原因:超出公告机构认证范围
IVDR申请被拒首要原因:其他原因
MDR & IVDR证书获批时间
MD
IVD
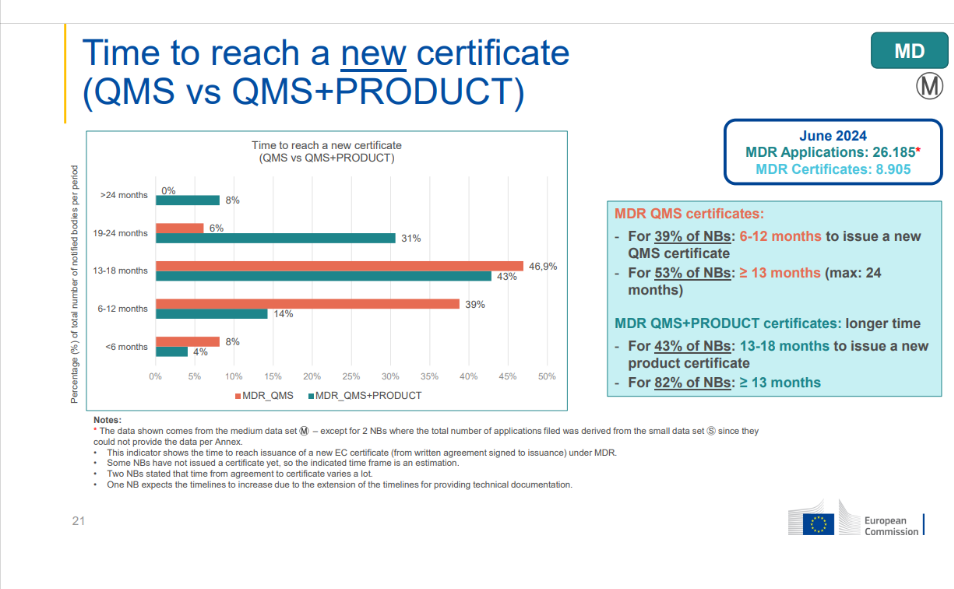
MDR QMS 证书所需时间
- 39%的NB机构:6-12个月颁发新的QMS 证书
- 53%的NB机构:≥ 13 个月(最长:24个月)
MDR QMS+产品证书所需时间则更长
- 43%的NB机构:13-18个月颁发新的产品证书
- 82% 的NB机构:≥ 13 个月
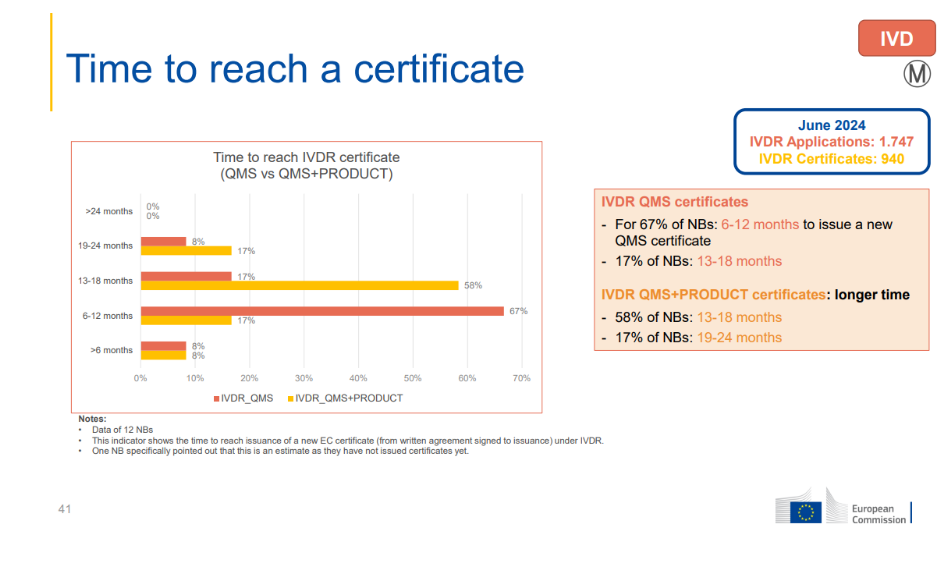
IVDR QMS 证书所需时间
- 67%的NB机构:6-12个月颁发新的QMS证书
- 17%的NB机构:13-18个月
IVDR QMS+产品证书所需时间则更长
- 58%的NB机构:13-18个月
- 17%的NB机构:19-24个月
知汇对于CE认证经验丰富,具有专业的法规顾问团队,可以为您提供一站式CE认证服务!了解更多关于CE认证的知识,欢迎咨询Wiselink知汇的小伙伴!
原文链接
https://health.ec.europa.eu/document/download/59b9d90e-be42-4895-9f6f-bec35138bb0a_en?filename=md_nb_survey_certifications_applications_en.pdf
Wiselink拥有包括原澳大利亚药品监督管理局局长Dr. Derrick Beech为首席顾问的国际专业团队,秉承源于澳洲、扎根中国、服务世界的精神,信守专业、真诚、开放的核心价值观,致力于为医疗器械、化妆品、食品、保健品和中药制造商提供全球合规认证和临床试验服务。


