目前进入加拿大市场销售的所有医疗器械,都必须获得加拿大卫生部(Health Canada)的许可。加拿大卫生部下属的医疗器械局(Medical Devices Directorate,MDD)是监督和评估加拿大诊断与治疗医疗器械的安全性、有效性和质量的国家重要权威机构。
食品药品法(Food and Drugs Act (R.S.C., 1985, c. F-27))
加拿大医疗器械法规(Canadian Medical Devices Regulations SOR/ 98 282)
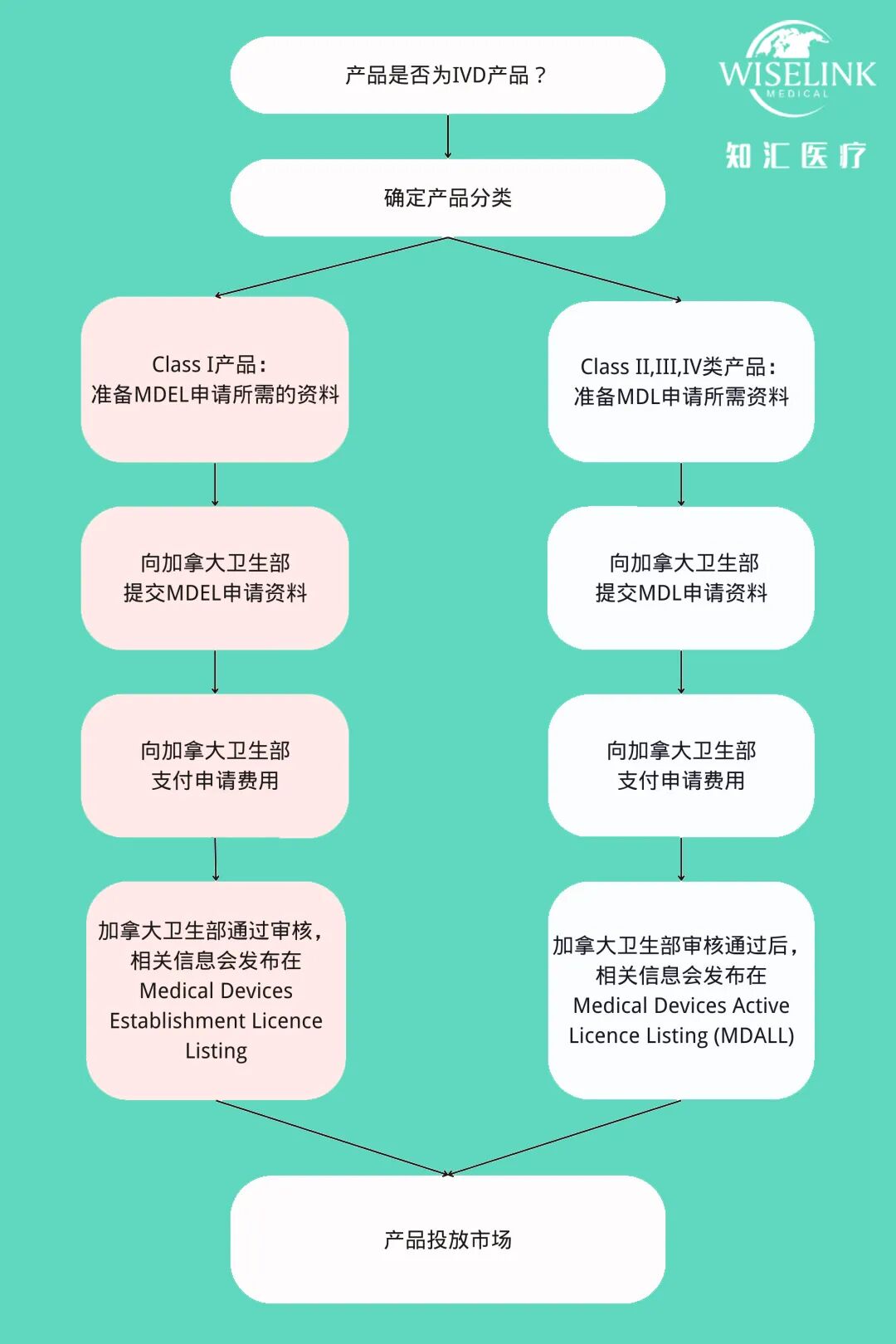
根据法规Medical Devices Regulations SOR/98-282.依据器械的使用风险将IVD医疗器械分为四类,依次为Class I、 Class II、Class III、Class IV。当中Class I类器械是最低风险,Class IV类器械风险为最高。
各医疗器械企业许可证是颁发给I类IVD器械制造商,和所有IVD器械类别的进口商或分销商的许可证,可以他们在加拿大进口和分销医疗器械。一般自申请之日起的120天内都会颁布医疗器械企业许可证的证书,这类证书不会过期,但仍然需要进行年度审核和缴纳每年的证书费用来续期,一旦不缴费就可能会被取消证书。有异于医疗器械企业许可证针对的是制造商、分销商、进口商的证书,医疗器械许可证是颁发给II, III和 IV类IVD产品的许可证书,该证书由制造商所持有。依据不同的风险等级,自申请之日起的28-225天内加拿大卫生部会发送医疗器械许可证证书给制造商,该证书不会过期,每年加拿大卫生部会发送邮件给制造商进行确认并要求缴纳每年的证书费用以续期,一旦不缴费将可能会被取消证书。申请医疗器械许可证时,制造商均需要拥有符合加拿大医疗器械法规要求的,且经过医疗器械单一审核计划(Medical Device Single Audit Program,MDSAP)认证的ISO 13485质量管理体系。
更多关于国际医疗器械注册等相关咨询和出口资质代办认证服务,请与wiselink顾问联系。




