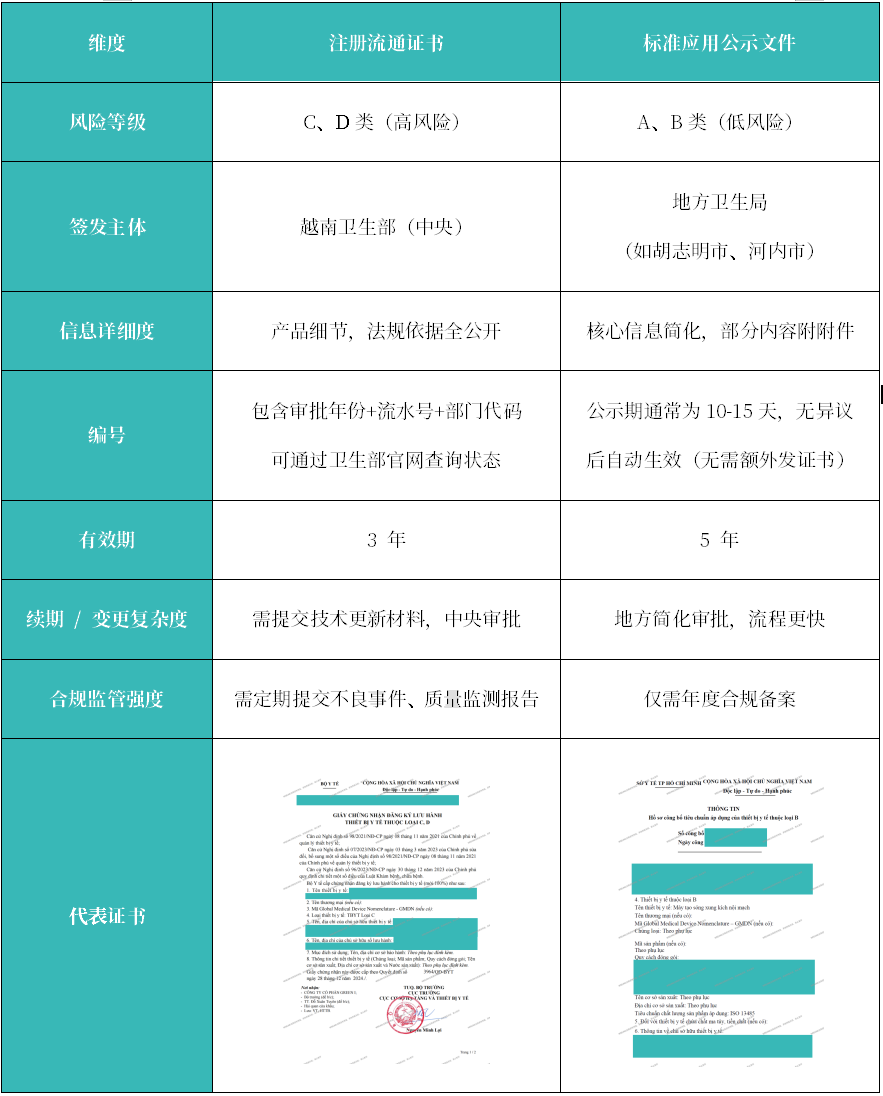
开拓越南医疗市场,最绕不开的就是注册证书,但越南根据器械风险等级,设计了两种不同的证书格式:低风险 A / B 类用公示文件,高风险 C / D 类发正式注册证书。不少企业初次接触时,常搞混两类文件的核心信息和合规要点。知汇结合实际证书案例,手把手拆解这两类证书的关键内容,帮你快速理清合规边界。
越南的医疗器械产品注册由越南卫生部药品和医疗器械管理局 MOH(Department of Medical Equipment and Construction under the Ministry of Health)下属的医疗设备和建设部(DMEC)监督 ,其主要职责是:负责审核、批准医疗器械的注册和监管,确保医疗器械在越南市场上符合安全性和有效性要求。越南将医疗器械分为 4 类,对应两种证书形式:低风险( A / B 类)和高风险( C / D 类)。越南 MOH 根据器械风险等级,对应的证书也不同:
不管是越南低风险 A / B 类的公示文件,还是高风险 C / D 类的注册证书,核心信息都是围绕产品、主体、合规三个维度展开的,这是所有证书的通用骨架。具体可归纳为 5 个必含模块:唯一标识(编号):不管是公示编号还是注册证书号,都是后续查询、续期、变更的唯一凭证;签发 / 公示主体:明确是中央(卫生部)还是地方(市卫生局)审批,决定了后续对接的监管部门;日期(签发 / 公示 + 有效期):直接关联产品合法上市的时间范围,是续期的关键节点。产品名称和类别:明确产品是什么、属于哪类风险等级( A / B / C / D ),直接决定监管要求;预期用途和适用范围:划定产品能做什么、给谁用、在哪用,是合规使用的边界;质量标准:证明产品符合的规范(如 ISO 13485),是质量合规的基础。本地主体(申请人 / 公示方 / 持证方):必须是越南本地企业,承担产品在越南市场的所有合规责任(如不良事件上报、标签更新);生产 / 技术主体:产品实际生产或技术持有方(常为境外企业),需明确其名称、地址,关联生产资质的有效性。引用的越南法规:证明证书是依据现行有效法规签发的,后续需同步法规更新;附件关联:产品规格、包装、详细技术参数等信息,会以附件形式补充,是货证一致的关键依据。监管要求:如高风险产品需定期提交质量报告,低风险产品需年度合规备案。
两类证书都有“见附件”的信息(如产品规格、生产地址),需将附件与主文件合并存档,避免货证不符。B 类的公示文件本身就是合法凭证,无需额外申请证书;C 类的注册证书需妥善保管原件,清关、投标时需提供。
越南医疗器械注册证书不仅是上市凭证,更是企业在越南市场合规运营的操作指南。只有精准拆解证书中的核心信息,明确责任主体、产品边界、合规要求,才能避免因细节疏漏导致的市场风险。欢迎咨询 Wiselink 知汇。