


https://www.fda.gov/media/186797/download
2025年6月6日,美国FDA官网发布了《疝修补网片包装标签指南(草案)》,该草案针对外科用疝修补网片的包装标签提出了新的规范性建议。这份文件的发布旨在通过标签透明化和标准化,降低医疗风险,提升临床安全性与使用效率。
近年来,FDA接收到大量与疝修补网相关的不良事件报告。自2019年至2024年间,FDA共接收了超过8.6万起不良事件报告,其中包括粘连、术后复发、疼痛和感染等问题,甚至出现死亡案例。
造成此类问题的一个关键因素,是医生在选用疝修补网时,难以从现有标签中快速获取所需的关键信息。由于产品种类繁多、材料差异大、适应症不同,缺乏统一、易读的标签信息可能导致临床误用。
该指南适用于《联邦法规》21 CFR 878.3300 条规定下、用于疝修补的外科网片产品,包括以下几类:
金属网片(EZX)
聚合物网片(FTL、FTM)
可吸收/不可吸收网片(OWT、OWU 等)
胶原蛋白网片(OWV、OXH 等)
适用于大面积腹壁缺损的专用网片(OXI、OXJ、OXK)
需要注意的是,用于整形、美容、泌尿、妇科等其他目的的网片(如JDJ、OLC等)不在此次指南覆盖范围之内。
为方便医生判断与使用,FDA建议将以下内容明确标注在包装外部标签上:
材质类别:如可吸收/不可吸收合成材料、生物来源材料等
动物来源材料需注明具体来源
是否含有抗菌剂、屏障层等附加成分
尺寸(长宽)
孔径大小
厚度
密度(单位面积重量)
纤维类型(如单丝、编织)
抗拉强度
爆破强度
若为可吸收材料,还需注明吸收时间
推荐的解剖部位(如腹膜内、腹壁间等)
固定方式(如使用钉子、缝合线)
若需要重复使用,需注明如何处理残留物
FDA在指南的附录中提供了一个标准化标签范例,内容采用表格形式直观展示各项指标。如下图所示:
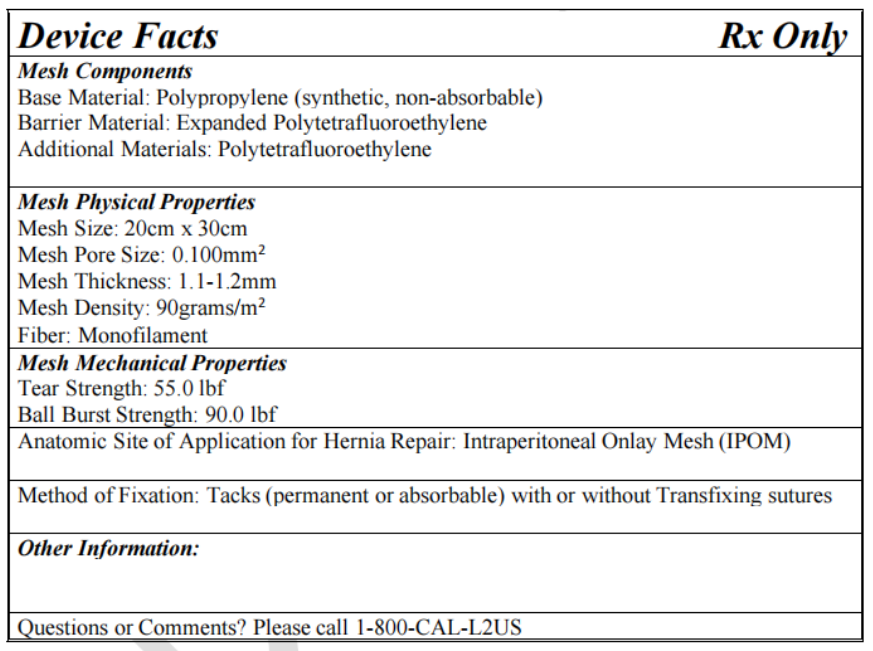
FDA此次推出的疝修补网片标签指南草案,释放出一个明确信号——医疗器械产品信息透明化、标准化已成为监管趋势。未来,医疗人员将拥有更清晰的产品认知,从而做出更安全、更有效的治疗决策。本指南草案目前仍处于征求意见阶段,FDA鼓励各方在60天内提交意见或建议。
知汇建议制造商在对现有产品进行标签更新时参考本指南内容,同时对新产品的510(k)申报应涵盖指南中建议的标签信息。相关从业者应密切关注后续定稿进程,并尽早做好标签优化准备。
Wiselink拥有包括原澳大利亚药品监督管理局局长Dr. Derrick Beech为首席顾问的国际专业团队,秉承源于澳洲、扎根中国、服务世界的精神,信守专业、真诚、开放的核心价值观,致力于为医疗器械、化妆品、食品、保健品和中药制造商提供全球合规认证和临床试验服务。


