

欧盟法规(EU)2017/746(IVDR)的实施对制造商提出了新的挑战和要求,为了帮助制造商更好地理解和应对IVDR认证流程,Team-NB发布了《IVDR认证流程共识文件》,这份文件详细描述了IVDR认证从申请前阶段到申请阶段,再到申请后阶段的全过程,为制造商提供了清晰的指导。 本篇文章,知汇将为您详细解读这份文件。 https://www.team-nb.org/wp-content/uploads/2025/04/Team-NB-PositionPaper-IVDR-Certification-Process-Consensus-Document-V1-20250409.pdf 《IVDR认证流程共识文件》旨在详细描述制造商如何向NB机构(Notified Bodies,NBs)申请IVDR认证的过程。该文件通过审查Team-NB成员的申请流程和相关文件,并尽可能协调这些流程而制定。它适用于所有需要从旧法规过渡到IVDR的遗留设备(legacy devices)以及首次申请认证的新设备。

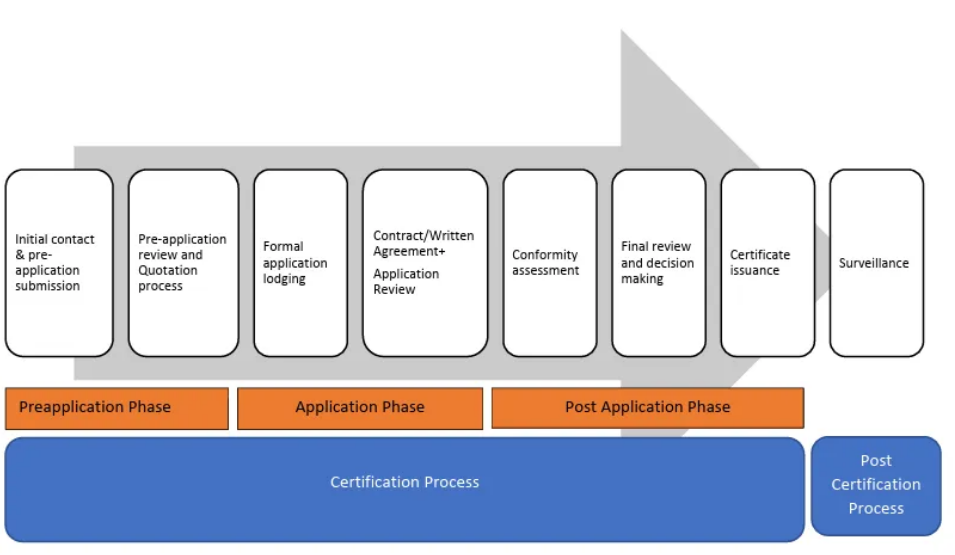
整个认证流程可以分为三个主要阶段:申请前阶段(Pre-application Phase)、申请阶段(Application Phase)和申请后阶段(Post Application Phase)。
(一)申请前阶段
1. 初次接触与预申请提交(Initial contact and Pre-application submission)
制造商与NB首次接触,提交预申请信息。NB需根据IVDR附件VII第4.2节(d)的要求,对预申请信息进行初步审核,以确认产品是否符合IVDR的范围及其分类是否准确。制造商需提供足够详细的信息,以便NB准备报价。
2. 预申请审核与报价流程(Pre-application review and Quotation process)
NB对制造商提交的预申请信息进行审核,并提供报价。如果预申请信息发生变化或出现可能影响报价的新信息,NB可在后续阶段修改报价。
(二)申请阶段
3. 正式申请提交(Formal application lodging)
如果制造商接受NB的报价并决定继续申请,需提交以下文件:
根据附件IX第2.1节或附件XI第3.1节的质量管理体系(QMS)评估文件。 对于B、C和D类设备,需提交附件IX第二章第4.2节的技术文件。 如果是自测或近患者检测设备,需提交附件IX第二章第5.1节(b)的内容。 对于伴随诊断设备(Companion Diagnostics,CDx),需提交附件IX第二章第5.2节(b)的文件。 D类设备可能还需要符合实施条例2022/944的欧洲参考实验室(EURL)的任务和标准。
4. 合同/书面协议与申请审核(Contract/Written Agreement and Application review)
NB在收到申请后,会提供合同文件,双方签署后正式开始审核。审核内容包括:
检查申请文件的完整性。 验证产品是否符合IVDR的定义及其分类。 确认所选的符合性评估程序是否适用。 确认NB是否有能力评估该申请。 确认是否有足够的资源进行评估。
(三)申请后阶段
5. 符合性评估(Conformity assessment)
NB根据设备的分类和所选的符合性评估程序,开展评估活动。
A类设备通常不需要NB的符合性评估,除非以无菌形式上市。
B、C和D类设备需要结合质量管理体系审核、技术文件评估和设备测试。
对于D类设备,可能还需要与欧洲参考实验室(EURL)合作进行性能验证。
6. 最终审核与决策(Final review and decision making)
NB完成所有评估活动后,进行最终审核并决定是否发放证书。审核团队需确保所有报告和文件完整,且没有未解决的不符合项。
7. 证书发放(Certificate Issuance)
如果审核通过,NB将根据IVDR附件XII的要求发放证书,并在EUDAMED系统中上传。
8. 监督活动(Surveillance activities)
在初始认证完成后,NB需制定监督计划,包括每年对制造商的质量管理体系进行审核,评估定期安全更新报告(PSUR)和安全与性能摘要(SSP),以及对B类和C类设备的技术文件进行抽样评估。
1. 语言要求:技术文件和质量管理体系文件的语言要求由NB具体规定。
2. 遗留设备过渡:对于从旧法规过渡到IVDR的遗留设备,制造商需提供足够的信息,以便NB验证产品的资格、分类和所选的符合性评估程序。
《IVDR认证流程共识文件》为制造商提供了一份详尽的指南,帮助他们更好地理解IVDR认证的全过程。通过明确每个阶段的要求和步骤,制造商可以更高效地准备和提交申请,减少因信息不完整或不符合要求而导致的延误。随着NB在IVDR实施过程中积累更多经验,这份文件也将不断更新和完善,以适应法规的变化和新的指导文件的发布。