

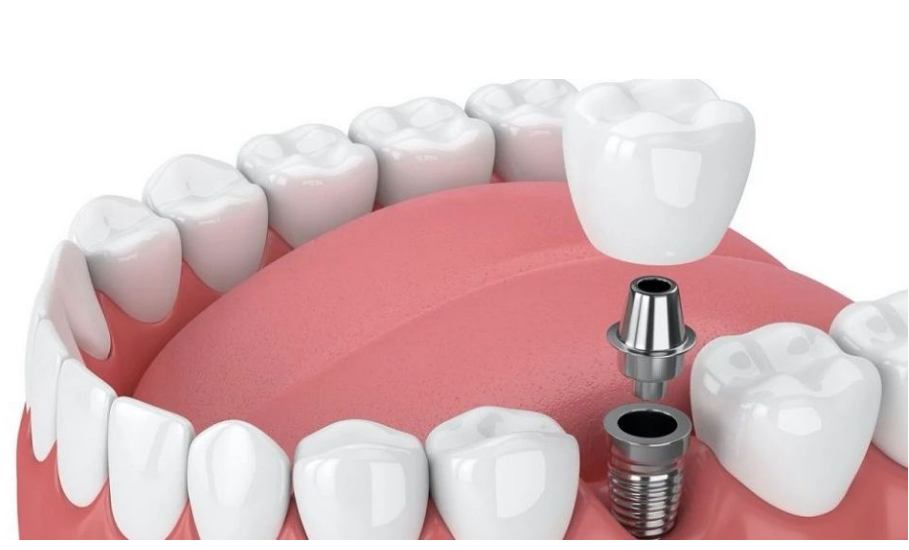
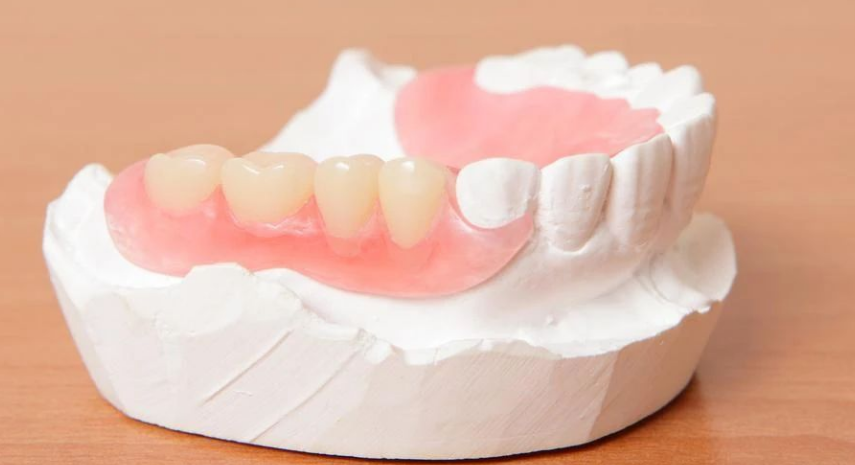
义齿是用于修复口腔内缺失牙齿及其周围软硬组织的修复体的总称。它通过人工材料制作,目的是恢复牙齿的形态、功能以及美观,帮助患者改善咀嚼、发音和面部外观等问题,同时改善口腔的生理状态和个人的心理状态。
义齿通常分为以下3类:
活动义齿(Removable Denture):患者可以自行摘戴的义齿,是靠义齿的基托和卡环来固位,是可以自行摘戴的假牙,不需要磨小周边健康的牙齿。包括局部活动义齿和全口活动义齿。
固定义齿(Fixed Denture):固定在口腔内,患者无法自行摘戴,包括单冠、固定桥等。
种植牙(Implant-Supported Denture):通过种植体植入牙槽骨内,作为支持和固位的基础,再在其上安装义齿。
1. 定义及预期用途

![]()
2. 分类
金属陶瓷牙冠及牙桥:包括作加固用途并植于陶瓷内部以求美观的金属支架;
无金属牙冠及牙桥:通常由氧化锆支架组成,并植于陶瓷内部,整个产品亦可以陶瓷、氧化锆或二硅酸锂玻璃陶瓷制成;
金属牙冠及牙桥:整件产品均由贵金属、次贵金属及非贵金属的牙科合金制成增加活动义齿的内容。
加拿大义齿市场预计从 2021 年的 7050 万美元增长至 2028 年的 1.202 亿美元,年复合增长率(CAGR)达 7.9%。人口老龄化加剧是核心驱动力,老年人口比例上升导致牙齿缺失需求增加,推动义齿市场持续扩大。
加拿大居民对牙齿美观和功能的关注度提高,推动对高质量义齿的需求。固定义齿因接近天然牙的外观和功能,更符合消费者对美观的追求;活动义齿则因便捷性和成本优势,仍保持稳定市场份额。
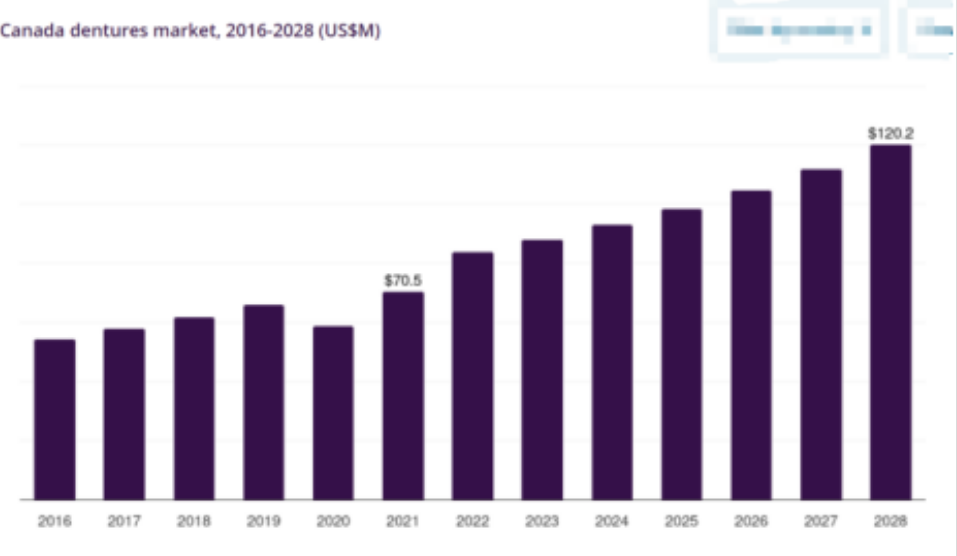
完整义齿(Complete Dentures):2021 年占据最大市场份额(73.76%),主要为活动义齿,满足全口牙齿缺失患者的需求。
部分义齿(Partial Dentures):增长最快的细分市场,预计在预测期内保持高速增长。部分义齿包括固定和活动两种类型,其中固定义齿(如桥接义齿)因稳定性和美观性更受青睐,可能推动该细分市场的增长。
根据加拿大医疗器械规定(CMDR)SOR/98-282第1部分附表1中的16条规定,医疗器械共划分为四种类别,分别是I类、II类、III类和IV类。
大多数义齿及相关材料(如义齿树脂、义齿重衬/修复材料、牙桥、牙冠、义齿涂层、修复基托、人工牙齿、义齿修复套件等)在加拿大根据其产品的特性通常被归为II类医疗器械,而部分带有金属成分的义齿及其相关产品则被分为lll类医疗器械。
如果您想确认您的义齿产品在加拿大的准确风险等级,欢迎咨询Wiselink的技术老师帮您判断!
MDL证书没有有效期,加拿大卫生部会在每年8月1 日至9月1 日之间以邮件形式将证书更新的申请材料发给制造商。每年11月1 日之前需要支付年费用于证书维护,否则证书将会被取消。 技术文件要求: 产品技术规格、设计图纸、性能标准;加拿大HC对型号描述差异要求需要很清晰( 设计图纸要求高 ),不同型号间差异可能会导致产品注册数量的增加; 风险管理报告( 需符合 ISO 14971、涵盖风险分析、评价及控制措施 ); 临床数据( 若产品设计或功能具有特殊性 )。 标签与说明书: 标签和说明书必须符合加拿大双语( 英语和法语 )合规要求。 检测要求: 生物相容性评估报告(需证明材料安全性)。 临床数据风险: 临床数据设计不合理、样本量不足或结论不明确,无法满足 Health Canada 的严格要求; 撰写符合加拿大HC要求的CER文件。 加拿大HC针对CER文件监管: 1. MDL--II类注册过程中,CER文件为非强制性需提交文件 ; 但在注册过程经验中,不排除注册过程中个别审核官员提出需要补交情况。 2. MDL--III类注册过程中,CER文件为强制性需提交文件 ; CER文件监管参照欧盟监管力度。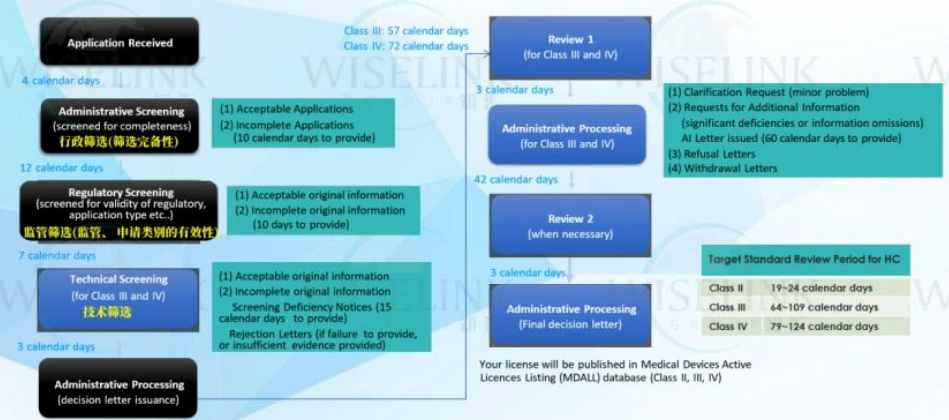

![]()