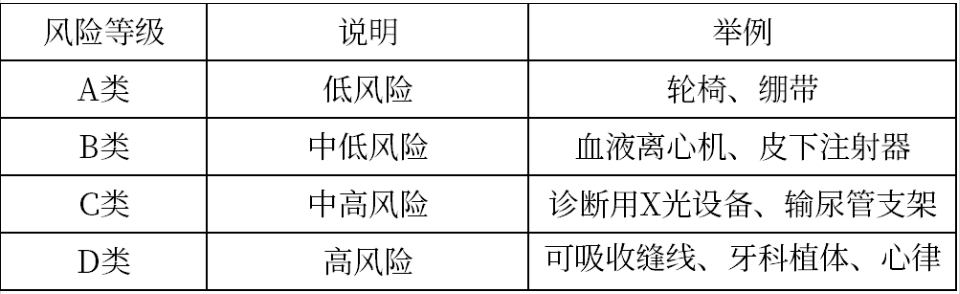
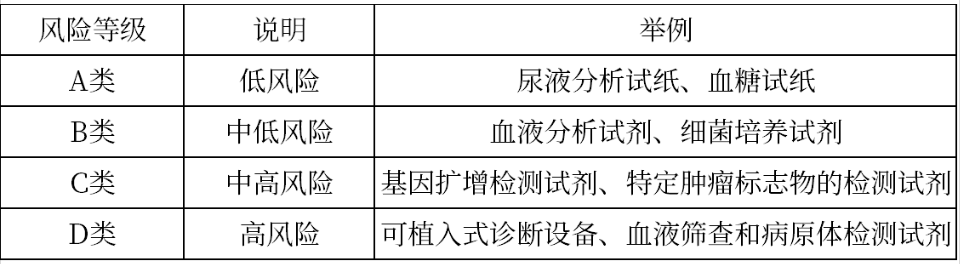
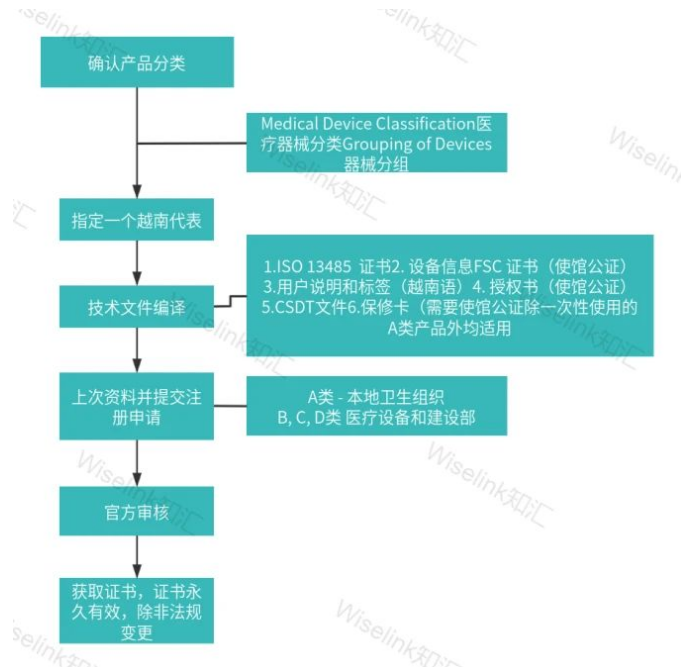
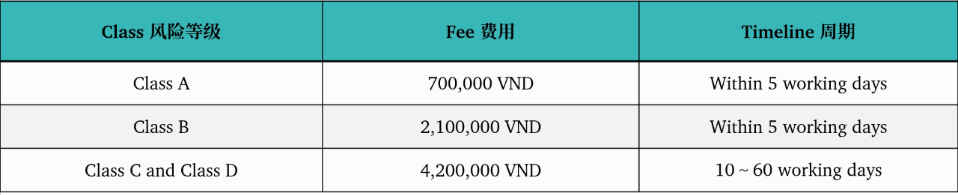
1 越南医疗器械监管部门MOH 1.1 越南监管部门 越南的医疗器械产品注册由越南卫生部药品和医疗器械管理局MOH(Department of Medical Equipment and Construction under the Ministry of Health)下属的医疗设备和建设部(DMEC)监督 ,其主要职责是:负责审核、批准医疗器械的注册和监管,确保医疗器械在越南市场上符合安全性和有效性要求。 1.2 监管法规 第 98/2021/ND-CP 号法令 – 12022年1月1日生效 第111/2021号法令 – 修订第43/2017号法令并更新标签要求 第 05/2022 号通知 – 提供进口前需要注册的产品清单 第 07/2023 号法令 (EN/VN) - 延长进口许可证的有效期并延迟实施 CSDT 申请要求以及其它说明 1.3 风险等级分类 MD-医疗器械 IVD-体外诊断 1.4 注册必须具备的资料 ISO13485证书 FSC自由销售证书 1.5 注册语言 英语+越南语。 2 注册流程|周期|官费 2.1 注册流程 2.2 注册周期及官费 3 越南医疗器械注册常见FAQ Q:越南注册一定需要原产国注册证书吗? A:不强制。 Q:一次性使用的医疗器械注册是否需要提交“一次性医疗器械保修书”,如果是重复使用的医疗器械应该注明什么? A:一次性使用的医疗器械需要提交文件“Explanation letter for single use”,可重复使用的医疗器械需要提供有售后服务能力的证明。 Q:越南证书是否可以转让? A:越南证书不可以转让。 Q:越南是独代吗? A:不是。 了解更多医疗器械注册信息及资讯,欢迎访问wiselinkchina.com官网查询!