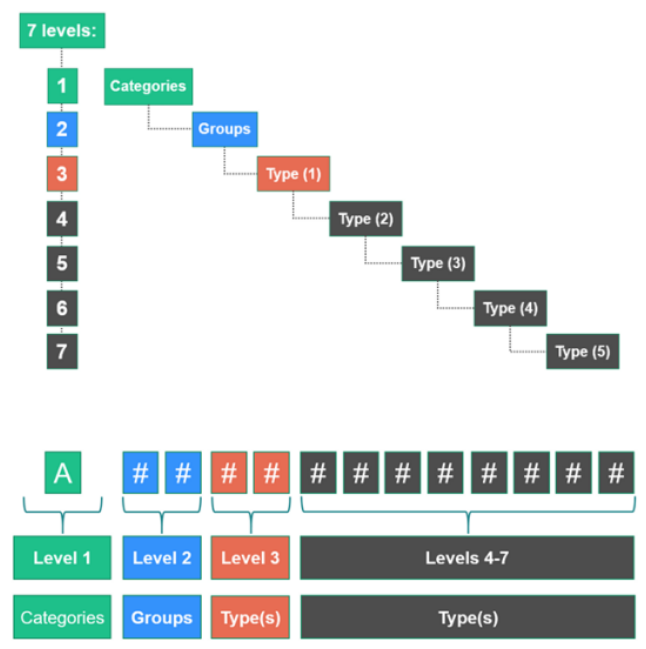
在医疗器械行业,欧盟的监管体系一直是全球最严格的监管体系之一。为了更好地支持欧盟医疗器械法规(MDR)和体外诊断医疗器械法规(IVDR)的实施,欧洲医疗器械命名系统(EMDN)应运而生。 而与之相匹配的文件《FAQ on the European Medical Device Nomenclature (EMDN)》 首次发布于2021年6月,并于2025年1月进行了首次修订,修订内容包括对问题的重新分类以及新增了第7至第24个问题,以进一步完善系统功能和适应行业需求。 本文知汇将为您介绍修订后的关于 EMDN 的24个常见问题,帮助您全面了解这一系统,确保您的企业和产品在欧盟市场保持合规性和竞争力。 根据欧盟医疗器械法规(MDR)第26条和体外诊断医疗器械法规(IVDR)第23条,EMDN旨在支持欧洲医疗器械数据库(EUDAMED)的运行。它将被制造商用于在EUDAMED中注册医疗器械,并与每个医疗器械的唯一设备标识符(UDI-DI)相关联。EMDN的核心作用是为监管机构、制造商、医疗机构和患者提供标准化的设备描述,支持医疗器械的全生命周期管理,包括技术文档审查、上市后监管、警戒和数据分析等。 EMDN的创建基于欧洲委员会和欧盟监管机构在医疗器械协调小组(MDCG)中设定的标准和要求。最初,意大利卫生部的“医疗器械分类(CND)”被选为EMDN的基础。当时,CND在意大利、希腊和葡萄牙等三个成员国已经使用,并支持了众多欧盟和国际制造商的注册。在2019年和2020年期间,经过与利益相关者和专家的多次协商和准备工作,EMDN系统的第一个版本于2021年5月4日发布。 EMDN遵循以下基本原则: 监管机构主导:监管机构在管理、验证、更新和建议命名方面发挥关键作用。 结构化:命名具有透明的层级结构,代码和术语可以有意义地分组。 可预测性:结构和内容保持足够稳定,以适应各种监管用途,同时能够容纳技术创新。 透明性:更新政策健全,反映监管机构和更广泛医疗社区的需求。 包容性:定期审查对所有人开放,基于实际使用和可证明的需求。 可用性:代码和术语对所有用户完全开放。 可访问性:任何制造商或自然人/法人使用命名时不应支付费用或受到歧视。 国际化:在MDR/IVDR实施时获得国际认可。 EMDN对所有利益相关者免费开放,包括制造商、患者、研究机构、医疗机构等。EMDN可以以Excel格式下载,具体链接可在欧盟委员会的MDCG认可文件和其他指导页面找到。 EMDN采用七级层次结构,分为“类别”“群组”和“类型”,其中“类型”进一步细分为多个层级(1°、2°、3°、4°和5°)。每个代码以字母开头,表示设备所属的“类别”,后面跟着两个数字表示“群组”,再后面是一系列数字表示“类型”。代码的最大长度为13位。每个代码都与一个术语相关联,提供对属于同一代码的设备的简洁而精确的描述。 制造商在为设备的UDI-DI分配EMDN代码时,必须使用最细粒度和终端的代码和术语(即树状结构中的最低级别)。这确保了设备描述的精确性和唯一性。 一般情况下,制造商必须为设备的UDI-DI分配唯一最合适的代码。但对于具有多种预期用途的复杂医疗器械系统(例如,具备多种诊断和治疗功能的设备),可以使用多个代码。 如果一个UDI-DI可以分配多个EMDN代码,则不需要对这些代码建立优先级。制造商可以根据设备的实际功能和用途选择合适的代码。 制造商应始终在EMDN的最细粒度级别中(最低层级)寻找最合适的术语。如果最细粒度级别中没有匹配的术语,制造商可以使用“99”作为代码扩展,表示“其他”。但请注意,使用“99”代码的UDI-DI将在年度EMDN审查过程中受到额外审查。 如果EMDN中没有合适的代码,制造商应使用“99”代码扩展(术语“其他”),如第9条所述。 在EMDN提交平台或通过MDCG命名工作组提交新代码的建议,并提供设备的详细描述;在新代码创建后,制造商必须在EUDAMED及相关监管文件中更新注册信息。 制造商可以通过EMDN提交平台或MDCG命名工作组提交更新提案。具体流程和要求请参考年度EMDN更新程序。 每年12月或次年1月,欧盟委员会将在MDCG认可文件和其他指导页面发布EMDN的变更文档,详细说明与前一版本相比的变更内容。 目前没有计划向受变更影响的用户发送通知,用户需要自行关注每年的EMDN更新公告。 是否会对已使用代码的变更进行协商? 目前没有计划联系已使用代码的用户进行协商,用户需要在提交变更提案时提供全面的信息,以确保评估的公平性和全面性。 如果提交的信息被认为不充分,EMDN技术团队可能会联系提交者。为避免不必要的延误,建议提交者在提交时提供全面的信息。 提交者在收到EMDN技术团队的澄清请求后,有15个工作日的时间进行回应。如果超过截止日期,提案可能无法在当年完成处理。 每年的EMDN更新过程中,会特别审查与多个EMDN代码关联的UDI-DI。例如,如果一个制造商为CT系统分配了一个代码,同时又为PET系统分配了另一个代码,可能会考虑创建一个新的代码来涵盖PET/CT组合系统。 每年的EMDN更新完成后,欧盟委员会将在MDCG认可文件和其他指导页面发布最终的变更公告。公告中将包括变更内容、所有提交的提案评估结果(接受/不接受)以及简要描述。 目前没有计划提供重新考虑或重新评估的机制。提交者可以在下一年度的更新程序中重新提交相同的提案,但建议先参考拒绝的理由和新版本的EMDN。 在年度收集过程中,针对同一代码的多个请求将根据以下优先级进行排序: 优先级1:成员国、公告机构、世界卫生组织; 优先级2:经济运营商、行业协会; 优先级3:医疗专业人员、医院、实验室、其他用户。 EMDN技术团队将对所有潜在变更进行评估,以确保变更能够改进EMDN结构,同时尽量减少对现有结构的影响。变更的目标是更好地满足MDR/IVDR的要求。 EMDN的变更旨在改进其使用效果,确保其结构的稳定性和适应性。评估提案的标准包括以下几点: 新增级别:新增级别的提案旨在包含当前EMDN中不存在的设备类型。这些提案通常涉及新技术或需要更详细描述的设备类别。在评估时,会重点关注以下方面: 预期用途:设备的预期用途是否明确且与现有代码不同。 结构特征:设备的物理结构和设计是否独特。 功能:设备的功能是否与现有代码中的设备有显著差异。 材料:设备的构成材料是否具有特殊性。 灭菌和可重复使用性:设备是否为一次性使用或可重复使用,以及其灭菌方式是否独特。 修改现有术语:修改现有术语的提案旨在使现有术语更易于理解或纠正错误。 清晰性:新术语是否更清晰、更准确地描述了设备。 一致性:新术语是否与EMDN的整体结构和风格保持一致。 错误纠正:现有术语是否存在拼写错误、逻辑错误或其他需要修正的问题。 删除现有级别:删除现有级别的提案旨在消除不再使用的代码。 实际使用情况:该代码是否已被市场上的设备广泛使用,或者是否已被其他代码替代。 监管需求:删除该代码是否会影响监管机构对设备的分类和管理。 层级结构合理性:该级别是否更适合放在其他类别、组或类型中。 任何违反EMDN原则(如影响结构稳定性)的提案将被拒绝。例如,如果一个提案会导致EMDN的层级结构混乱或增加不必要的复杂性,那么该提案很可能会被拒绝。 当EMDN中的代码被标记为过时或拆分时,EUDAMED中的处理方式如下: 过时代码: 保留期限:过时的代码不会立即从EUDAMED中删除,而是会保留至少5年。这5年期间,制造商将无法使用过时代码进行设备注册或更新现有注册。 档案维护:过时代码的档案将保持公开,包括过时日期和原因。这有助于制造商和监管机构了解代码的变化历史。 证书和注册:在代码过时后,制造商需要在EUDAMED中更新其设备的注册信息,使用新的有效代码。过时代码的设备在证书到期后将无法续期。 拆分代码: 可见性:拆分的代码将保持可见,但不再作为终端代码使用。这意味着制造商不能使用拆分后的代码进行设备注册或更新现有注册。 档案维护:拆分代码的档案将保持公开,包括拆分日期和拆分理由。这有助于制造商和监管机构了解代码的变更背景。 注册更新:制造商需要根据新的代码结构更新其设备的注册信息,确保设备的分类和描述符合最新的EMDN要求。 制造商需要在合理的时间内更新EUDAMED中的相关代码,具体要求如下: 更新时间:制造商和公告机构应在每年EMDN更新完成后,尽快在EUDAMED中更新相关代码。最晚应在下一次年度监督审核之前完成更新。 文档更新:制造商需要在相关文档中反映代码的变更,包括证书、符合性声明等。这确保了设备的注册信息与最新的EMDN保持一致。 年度审核:由于EMDN的年度更新通常在每年1月发布,因此制造商需要在年度监督审核之前完成所有必要的更新。如果审核在年初进行,制造商可能需要在审核后尽快完成更新。 持续关注:制造商应将定期检查EMDN更新作为标准操作程序,以便及时发现可能影响其产品组合的变更,并提前通知公告机构。