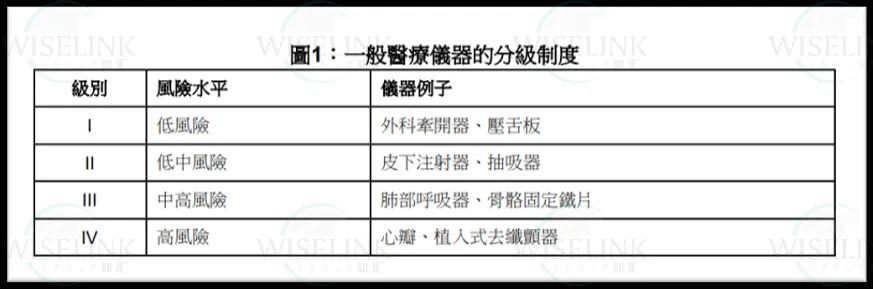
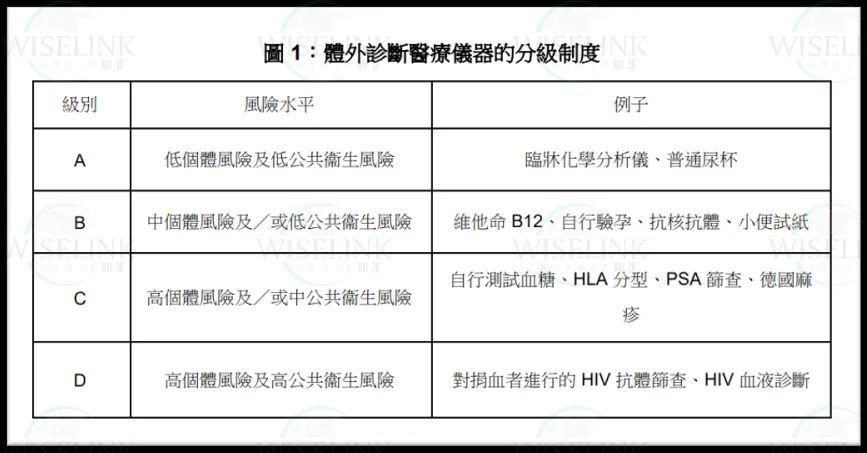
随着医疗技术的发展,医疗仪器的监管显得尤为重要。香港特别行政区为了确保市民使用医疗仪器的安全,制定了一套医疗仪器行政管理制度(MDACS)。WISELINK 知汇整理了相关的文件资料,本文将为您简单解读这一制度的核心内容。 提高安全意识:通过监管医疗仪器,提高市民对使用安全性的认识。 协助从业人员熟悉规定:帮助医疗行业人员了解未来的强制性规定。 收集行业资料:为未来的法规改进收集意见和资料。 列表制度:医疗仪器科备存并更新包括符合安全及性能标准的医疗仪器列表,以及进口商、分销商和本地制造商的列表。 本地负责人制度:制造商如在香港无注册地址,须委任本地负责人承担相关责任。 医疗事件呈报制度:涉及列表仪器的须呈报事件必须向医疗仪器科报告。 根据香港医疗仪器行政管理制度的规定,不属于医疗仪器范围的产品包括以下几类: 药剂制品及先进疗法制品:包括受《药剂业及毒药条例》(第138章)规管的药剂制品,但结合医疗仪器及药品于一身的产品,如果药品辅助仪器对人体发挥作用,则作别论。 人类血液、血液制品、源自人类的血浆或血细胞:或在推出香港市面时或使用时包含人类血液、血液制品或源自人类的血浆或血细胞的仪器,但如果仪器包含人类血液、血液制品或源自人类的血浆或血细胞的衍生物,并辅助仪器发挥作用,则作别论。 源自人类的移植物、组织或细胞:或衍生物、或包含组成该等组织或细胞的产品,但如果产品是包含以非存活人类组织活细胞,或从人类组织衍生出来的非存活产品制造的仪器,并辅助仪器发挥作用,则作别论。 源自动物的移植物、组织或细胞:或衍生物或包含或组成自该等组织或细胞的产品,但如果产品是包含以非存活动物组织活细胞,或从动物组织衍生出来的非存活产品制造的仪器,并辅助仪器发挥作用,则作别论。 个人防护装备:但拟用以保护病人的则除外。 拟接触人体外各部位的物质或制剂:如表皮、毛发系统、指甲、口唇及外生殖器、牙齿或口腔粘膜,而其目的纯粹或主要用作清洁该等部位、改变其外观、及/或改善体臭,及/或给予保护使其处于良好状况以求美观。 不拟作诊断疾病、治疗临床情况、控制受孕(包括避孕)或消毒医疗仪器的家居及化妆品:包括作化妆用途的家庭用品。 屋宇设备。 专门改善空气素质的设备:但如该设备已成为医疗仪器一部分或设计为医疗仪器配件,则作别论。 经翻新的医疗仪器。 个人化医疗仪器:但病人匹配医疗仪器和适应性医疗仪器除外。 非临床用途的仪器:包括只供研究用途(RUO)、只供教学用途、只供一般化验室使用、只供在展销会、展览会或示范会中展出或示范用途。 以上产品根据香港医疗仪器行政管理制度的规定,不被纳入医疗仪器的现行覆盖范围。 包括产品:结合医疗仪器及药品的产品,如果药品辅助仪器对人体发挥作用,则视为医疗仪器。 采用IMDRF公布的分级规则,将医疗仪器分为4级(第I至IV级),体外诊断医疗仪器分为四级(第A至D级)。 本地负责人需证明仪器符合安全及性能基本原则。 本地负责人的角色与责任: 1.5.1 委任本地负责人的必要性: 作为使用者、制造商、进口商、分销商及政府之间的沟通中心。 1.5.2 本地负责人的责任: 沟通渠道:与各方沟通,处理市面前后的事宜。 仪器列表申请:负责与政府进行所有必要的联系。 供应记录:保存进口商、分销商和医疗仪器供应记录。 处理投诉:设立投诉处理程序,提供联系信息。 维修保养:提供或安排维修服务。 特定仪器追踪:对高风险仪器进行追踪。 产品回收及安全通知:管理产品回收及安全通知。 1.5.3 医疗仪器列表事宜: 申请资格:仅限仪器的本地负责人申请。 申请流程:通过医疗仪器信息系统(MDIS)提交申请。 审批时间:一般在提交申请及所需文件后12周内完成审批。 上诉机制:本地负责人可在得知决定后14个工作日内提出上诉。 列表批准效力:仪器列表的批准或有条件批准有效期为5年。 香港特别行政区对医疗仪器的行政管理制度是全面且严格的,旨在确保医疗仪器的安全性和有效性,保护公众健康。 A:目前,香港并无特定法例规管医疗仪器的临床研究。但这并不意味着制造商不需要进行临床研究。 A:有意申请把仪器纳入「医疗仪器列表」的制造商,如在香港没有注册营业地址,则须在提出申请前委任一名本地负责人 (LRP) 。 A:本地负责人须在 5 年有效期届满前最少12周至1年内 (包括首尾两天),向医疗仪器科递交表列医疗仪器的续期申请。续期申请必须在上述期限内送达医疗仪器科,否则医疗仪器科将不会处理该续期申请。 A:卫生署可在下列情况下,有权酌情把仪器从「医疗仪器列表」上永久或暂时删除: ①卫生署基于公众健康或安全考虑,认为有需要把仪器从列表上删除,如制造商或本地负责人未能处理或妥善处理仪器所构成的危险; ②制造商或本地负责人未能符合医疗仪器行政管理制度的规定或任何批准表列条件; ③制造商或本地负责人未能完全遵从卫生署的指示,从宣传中撤回没有充分理据的声称; ④制造商或本地负责人已清盘或不复存在; ⑤制造商或本地负责人要求除名。 A:原产国注册并不是香港注册的先决条件,但如果有全球医疗器械协调工作组(IMDRF)五个创始成员国(欧盟、澳大利亚、加拿大、日本和美国)的任意一个国家注册证,能够加速在香港的注册。