一、阿联酋医疗器械市场分析
阿联酋的医疗器械市场规模和份额在过去几年呈现持续增长的趋势。根据阿联酋通讯社的报告,预计到2025年,阿联酋的医疗器械市场将达到56亿迪拉姆,2020-2025年的年复合增长率(CAGR)为4.4%。
随着阿联酋政府对医疗基础设施的持续投资,医疗器械市场将迎来更多的发展机遇。外国医疗器械制造商要想进入阿联酋市场并取得成功,必须密切关注市场动态和法规变化,以及不断提升产品质量和科技水平,以满足市场的需求。
二、阿联酋医疗器械监管机构及法规要求

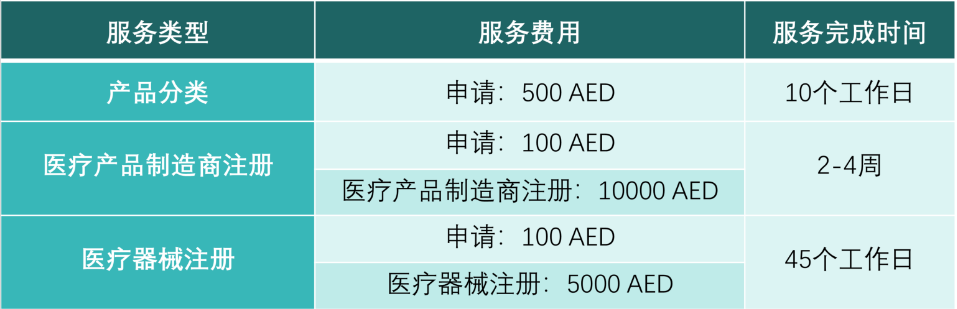
在阿联酋销售医疗器械需要符合一系列的法规和标准。阿联酋的医疗器械市场监管部门主要是阿联酋药品和医疗器械管理局(Dubai Health Authority)和阿联酋国家卫生部(Ministry of Health and Prevention),负责监管和审批医疗器。进口商和制造商需要确保其产品符合相关的规定,并获得必要的许可证和注册证书。 三、阿联酋医疗器械分类原则 阿联酋MOHAP(阿联酋国家卫生事务部)对医疗器械的分类分为以下四个类别,Ⅰ、Ⅱ、Ⅲ&Ⅳ类,Ⅳ类为最高风险类别。 四、阿联酋医疗器械注册流程及路径 注册流程: Step 1:卫生部分类 医疗器械产品进入阿联酋前首先需要申请分类,MOHAP将审查您的产品,并确认您的医疗器械将按照哪个风险类别进行注册。 一般需要10个工作日,并要求提供如下文件: ●产品图片 ●英文/阿拉伯文的宣传手册/商品信息 ●产品目录 ●带有清晰可读的商品名称和信息的内包装标签及外包装标签 ●原产国监管机构出具的与所提交医疗器械相关的证书(如:CPP、FSC、CFG、CE、ISO等) ●阿联酋身份证或申请人的护照或贸易许可证或药店许可证(取决于用户类型) Step 2:制造商场地注册 在进行产品注册之前,根据法规要求,制造商需要在MOHAP网站先提交材料并支付一定的费用,用于进行制造商场地注册。 一般需要2-4周,证书有效期为5年。 注册医疗器械制作商场地所需文件: ●公司出具含有公司抬头、logo等信息的合法信函,由公司负责人签名盖章,授权阿联酋当地代表向MOHAP提交注册文件 ●由原籍国主管当局颁发的ISO 13485证书 ●需要原产国主管当局颁发的营业执照/制造许可证(需通过在该原籍国的阿联酋大使馆公证) ●产品清单 ●详细的公司简介和产品手册 Step 3:医疗器械注册 完成以上两个步骤后,就可以进行医疗器械注册了。 注册过程一般需要45个工作日,证书有效期为5年。由于需要提交的各类文件数量繁多,且不同分类的医疗器械所需要提交的文件各不相同,因此,在收到医疗器械说明书及具体细节文件后,知汇将会和您分享需要提交的具体文件清单细节。 五、阿联酋医疗器械注册所需费用及时间