一. 新加坡医疗器械市场分析
新加坡预计2024年的医疗器械市场收入将达到10.84亿美元,其中心脏病学设备是新加坡医疗器械市场中规模最大的类别,2024年规模约为1.564亿美元。预计2024至2029年将以9.16%的复合年均增长率增长,到2029年市场规模将达到16.8亿美元。新加坡凭借其医疗创新技术和强大的监管框架在医疗器械市场中处于领先的地位。

二. 新加坡医疗器械监管机构及法规要求
监管机构:新加坡医疗器械注册是由Health Sciences Authority(HSA)卫生科学局的医疗器械监管部门负责监管。
法规要求:
1. the Health Products Act 2007,《2007 年健康产品法》
2. Health Products (Medical Devices) Regulations 2010,《2010 年健康产品(医疗器械)条例》
三. 新加坡医疗器械定义及分类
定义:
医疗器械是指直接或间接用于人体时产生物理或机械效应的健康产品。这些器械的使用旨在达到以下预期目的:
体外诊断试剂也是由低风险到高风险分为:A/B/C/D四类。
2. 提交完成并支付费用后,由HSA当局审查医疗器械申请。
3. 审查文件后,HSA当局将通过 MEDICS 生成输入请求,以请求进一步的文件和说明。
4. 所有信息交流均通过 MEDICS 系统进行,该系统会自动向申请人的电子邮件地址发送消息。
5. 在此阶段,HSA 将再次评估提交的内容,如果成功,将发出批准通知。
6. 尽管 A 类医疗器械无需进行产品注册,但在投放新加坡市场之前,必须符合法规中规定的《医疗器械安全和性能基本原则》,所有 A 类医疗器械都必须通过 MEDICS 提交豁免清单。
7. 如果医疗器械获得了美国FDA、欧洲EU NB、澳大利亚TGA、日本MHLW或加拿大HC等参考国的认证,那么拥有多个参考国认证的医疗器械在注册时将享受简化的审核流程。具体可以咨询Wiselink知汇。
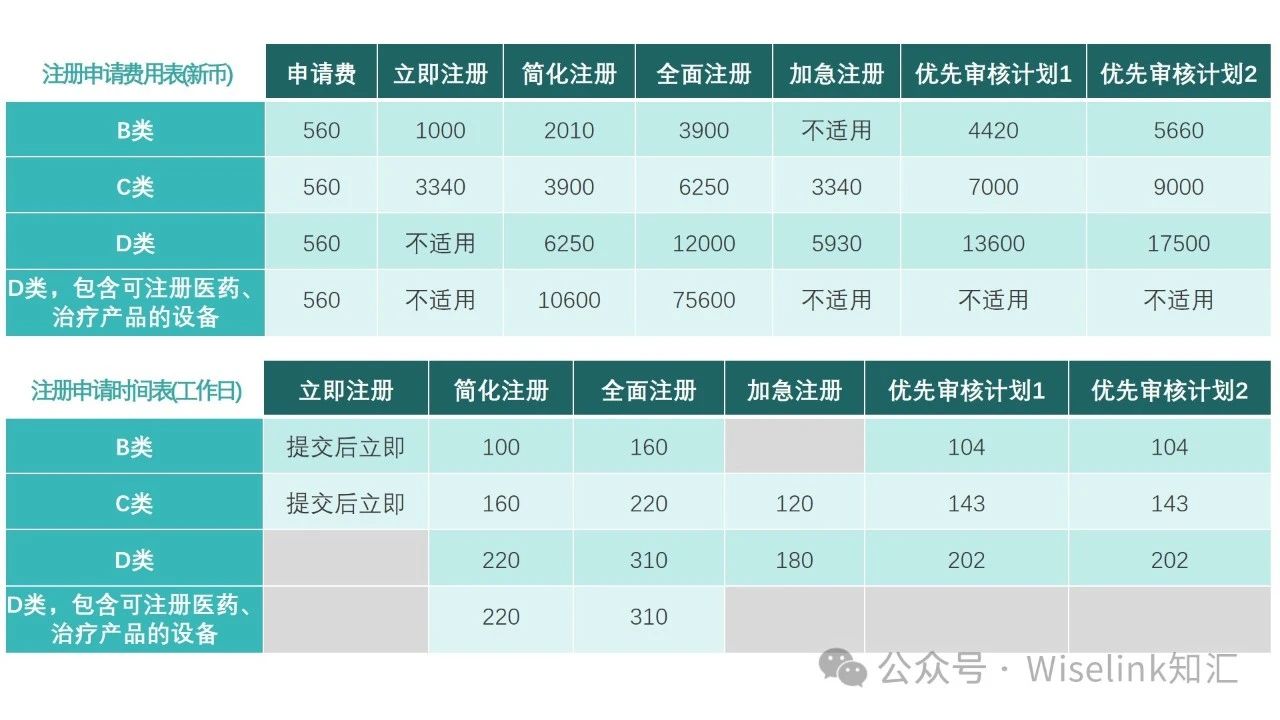
(二)注册路径:
C类分为立即、全面、简化、加急注册
D类分为全面、简化、加急注册
D类(含有可注册药物)分为简化和全面注册
(1)全面审核注册是指产品没有在上述五个参考国家的注册历史。
(2)简化注册是指产品至少得到一个参考国家的注册历史。
(3)C类的加急注册需要满足:至少有一个参考国家的注册历史,且产品上市3年内没有不良事件的发生,或有至少两个参考国家的注册历史;D类的加急注册:至少要有两个参考国家的注册历史。(不包含可注册药物的D类器械)
(4)B类的立即注册需要满足:至少有一个参考国家的注册历史,且产品上市3年内没有不良事件的发生,或有至少两个参考国家的注册历史;C类的立即注册只能是独立软件,且至少有一个参考国家的注册历史。
如果您对注册路径有更多疑问,可以咨询Wiselink知汇。
(三)除上述四种路径之外,还有两条全面审核路径下的优先审核计划。
分别是优先审核计划1和优先审核计划2,这两种计划可以为医疗器械提供更快的注册和市场准入。
需要注意的是该计划仅适用于按照全面审核途径提交的 B、C 和 D 类器械,不包括以可注册药物为辅助作用的 D 类器械。优先审评计划的周转时间(TAT)比标准全面途径的周转时间短 25%。
申请优先审核计划1的医疗器械需要满足以下两个标准,不符合以下两个标准的医疗器械可以申请优先审核计划2。
此次知汇助力合作伙伴获得批准的C类IVD耐药五联检产品便是通过全面审核路径,由于该产品之前没有上述五个参考国家之一的注册历史,所以只能通过全面审核路径完成。如果您对全面审核路径有疑问,可以咨询Wiselink知汇以获取详细的信息。
五. 新加坡医疗器械注册所需文件清单
该文件清单以全面审核路径下的C类医疗器械注册所需文件为例
1. 执行摘要