一. 什么是UDI?
Unique device identifiers(UDI)—唯一设备标识符,是在美国销售医疗器械的要求,并且正在逐步被欧盟和其他国家/地区采用。UDI 系统旨在通过提供以下功能使医疗保健提供者、制造商、授权卫生当局、医院和机构以及个人消费者受益:
1.卫生当局可以更快地发现可能存在缺陷的医疗器械信息。
2. 更快地访问已召回医疗器械信息并了解当前库存。5. 确保有关植入设备的信息得到安全保留并后续可追溯。UDI 时间表和截止日期因市场和产品而异,并且在一些国家和地区已多次修订。Wiselink知汇为您详细整理了已宣布具体计划的国家和地区的 UDI 截止日期。请注意,随着参与国和地区调整其计划,这些日期可能会发生变化。随着更多信息的出现,Wiselink知汇将持续更新。
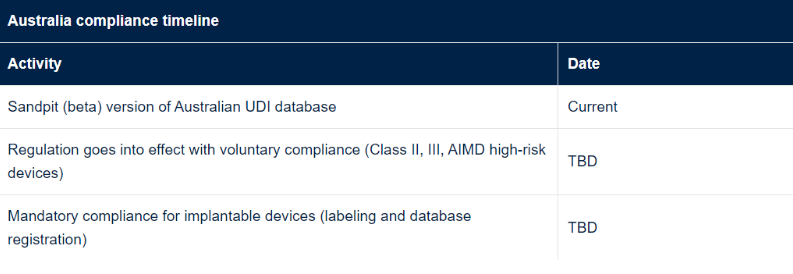
二. 澳大利亚UDI要求
澳大利亚TGA 宣布,将按照医疗器械分类逐步分阶段强制合规,首先是高风险和植入式医疗器械,随后几年将是风险级别较低的医疗器械。直到 2024 年医疗器械法规更新后,强制合规可能才会生效。
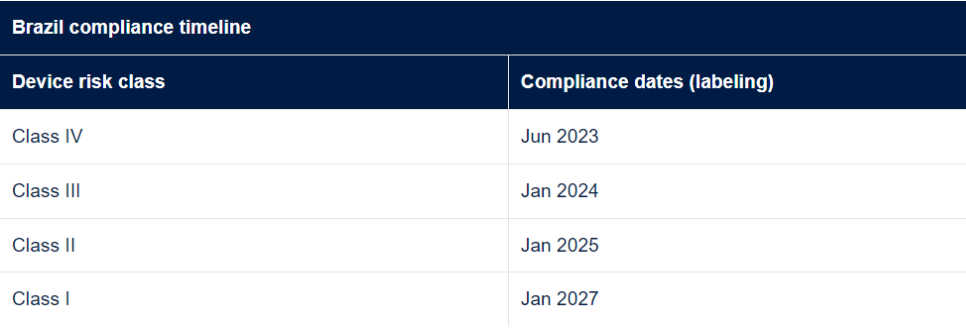
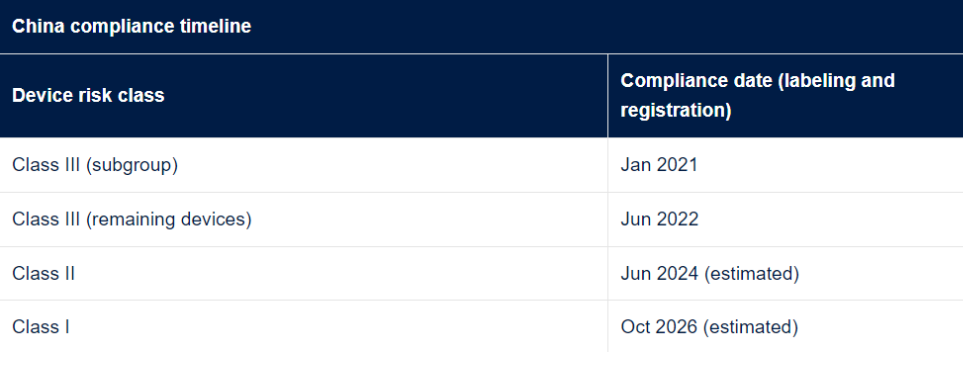
自 UDI 法规生效之日起,Sponsor和医疗器械制造商可以选择自愿遵守 UDI 要求。自法规生效之日起至少 12 个月后将开始强制遵守。UDI (AusUDID) 报告数据库也仍处于生成阶段。2022 年 1 月 10 日,RDC 591/2021 生效,该法规要求巴西监管机构 ANVISA 监管的设备进行 UDI 标签和数据库注册。该法规要求根据风险等级灵活实施,并建立巴西UDI数据库。对于 UDI 信息直接放置在产品上的可重复使用器械,下面的过渡期额外增加了两年。UDI 报告数据库的详细信息以及相关合规日期尚未公布。其他信息可在此处找到:“https://in.gov.br/en/web/dou/-/resolucao-rdc-n-591-de-21-de-dezembro-de-2021-370622845”.加拿大卫生部提出了一个严格基于IMDRF 国际 UDI 指南的UDI 框架。当前的提案涉及要求所有医疗器械设备都贴上 UDI 标签,I 类低风险医疗器械设备除外。加拿大卫生部打算开发一个 UDI 数据库或修改现有的医疗器械有效许可证列表数据库 (MDALL) 以容纳 UDI 数据。五. 中国UDI要求
除了标签要求外,中国还要求将 UDI 记录在中国国家 UDI数据库中,作为医疗器械注册的一部分。有关中国 UDI 要求的更多信息(中文链接:https://www.gov.cn/gongbao/content/2019/content_5462534.htm)来自中国国家药品监督管理局官网。
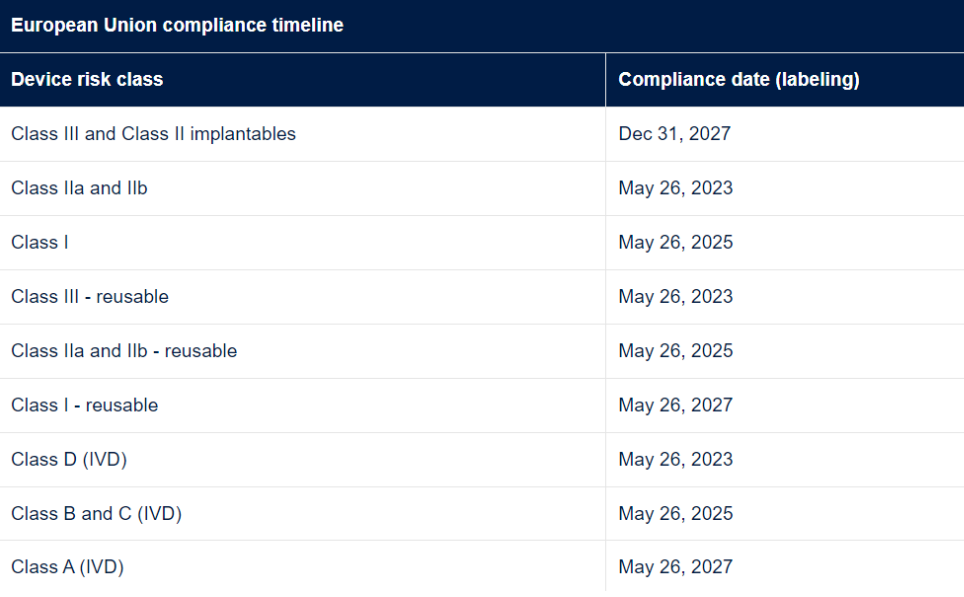
六. 欧盟 UDI 要求
根据欧洲 MDR 和 IVDR 法规的初步规定,在所有模块均被宣布完全功能之前,可能不会强制要求 EUDAMED 的行业使用。在过去的几个月中,发布了 MDR/IVDR 修订提案,建议在每个 EUDAMED 模块经过审核并宣布功能后逐步实施各个模块。发布该提案的目的是加快 EUDAMED 模块的推出,因为每个模块都已最终确定,以便行业实施和采用,而不会造成额外的、不当的延误。EUDAMED 的 UDI 模块目前可供自愿使用,根据拟议修正案的规定,可能会在 2025 年末强制行业使用,预计过渡期从 UDI 模块准备就绪时开始。有关欧盟 UDI 系统和要求的其他信息:
“https://health.ec.europa.eu/medical-devices-topics-interest/unique-device-identifier-udi_en”
七. 印度UDI要求
2021年底,印度推迟了UDI要求在印度的实施,并且尚未设定新的截止日期。最初,《2017 年医疗器械规则》第 46 条规定,要求在 2022 年 1 月 1 日之前为获准在印度制造、销售、分销或进口的医疗器械贴上 UDI 标签。关于UDI需要如何显示以及需要包含的具体信息的详细信息尚未发布。
八. 日本UDI要求
日本是标准化条形码的早期推动者,但仍在努力协调其要求与全球 UDI 同步。自2022年12月起,根据器械类型,医疗器械的直接容器/包装材料/零售包装需要基于国际标准的条形码标签。预计条形码将显示在供患者使用的每件药品和医疗设备上。此外,应推广在临床环境中使用条形码标签的安全措施,以及 MAH 在数据库中注册生产信息。
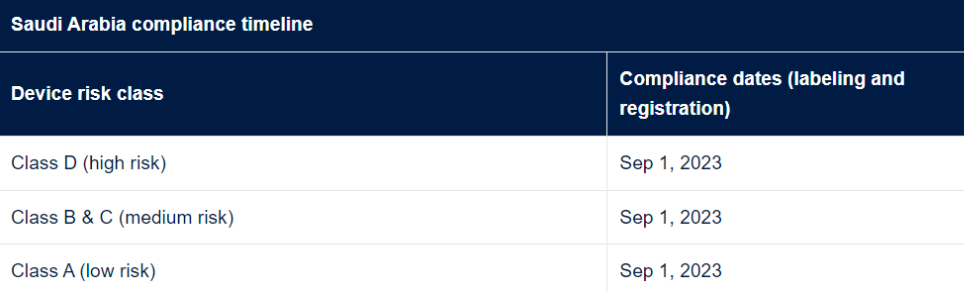
九. 沙特阿拉伯 UDI 要求
沙特阿拉伯自 2020 年 10 月 1 日起允许自愿 UDI 注册,但 B、C 和 D 类设备的强制合规性于 2023 年 9 月 1 日生效。这些要求适用于标签和数据库 (SaudiDI) 注册。在合规日期之前进口的医疗器械可以在没有 UDI 信息的情况下进行分发,直到完全可执行之日后一年。但是,此例外不适用于直接标记 (DM) 要求,直接标记是设备本身上 UDI 的永久标记。有关更多信息,请参阅沙特阿拉伯指导文件:“https://www.sfda.gov.sa/sites/default/files/2022-06/RequirementsUDI_0.pdf”
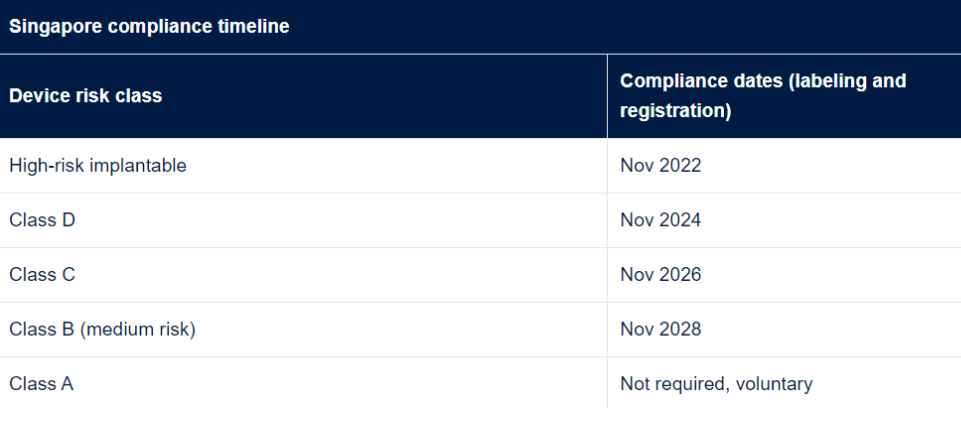
新加坡要求遵守基于分类和分阶段方法的UDI 标签或数据库注册法规。新加坡将接受已在美国和欧盟销售的医疗器械设备的 UDI 标签,否则 UDI 将需要遵守新加坡 HSA 的所有准则,包括与 HSA 指定的 UDI 发行实体合作。新加坡还允许公司在下列 11 月截止日期之前进口医疗器械 6 个月的宽限期。新加坡医疗器械 UDI 系统指南:
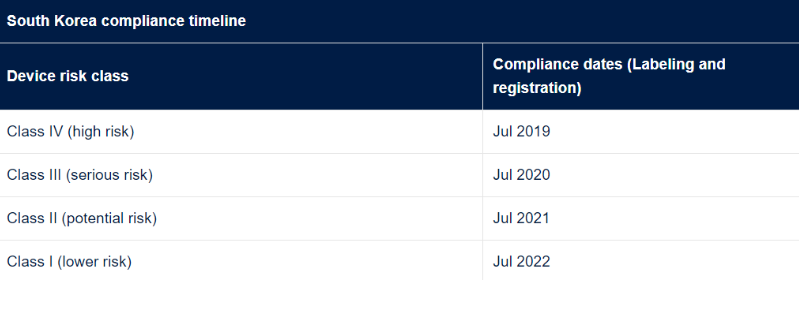
“https://www.hsa.gov.sg/docs/default-source/hprg-mdb/guidance-documents-for-medical-devices/gn-36-r2-guidance-on-medical-device-udi-system-(2022-july)-pub.pdf?sfvrsn=b2c113ad_2”(GN-32-R2)”.韩国UDI 合规性是强制性的,并由《医疗器械法》(第 14330 号)第 20 条和《医疗器械法执行条例》(第 1512 号)第 54-2 条实施。请注意,韩国法规提到“综合医疗器械信息系统”或 IMDIS,这是他们的 UDI 数据库和“医疗器械标准代码”,即 UDI 代码本身。作为引入 UDI 的一部分,韩国还要求医疗器械制造商提供设备每月供应历史报告,要求自 UDI 合规日期起 1 年内提供。
了解更多有关韩国UDI要求的可以阅读以下韩国法规:
"https://www.nids.or.kr/board/view.jspi_mst_idx=&i_current_page=6&board_seq=&flag=view&data_seq=7733&user_id=&page=sdcode&mnu=19&tabno=0&category=1&search_gbn=title&search_value="
“https://law.go.kr/lsInfoP.dolsiSeq=188095&lsId=009740&chrClsCd=010202&urlMode=lsInfoP&viewCls=lsInfoP&efYd=99990101&vSct=%EC%9D%98%EB%A3%8C%EA%B8%B0%EA%B8%B0#0000”
“https://law.go.kr/admRulLsInfoP.doadmRulSeq=2100000073289&vSct=%EC%9D%98%EB%A3%8C%EA%B8%B0%EA%B8%B0”
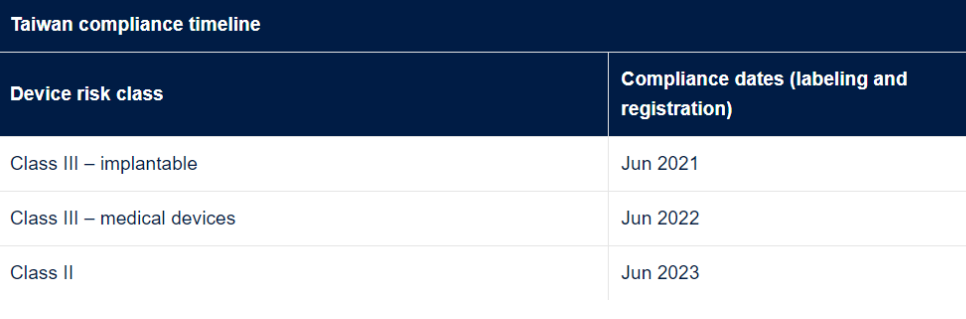
台湾已经实施了 UDI 法规,其中包括标签和数据库报告要求。UDI 报告数据库称为台湾 UDID (TUDID),有 23 个必需的数据元素。但是,如果医疗材料满足以下条件之一,则可以免除UDI:A.定制医疗器械
B.出口专用医疗器械
C.医疗器械包装中的非植入性医疗器械部件和单件体外诊断医疗器械包装中的非植入式医疗器械部件,仅供使用,不得单独使用和出售。
请阅读台湾 FDA 的指导文件了解更多信息:
“https://www.fda.gov.tw/TC/newsContent.aspx?cid=5072&id=26490”.
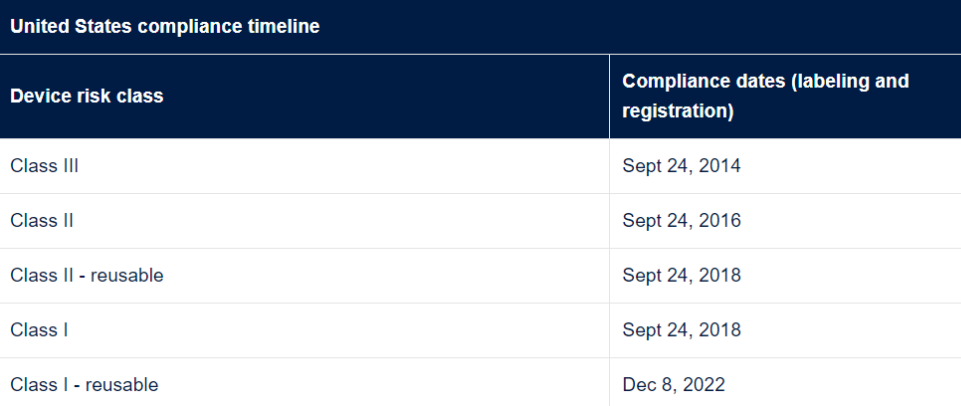
美国要求所有设备遵守标签和数据库要求。FDA 不打算在 12 月 8 日之前对 I 类和非分类设备强制执行 GUDID 提交要求,但植入式、生命支持或生命维持设备 (I/LS/LS) 除外,无论它们是否是消费者健康产品。
植入式生命支持或生命维持医疗器械设备,包括 II 类/LS/LS 设备,也应符合 GUDID 提交要求。美国FDA要求所有UDI信息均输入美国特有的GUDID数据库。有关更多信息,请参阅FDA UDI链接:https://accessgudid.nlm.nih.gov 和 https://www.fda.gov/medical-devices/device-advice-comprehensive-regulatory-assistance/unique-device-identification-system-udi-system”.
知汇Wiselink CN拥有包括原澳大利亚药品监督管理局局长Dr. Derrick Beech为首席顾问的国际专业团队,秉承源于澳洲、扎根中国、服务世界的精神,信守专业、真诚、开放的核心价值观,致力于为医疗器械、化妆品、食品、保健品和中药制造商提供全球合规认证和临床试验服务。