


一
印度尼西亚医疗器械监管机构
二
印度尼西亚医疗器械监管机构
印度尼西亚进口医疗器械注册适用法规:http://www.wiselinkchina.com/IndonesiaBPOMcertified/
三
印度尼西亚医疗器械法规分类规则
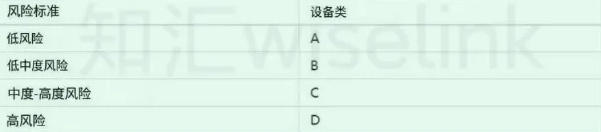
四
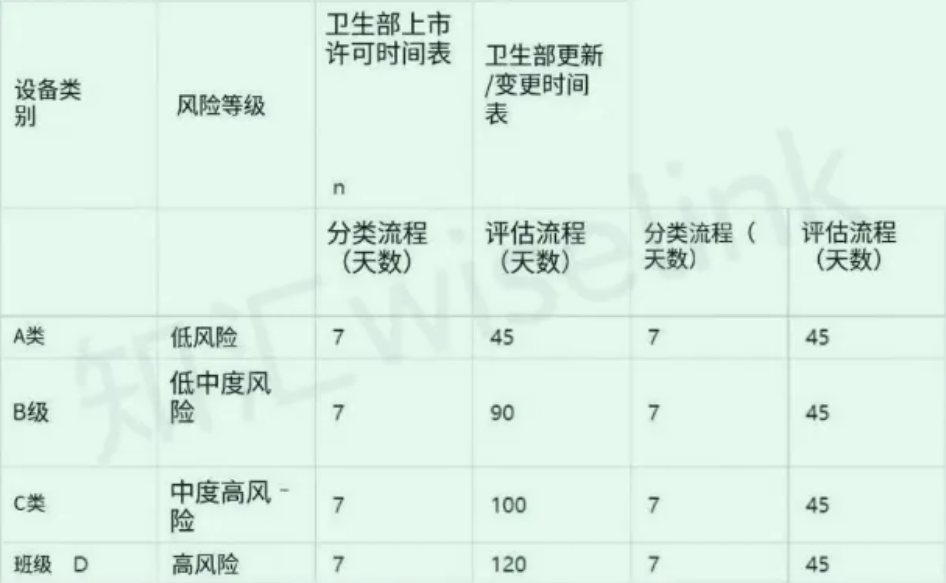
印尼医疗器械注册流程
印度尼西亚LAR必须在在线门户中创建一个账户。所有设备类别的注册过程都是一样的。然而,对文件的要求因设备类别而异。注册是一个两阶段的过程,即:
1、预注册过程
2、评估过程
卫生部核实设备的分类并确定评估费用。预注册的结果和发票将通过电子邮件发给申请人。当地代表代表制造商支付费用并上传支付证明。卫生部将审查这些文件,并通过电子邮件将结果发送给申请人。有些设备需要在认可的实验室进行国内测试。
五
关于印尼注册Q&A?
http://www.wiselinkchina.com/IndonesiaBPOMcertified/
Q:注册过程产品是否需要进行本地测试(型式测试/样品测试)?
——不需要,在印尼注册医疗器械通常不需要进行本地测试。
Q:完成注册需要进行临床试验吗?
——注册时可能需要临床试验,但在大多数情况下,国外临床资料是可以的。
Q:注册流程需要原产国的批准吗?
——在印度尼西亚注册大多数情况下需要原产国的批准。需要提供自由销售证明。
Q:申报资料格式
——基于东盟通用提交资料模板ASEAN CSDT的基础上略做修订。
Q:注册证有效期是多久?
——在LOA生效后5年。在注册证届满前至少6个月提交延续注册申请
Q:取证后发生变更怎么办?
——生产地址、商品名、适应症、产品/证书持有人发生变化,需要新注册;新增型号、标签和/或IFU微小变更,灭菌场地和/或方法(产品技术规范不变)变化,可以进行变更注册。
Q:知汇Wiselink可以为大家提供办理印尼或其他国际注册的全程服务吗?
——可以的,知汇wiselink母公司隶属于澳洲悉尼,在国际市场上有着丰富的资源,无论是医疗器械、药物等认证注册代办或是海牙认证等,我们都有着为您快速、高性价比办理的能力和资源,提供一站式服务。如果在相关国际认证注册方面有着疑问或需求,欢迎随时与我们取得联系。


