当地时间2024年2月20日,美国FDA提醒器械研究的发起人和器械制造商认真评估他们参与进行性能测试的第三方,并在提交给FDA之前独立验证所有测试结果。设备公司有责任对生成数据的第三方进行资格认证,并确保提交给FDA的所有信息是真实和准确的。
一、FDA发现有第三方测试实验室伪造数据
近年来,FDA注意到越来越多与器械公司签订合同进行医疗器械测试的实体(“第三方测试实验室”)正在生成伪造的测试数据,复制其他器械提交的数据,或者其他不可靠的测试数据,但FDA希望器械公司能够识别出表面上不太可能或不可能的测试结果,或者似乎与器械的已知信息不一致。当这些数据提交给FDA时,该机构无法依靠它们来授予上市许可,并且会质疑整个文件的数据完整性。
以下是在FDA获得ASCA资质的中国实验室:
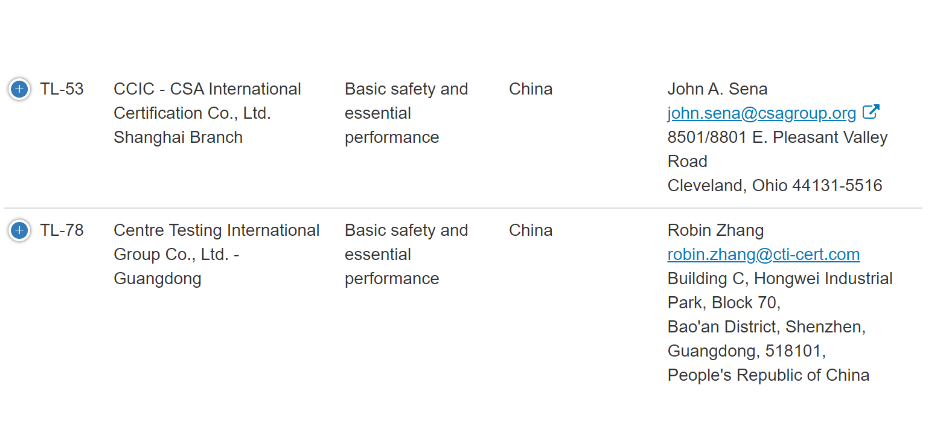
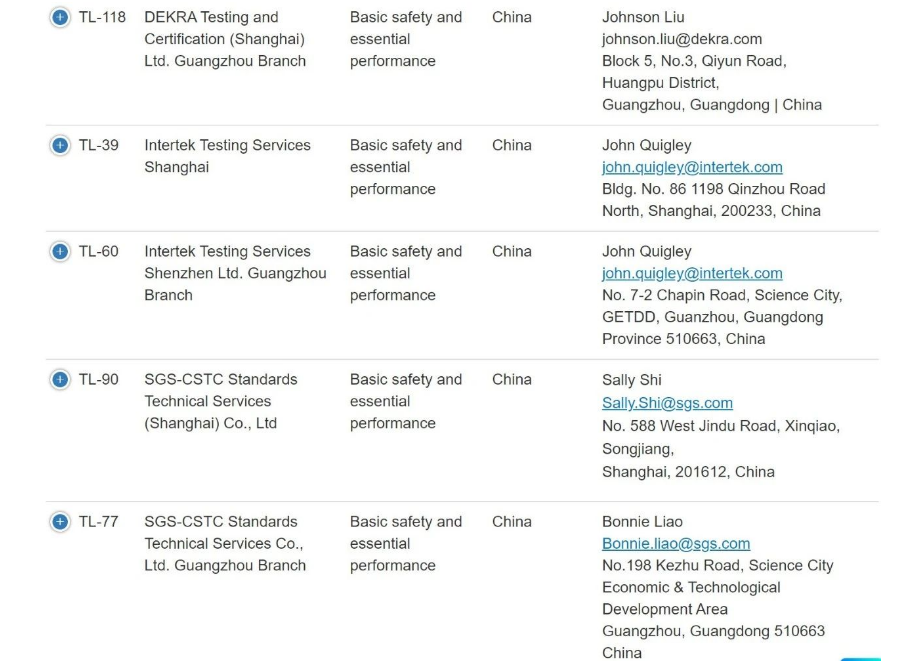

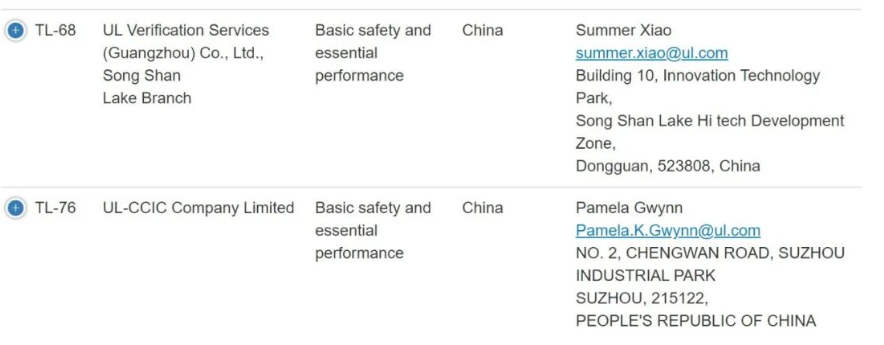
(1). FDA已经发现,第三方检测实验室(包括中国和印度的许多此类实验室)生成的不可靠数据提交量有所增加。这一令人担忧的趋势导致FDA无法达到实质性等效的确定或以其他方式授权提交包含此类数据的医疗器械的营销。
(2). 在这些情况下,当设备无法获得授权时,提交申请的赞助商和制造商显然会受到直接影响。这些负面决策的另一个影响是减少了患者和医疗保健提供者获得新设备的机会,并可能破坏设备供应链。为了制止这种情况,设备公司需要加倍努力。
(3). 为了保护患者和医疗保健提供者免受不合格产品的影响,并确保美国患者能够获得安全、有效和高质量的医疗器械,FDA正在采取各种行动,包括通过我们的生物研究监测计划,识别和应对数据完整性违规行为。与此同时,FDA呼吁医疗器械行业保持警惕,积极主动地确保医疗器械提交文件中所有数据的完整性。
三、ASCA相关介绍:
ASCA Pilot,全称为Pilot Accreditation Scheme for Conformity Assessment Program,即符合性评估认定计划,是自愿参加的试行项目。参加该项目之后,在入市前医疗器械审核中,可增加FDA评估ASCA认可标准的一致性和可预测性。目前ASCA试行项目认可的标准,覆盖生物相容性、安规性能测试等相关标准,目前ASCA试行项目共纳入了94个标准,这些标准的测试,可考虑在有ASCA认定资质的测试实验室进行。ASCA试行项目,与制造商最相关的好处是,可增加产品测试的可信度,并减少制造商在测试报告上的审核负担,不递交完整报告(可递交总结报告,由ASCA认定的测试实验室提供),并可减少FDA对测试报告的AI问题。
原文链接:
https://www.fda.gov/medical-devices/industry-medical-devices/fraudulent-and-unreliable-laboratory-testing-data-premarket-submissions-fda-reminds-medical-device
ASCA实验室网址:
https://www.fda.gov/medical-devices/division-standards-and-conformity-assessment/asca-accredited-testing-laboratories






