

无论MDR咨询公司如何向外界宣称他的高大上,但是,一个无争的事实就是,低风险产品的业务量永远都占公司业务的绝对多数的比重,也是咨询机构业务利润的主要来源。高风险产品虽然咨询费用看似巨大,但是咨询机构投入的资源也是巨大的。最后基本都很难给公司带来实际的利润。
对于一类医疗器械,很多人可能有些误解,认为只需要一个自我申明,即可在欧盟市场上自由销售。也有人心有执念,一心想要获得公告机构颁发的所谓“证书”。
我们知道欧盟MDR划分的一类器械和我们国内的划分有些区别。
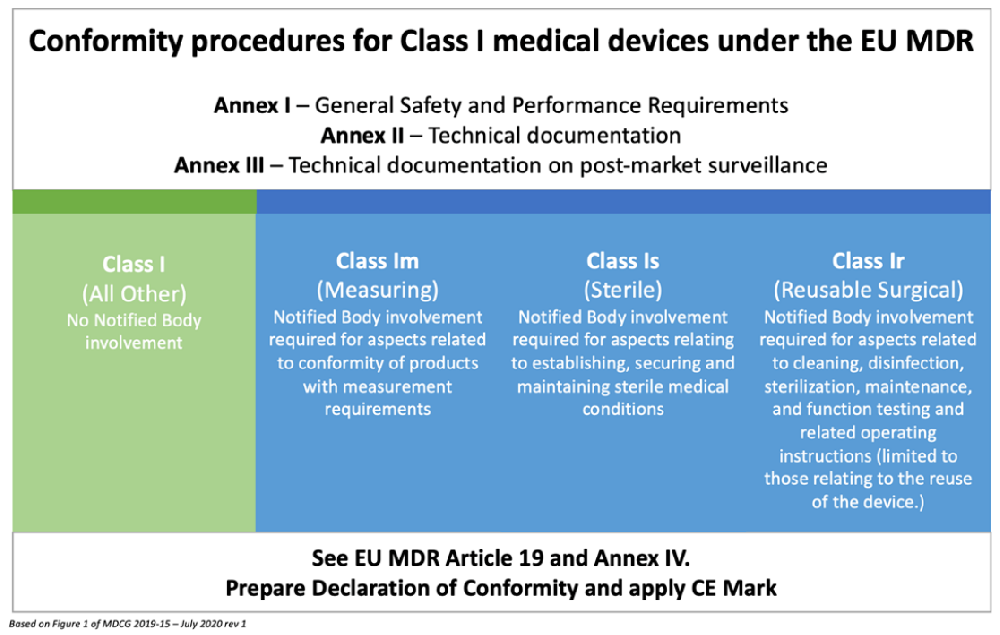
一般I类(自我声明)
Im 类(公告机构对测量方面的审查)
Class Is(公告机构对无菌方面的审查)
IR 类(公告机构对可重复使用方面的审查)
所有 I 类无菌和测量设备,以及可重复使用的手术器械,现在都需要公告机构审查。此外,如果您销售的软件以前是 MDD 下的 I 类设备,请阅读 MDR 的规则 11,因为分类可能已更改。
欧盟MDR 对一类医疗器械符合性评价程序区分:
所有 I 类制造商都必须按照欧盟 MDR 第 VII 章第 85 条的规定制定 PMS 计划和 PMSR。您的 PMSR 需要总结 PMS 数据的结果和结论,以及对市场上产品采取的任何纠正措施的基本原理和描述。该报告将成为您的技术文档(技术文件的新名称)的一部分,并在必要时进行更新,并根据要求提供给欧盟主管当局。您的 PMSR 应在设备的整个生命周期内进行维护。
MDR附件II要求所有医疗器械制造商拥有足够的技术文件。这包括有关器械的非常详细的信息、器械的上一代和类似产品、器械的完整标签集、设计和制造信息、一般安全和性能要求、效益风险分析和风险管理信息、产品验证和确认数据、临床数据等,所以根据法规,哪怕是自我申明的器械一套完整的技术文件也是必须建立的。
如果您制造的 I 类设备是无菌的或具有测量功能的,您可能已经拥有符合 MDD 的技术文件。但是,您的旧技术文件不一定满足 MDR 第六章和 MEDDEV 2.7/1 rev. 4 的严格新要求。尤其是测量类的,可能需要提供关于准确度的临床验证资料(也就是我们经常说的小临床试验)。
无论您的情况如何,我们都建议您从 MEDDEV 的第 7 节(第 15-17 页)开始,因为它讨论了所需临床评估的范围。很多人都对黄老师的建议嗤之以鼻,但公告机构不会关心您的设备是否已经安全销售了 25 年——他只需要你收集临床证据来证明您的设备是安全的。
如果您的公司生产 I 类无菌或测量设备,您可能已经拥有质量管理体系。如果您尚未导入 ISO 13485:2016质量体系,您可能需要考虑开始着手这样做了。虽然MDR没有明确要求获得质量管理体系(QMS)认证,但遵守第10条中QMS要求的最简单方法是获得ISO 13485:2016认证。虽然市场上有很多认证机构都宣称可以核发ISO 13485:2016认证,但是您一定要问清楚发的证书是不是带标的。如果您最终要谋求MDR的欧盟申请,ISO 13485:2016认证最好还是找SGS、TUV这样的欧盟机构去做。即使是自我申明的 I 类设备制造商也需要实施基本的 QMS,其中包括内审、管理评审、纠正措施、警戒、PMS 等程序。
所有在欧盟以外的器械制造商如果要在欧盟销售产品,都必须指定一个欧盟授权代表。他的作用主要就是为您在欧盟境内保管您的符合性声明、技术文件,负责和CA等监管机构的沟通。所以回到前面的话题,虽然一类普通器械不需要公告机构的介入。但是您的完整的技术文件是必须由您的欧盟代表保存随时接收主管机构的检查的。如果没有这些资料,您将面临非常大的法律风险。作为您的欧盟授权代表,在您的产品出现质量问题时,也是监管机构第一个要找的对象,所以很多制造商上觉得欧盟授权代表收取您5年壹万五六千的代表费很贵。其实考虑到他们需要承担的法律风险,这些费用其实是非常的低的。
最后,根据MDR,所有制造商最终被要求在新的EUDAMED在线数据库中注册其公司和设备。您的 SRN 将出现在您的产品标签、说明书、未来的证书和您的符合性声明中。
二、欧盟医疗器械质量体系与生产监督介绍
三、医疗器械的相关法规文件
1、有源植入医疗器械指令 (EC-Directive 90/385/EEC)。该指令适用于心脏起搏器、可植入的胰岛素泵等有源植入医疗器械,于1993年1月1日生效,1995年1月1日强制实施。
2、医疗器械指令 (EC-Directive 93/42/EEC)。该指令适用于除90/385 EEC指令和98/79 EEC指令规定以外的一般医疗器械,于1995年1月1日生效,并于1998年6月14日强制实施。
3、体外诊断医疗器械指令 (EC-Directive 98/79/EEC)。该指令适用于血细胞计数器、妊娠检测装置等体外诊断用医疗器械,于1998年12月7日生效,2003年12月7日强制实施。
医疗器械指令 (EC-Directive 93/42/EEC)由23项条款和12个附录组成,其主要内容为:
1、定义和范围 (Definitions,scope)
2、上市与投入使用 (Placing on the market and putting into service)
该条款中规定制造商需采取所有必要的措施,确保医疗器械在依照设计的目的安装、维护和使用时不会危及患者、使用者或相关人员的安全及健康。
3、基本要求 (Essential requirements)
该条款中规定医疗器械必须符合指令附录Ⅰ中的基本要求。
4、医疗器械的自由流通和特殊用途的医疗器械 (Free movement,devices intended for special purposes)
该条款中规定各成员国不能对符合指令规定的临床研究用器械、定制器械和带有CE标记的医疗器械产品设置流通障碍。同时规定定制器械、参展器械和临床研究用器械在使用时可无需带有CE标记。
5、可参考的标准 (Reference to standards)
6、标准与技术法规委员会 (Committee on Standards and Technical Regulations)
该条款规定依据83/189/EEC号指令第五条所设立的委员会应协助欧盟委员会工作。
7、医疗器械委员会 (Committee on Medical Devices)
该条款规定依据90/385/EEC号指令第六条第二项所设立的委员会应协助欧盟委员会工作。
8、保护条款 (Safeguard clause)
该条款中规定了成员国对被发现不符合指令要求的医疗器械产品的处理措施。旨在最大限度保护患者、使用者及相关人员的安全与健康。
9、分类 (Classification)
该条款中规定医疗器械划分为四类,具体分类标准参考附录Ⅸ中内容。该条款同时规定,当制造商与公告机构在管理类别上发生分歧时,由公告机构所属成员国的主管当局裁决。
10、医疗器械上市后不良事件的通报 (Information on incidents occurring following placing of devices on the market)
11、符合性评估程序 (Conformity assessment procedures)
12、对已有CE标记的医疗器械产品进行组合、包装、灭菌的特殊规定 (Particular procedure for systems and procedure packs and procedure for sterilisation)
13、医疗器械分类问题的处理措施 (Decisions with regard to classification and derogation clause)
14、上市医疗器械相关责任人的注册 (Registration of persons responsible for placing devices on the market)
15、临床研究 (Clinical investigation)
该条款中规定制造商在进行临床研究前,应将临床研究内容通知临床研究工作所在成员国的主管机构。经主管机构批准后方可实施。
16、公告机构 (Notified bodies)
17、CE标记 (CE marking)
该条款中规定,除定制器械和临床研究用器械外,符合该指令第三项条款规定基本要求的医疗器械在上市时必须带有CE标记。
18、不当使用CE标记的处理措施 (Wrongly affixed CE marking)
19、关于拒绝和限制某医疗器械上市、使用或临床研究的处理措施 (Decision in respect of refusal or restriction)
20、保密责任 (Confidentiality)
21、其他相关指令的修订与废止 (Repeal and amendment of Directives)
22.实施及过渡性条款 (Implementation,transitional provisions)
23、“本指令通知所有会员国”。
附录Ⅰ、基本要求
附录Ⅱ~附录Ⅶ为不同的符合性评估程序
附录Ⅷ、关于特殊用途器械的声明 (Statement concerning devices for special purposes)
该附录中规定了生产者对用于临床研究和定制器械所出具的声明中所需的必要信息。
附录Ⅸ、分类标准 (Classification criteria)
附录Ⅹ、临床评估 (Clinical evaluation)
附录Ⅺ、公告机构的相关规定 (Criteria to be met for the designation of notified bodies)
附录Ⅻ、EC标志的格式 (CE marking of conformity)
四、欧盟医疗器械指令中涉及的机构
欧盟已颁布的三个医疗器械指令中涉及的机构有:
欧盟委员会 (European Commission)
欧盟标准委员会 (CEN / CENELEC)
主管当局 (Competent Authorities)
公告机构 (Notified Bodies)
医疗器械制造商 (Manufacturers)
五、欧盟医疗器械指令中部分定义
1、医疗器械(medical device):
对疾病的诊断、预防、监护、治疗或缓解;
对损伤或残疾的诊断、监护、治疗、缓解或补偿;
对解剖或生理过程的研究、替代或纠正;
妊娠控制;
2、体外诊断医疗器械(in vitro diagnostic medical device):
是指任何医疗器械, 包括试剂、试剂成分、校准物品、对照材料、试验工具、仪器、设备、器具或系统, 不论是单独使用还是组合使用,对从人体内提取的样本(包括捐献的血液和组织)在体外进行检查,以提供下列信息为唯一或主要目的:
- 生理或病理状态;
- 先天畸形状况;
- 确定安全性和与受体的相容性;
- 监测治疗措施.
样本的容器也被认为是体外诊断医疗器械。
3、有源医疗器械(active medical device):
是指依靠电能或其他能源,而不是直接由人体或重力产生的能源发挥功能的任何医疗器械。
4、有源植入医疗器械(active implantable medical device)
是指预期通过外科或医疗手段全部或部分介入人体或通过医疗手段进入人体自然孔道,并在操作后仍保留在人体的任何有源医疗器械。
5、定制器械(custom-made device):
根据医生或其他专业人士的书面要求, 为某一特定患者而制造的任何器械。
6、制造商(manufacturer):
指在以其名义将医疗器械投放市场前负责医疗器械的设计、制造、包装和标签的自然人或法人,无论这些工作是他自己完成的,还是他委托第三方完成
六、欧盟对医疗器械管理类别的划分
1、93/42/EEC指令适用的医疗器械的分类
Ⅰ类医疗器械:普通医用检查手套、病床、绷带;
特殊I类医疗器械:灭菌检查用手套、创口贴、、血压计;
Ⅱa类医疗器械:手术用手套、B超、输液器;
Ⅱb类医疗器械:缝合线、接骨螺钉;
III类医疗器械:冠状动脉支架、心脏瓣膜。
2、体外诊断医疗器械的分类
附录Ⅱ清单A中所列器械:包括血型检测用器械,艾滋病及乙型肝炎病毒检测用器械等;
附录Ⅱ清单B中所列器械:包括风疹、弓形虫检测用器械、血糖仪、肿瘤标记物等;
自我测试用体外诊断器械:早孕试纸等;
其他体外诊断器械。
七、上市前的评估程序
该附录描述了一个质量体系,该体系通过产品的最终检验和试验以确保生产的器械符合已经过EC型式检测的型号,或技术文件中规定的器械。该程序适用于IIa和IIb 类器械。该程序不适用于无菌医疗器械。
6、附录VII EC符合性声明 (EC DECLARATION OF CONFORMITY)
该附录中规定制造商出具符合性声明确认其医疗器械产品符合医疗器械指令的要求,并描述用于支持符合性声明的必需的技术文件。该符合性声明无需公告机构审查。该附录适用于 I和IIa 类器械。
不同管理类别医疗器械有不同的评估程序,具体如下:
附录Ⅶ EC符合性声明
附录Ⅶ EC符合性声明 + 附录Ⅴ 生产质量保证;
附录Ⅶ EC符合性声明 + 附录Ⅵ 产品质量保证;
附录Ⅶ EC符合性声明 + 附录Ⅳ EC确认。
3、Ⅱa类医疗器械
附录II 全面质量保证体系(不包括设计审查);
附录Ⅶ EC符合性声明 + 附录Ⅴ 生产质量保证;
附录Ⅶ EC符合性声明 + 附录Ⅵ 产品质量保证;
附录Ⅶ EC符合性声明 + 附录Ⅳ EC确认
附录II 全面质量保证体系(不包括设计审查);
附录Ⅲ EC型式检测+ 附录Ⅴ 生产质量保证;
附录Ⅲ EC型式检测+ 附录Ⅵ 产品质量保证;
附录Ⅲ EC型式检测+ 附录Ⅳ EC确认。
5、Ⅲ类医疗器械
附录II 全面质量保证体系 + 设计审查
关于体外诊断器械的评估程序有:
1、附录Ⅱ清单A中器械:
附录Ⅴ EC型式检测 +附录Ⅶ 生产质量保证;
附录Ⅳ 全面质量保证体系 + 设计审查;
2、附录Ⅱ清单B中器械:
附录Ⅴ EC型式检测 +附录Ⅶ 生产质量保证;
附录Ⅴ EC型式检测 +附录Ⅵ EC确认;
附录Ⅳ 全面质量保证体系;
3、自我测试类器械:
附录Ⅲ EC符合性声明 +附录Ⅲ.6 设计审查;
附录Ⅴ EC型式检测 +附录Ⅶ 生产质量保证;
附录Ⅴ EC型式检测 +附录Ⅵ EC确认;
附录Ⅳ 全面质量保证体系;
附录Ⅲ EC符合性声明(不包括设计审查)。
八、欧盟医疗器械指令的基本要求及协调标准
八条特殊要求涉及的方面包括:
化学、物理学和生物学特性;
传染和微生物污染;
结构和环境特性;
具有测量功能的器械;
辐射防护;
对连接或装配能源的医疗器械的要求;
制造商提供的信息;
临床资料。
九、对上市后医疗器械的监督和保护措施
医疗器械指令 (EC-Directive 93/42/EEC)在第十项条款中规定:
成员国负责记录和处理上市后的不良事件。
医务人员或医疗机构应及时报告不良事件,同时通知制造商或其欧洲代表。
对事件分析后, 成员国应确定是否启用保护条款。
医疗器械指令中还制订了相应的保护性条款:
医疗器械指令 (EC-Directive 93/42/EEC)在第八项条款中规定:
1、当成员国发现已上市或投入适用的医疗器械存在不符合基本要求、使用协调标准不当或标准本身不完善的情况,并在依照设计的目的安装、维护和适用时危及患者、使用者或相关人员的安全及健康时,应将欧盟委员会报告原因及处理措施。
2、欧盟委员会应尽快听取被处理方意见, 然后做出决定:
如认为处理适当,则立即通知各成员国。
如处理不当,则立即通知处理决定国和受处理者。
如认为是属于标准问题,则提交标准和技术法规委员会处理。
3、对于不符合规定的带有CE标志的医疗器械,各成员国应采取措施制止,并通报欧盟委员会和其他各成员国。
十、公告机构简介
十一、临床研究
十二、欧盟医疗器械监管模式的特点
1、按风险高低划分产品的管理类别
2、管理灵活,法规适用性强
3、上市前评估程序多样
4、分权管理