一类医疗器械欧盟CE认证注册
一、I类医疗器械的CE认证步骤:
1.分类:确认产品属于I类医疗器械
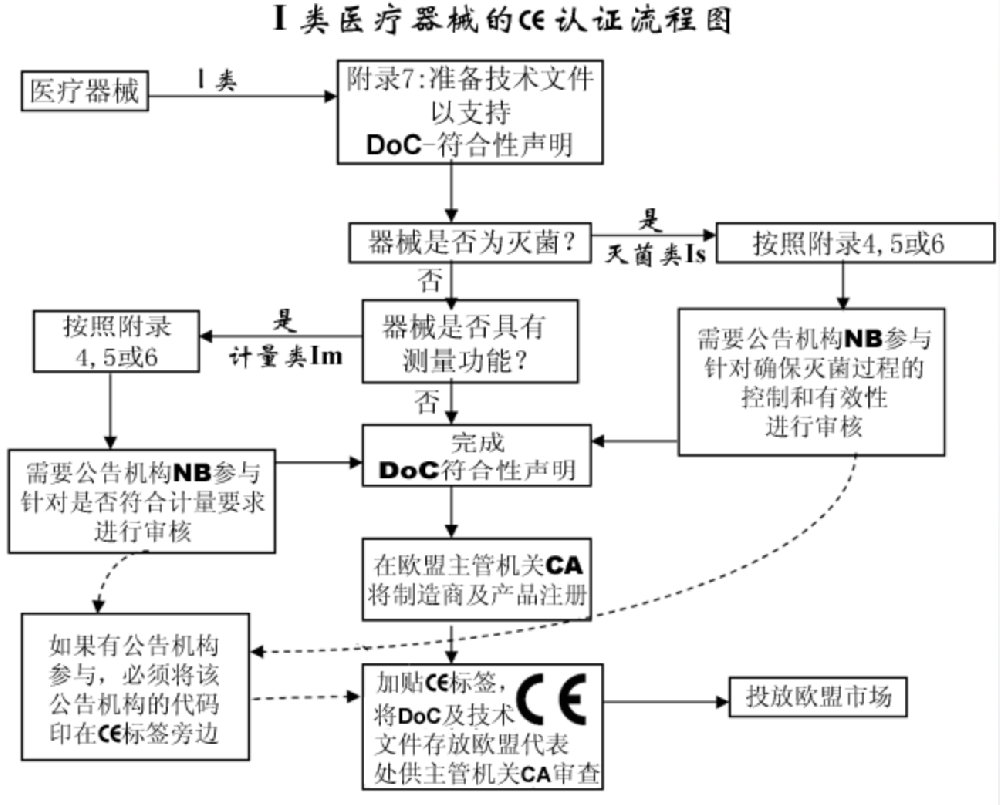
2.选择符合性评估途径: 请参考下面的流程图
3.编制技术文件
4.CE符合性声明
5.委任欧盟授权代表
6.由欧盟授权代表将制造商及产品在欧盟主管机关注册7.建立售后警戒系统/加贴CE标签并将产品投放市场
二、I类医疗器械: CE 符合性评估途径:
1.制造商有责任确保其产品符合MDR指令的所有相关的基本要求,必须制定一份书面(自我) 声明来保证
2.不具备测量功能或非灭菌的I类医疗器械(的CE认证过程中)不需要第三方公告机构(NB)参与。是否符合ISO13485:2016标准,由制造商自愿选择,并非强制性。
3.具有测量功能或灭菌类的I类医疗器械(的CE认证过程中) 必须要有第三方公告机构(NB)参与。
4.一旦制造商认为其立品符合MDR指令的所有相关的基本要求, (欧盟境内的)制造商,或者 (欧盟境外制造商的)欧盟授权代表必须先在欧盟主管机关注册,然后才可加贴CE标签并将产品投放EEA市场。