在2000年日本引入第三方认证制度之前,任何医疗器械的生产和上市都必须经过厚生劳动省(MHLW)的质量、有效性和安全性审查和评估,并由厚生劳动省从公众健康的角度进行批准。因此在引入第三方认证制度前的日本欧洲和美国相比,在日本上市和销售医疗器械往往需要更长的时间。
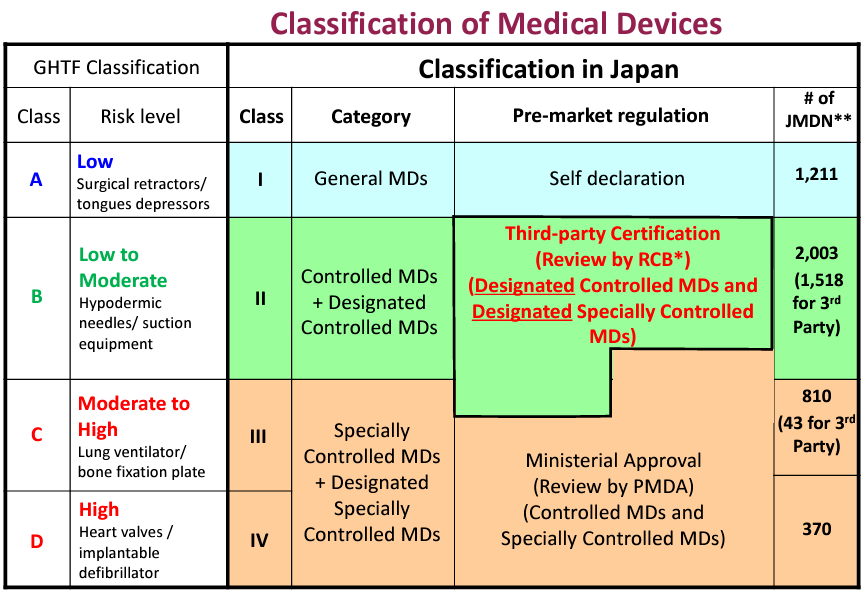
从确保国际协调的角度来看,日本官方认为有必要根据医疗器械或体外诊断器械的特点进一步完善安全措施。于是,引入第三方认证制度的需求迫在眉睫。以下是日本官方针对医疗器械质量、有效性和安全性审查和评估做出的部分变化:- 根据全球协调医疗设备工作组(GHTF)的分类规则,引入医疗设备风险分类系统。
- 对低风险医疗器械和体外诊断引入第三方认证制度,以取代厚生劳动省MHLW的审批制度。
- 审查过程不仅包括以文件为基础的质量、功效和安全性检查,必要时还包括制造现场检查。
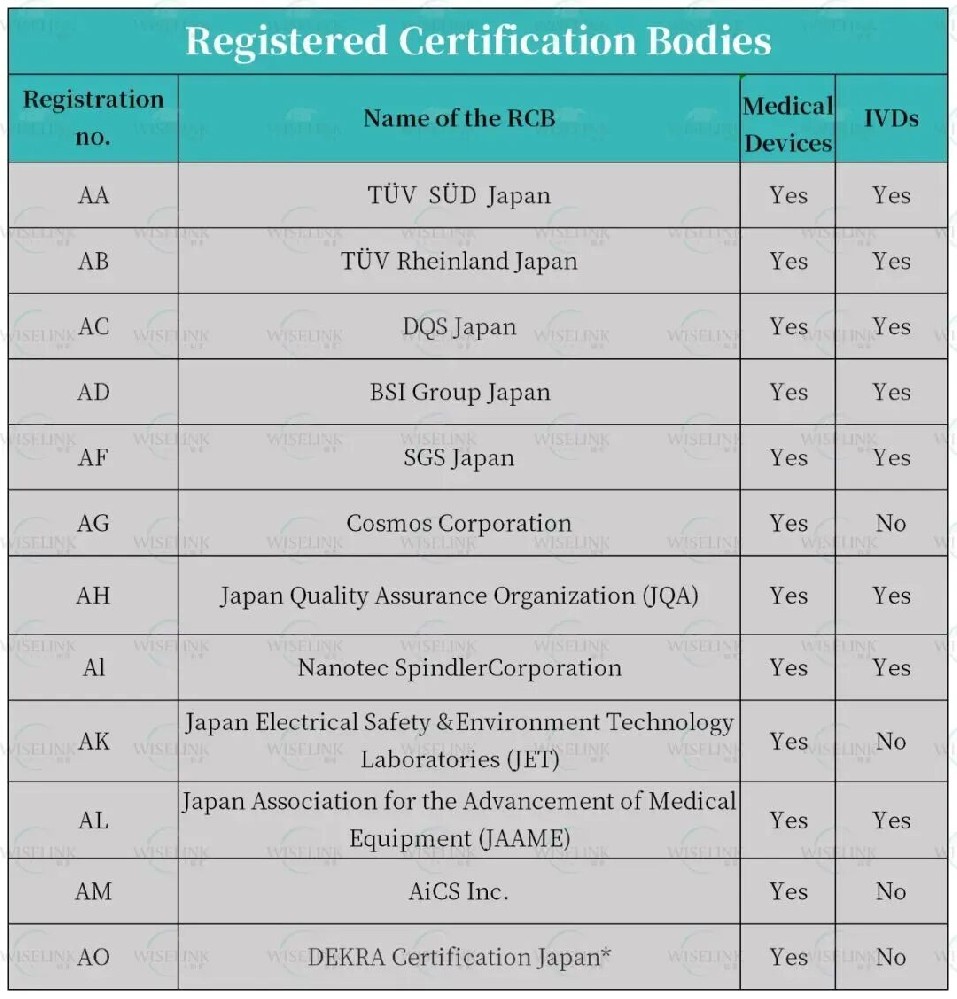
本篇文章,知汇将为您介绍符合日本ISO13485和医疗器械认证要求的第三方机构清单以及RCB机构审核的相关知识。
符合日本ISO13485质量体系认证要求机构清单链接:https://webgate.ec.europa.eu/single-market-compliance-space/notified-bodies/free-search二、日本不同分类 MD & IVD 对应的监管要求
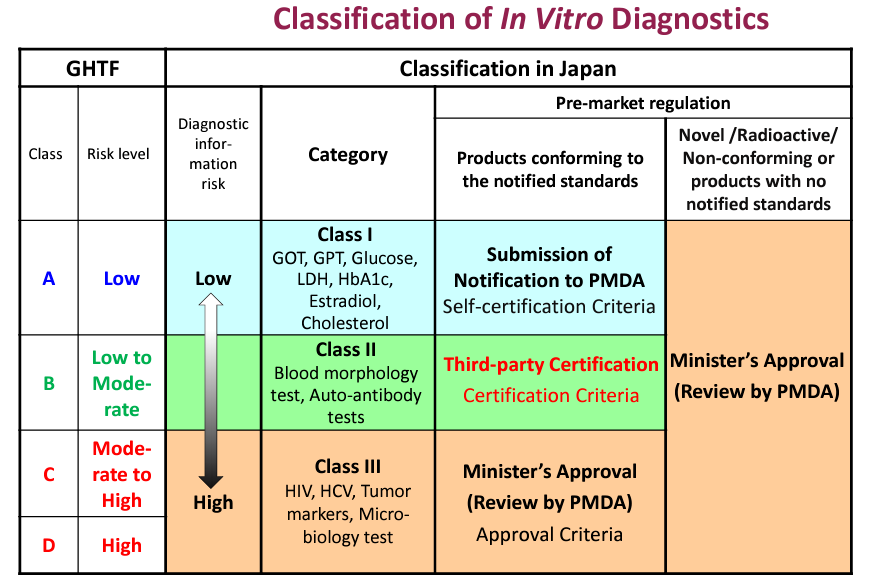
I类:General MDs——Self declaration(自我声明)II类:Controlled MDs+ Designated Controlled MDs——Third-party Certification(Review by RCB*:由RCB机构审查)III & IV类:Specially Controlled MDs+ Designated Specially Controlled MDs——Ministerial Approval(Review by PMDA:由PMDA当局审查)注意,部分 II类医疗器械和 III&IV类医疗器械审查方式有所不同,如果您想确认您的医疗器械属于哪一种监管要求,欢迎咨询Wiselink知汇。- 参考 IVD 器械类别:GOT, GPT, Glucose(葡萄糖), LDH, HbA1C, Estradiol(雌二醇), Cholesterol(胆固醇)
- 上市前监管:Submission of Notification to PMDA(Self-certification Criteria 自我认证标准)
- 参考IVD器械类别:Blood morphologytest(血液形态检测), Auto-antibodytests(自身抗体检测)
- 上市前监管:Third-party Certification(certification Criteria 认证标准)
- 参考IVD器械类别:HIV, HCV, Tumormarkers(肿瘤标志物), Micro-biology test(微生物学检测)
- 上市前监管:Minister's Approval (Review by PMDA)(Approval Criteria 审批标准)
如果您想确认您的IVD器械属于哪类上市前监管要求,欢迎咨询Wiselink知汇。
大多数II类医疗器械和体外诊断器械在上市前都需要经过注册认证机构(RCB)的认证,这意味着制造商的产品无需经过 PMDA 的审查和厚生劳动省(MHLW)的批准即可获得认证。
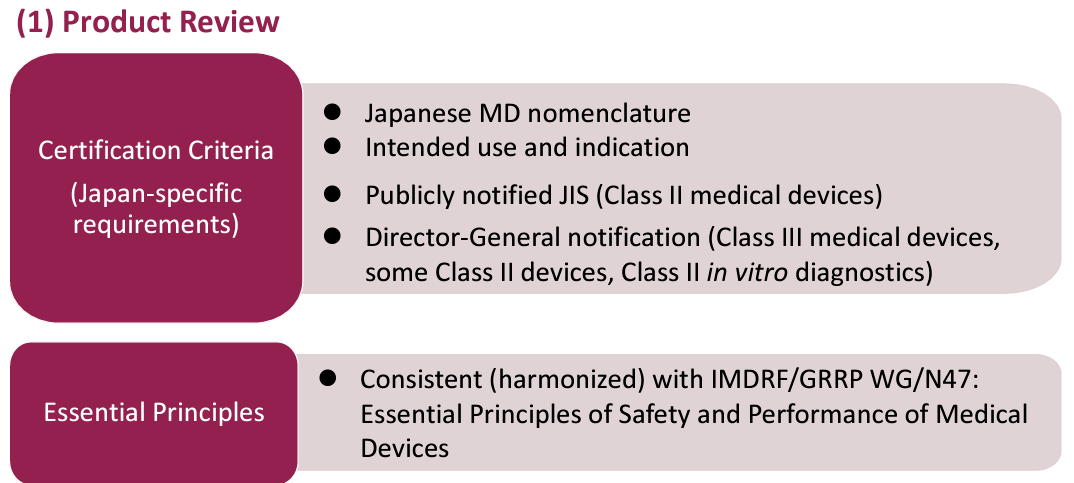
四、医疗器械 MD & IVD 审查的认证标准和基本原则
(一)认证标准(日本特定要求)
- 总干事通知( III 类医疗器械、部分第 II 类器械、第 II 类体外诊断器械)
与 IMDRF/GRRP WG/N47 一致(协调):医疗器械安全和性能基本原则
- 质量管理体系检查根据与 ISO 13485 一致的质量管理体系要求进行。
Wiselink Japan 株式会社是 Wiselink Group 的全资日本子公司,拥有日本医疗器械、化妆品的进口、经销资质,可以作为制造商在日本的当地代表,也可提供日本公司注册、申请经营资质、技术负责人、质量负责人等服务。如果您有相关需求,欢迎咨询Wiselink知汇!