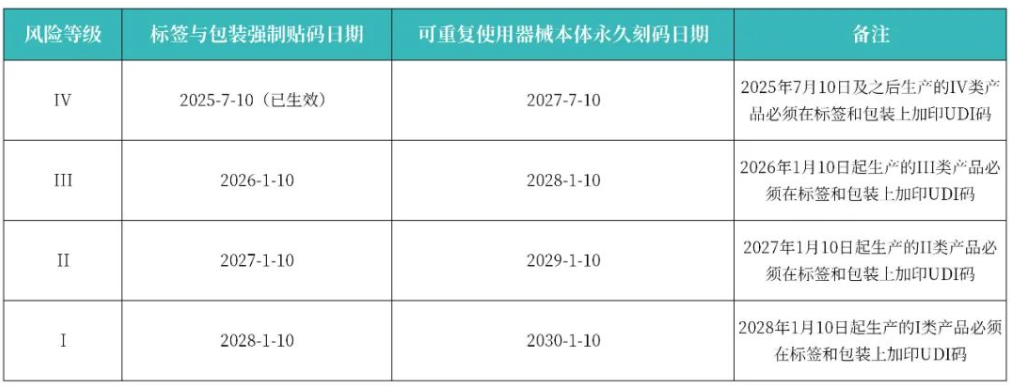
背景:巴西国家卫生监督局(Anvisa)于2021年12月21日发布了第591号决议(RDC 591/2021),正式引入医疗器械唯一标识(UDI)体系。这一举措旨在通过为医疗器械分配全球唯一的标识码,实现从生产到使用环节的全程追溯,从而提高患者安全性。该体系遵循国际医疗器械监管机构论坛(IMDRF)的规则,确保与全球标准接轨。 2025年7月10日是一个关键节点,标志着巴西UDI系统正式进入实施阶段。从这一天起,所有风险等级为IV类(最高风险)的医疗器械,如果是在2025年7月10日及之后生产的,必须在标签和包装上加印UDI码。这一要求不仅适用于巴西本土生产的医疗器械,也适用于所有出口到巴西的医疗器械。因此,对于国内医疗器械制造商来说,这是一个必须遵守的硬性规定,直接影响到产品能否顺利进入巴西市场。 特别提示: 高风险产品提前执行:冠状动脉支架、药物涂层支架、髋关节和膝关节植入物自2020年6月20日起已提前执行UDI要求。 豁免情况:运输外箱(如海运集装箱)无需加贴UDI码,但产品本身的标签和包装必须符合要求。 (一)核心概念 1. UDI-DI(设备标识符):每个型号的医疗器械的唯一代码,用于访问 UDI 数据库中的信息。 2. UDI-PI(生产标识符):用于识别单件产品的生产信息,如序列号、批号、生产日期、有效期或软件版本号(对于软件作为医疗器械,即 SaMD)。 (二)操作流程 1. 确认产品风险等级:根据 Anvisa 的分类规则(RDC 185/2001),确认产品所属的风险等级。 2. 选择发码机构:选择 GS1、HIBCC 或 ICCBBA 等国际认可的发码机构,获取 UDI-DI。 3. 生成 UDI 码: UDI-DI:为每个型号生成一个唯一的 UDI-DI。 UDI-PI:根据生产批次或单件产品生成 UDI-PI。 4. 设计标签: AIDC(自动识别和数据捕获):支持一维条形码、二维码(如 QR 码)或 RFID。 HRI(人工可读文本):UDI 码的文本形式,需清晰可读,无需强制换行。 标签布局:AIDC 和 HRI 必须同时出现在标签上,若标签上有多个 AIDC 码(如同时有条形码和二维码),必须标注 UDI 符号。 标签示例: 5. 建立 SIUD 数据表:根据 RDC 591/2021 附件 I 的要求,准备上传至 SIUD 的数据。 6. 上传数据至 SIUD:待 Anvisa 发布相关指令(IN)后,按照规定的时间表上传数据。 7. 内部培训:对质量、物流、法规等部门进行 UDI 相关培训,确保 SOP(标准操作程序)更新。 8. 上市后维护:在产品版本更新、标签改版或灭菌工艺调整时,及时更新 SIUD 中的信息。 (一)系统状态 开发完成:SIUD 系统已于 2025 年 5 月 30 日开发完成,并于 2025 年 6 月 30 日进行了公开展示。 上线时间:系统正式运行需等待 Anvisa 发布相关指令(IN),预计不早于 2025 年 9 月。 等待开放:目前无法在 Anvisa 官网验证 UDI 码或查询产品信息,需等待 SIUD 开放。 (二)数据字段 核心字段:UDI-DI、商品名、型号、制造商、分类、GMDN 代码、灭菌方式、存储条件、IFU 链接等。 数据模板:Anvisa 提供了详细的 CSV/XSD 模板,企业需按照模板准备数据。企业向SIUD上传UDI数据的强制时间表将在IN生效后启动。 1. 立即核查产品风险等级 确认出口巴西的医疗器械是否属于 IV 类(最高风险等级)。根据新规,自 2025 年 7 月 10 日起,所有 IV 类医疗器械必须在标签和包装上加印 UDI 码。制造商应立即梳理产品清单,确定受影响的产品型号,并统计 2025 年 7 月 10 日及之后的生产计划。 2. 生成合规 UDI 码 联系国际认可的发码机构(如 GS1、HIBCC 或 ICCBBA)获取 UDI-DI(设备标识符)和 UDI-PI(生产标识符)。确保 UDI 码符合国际医疗器械监管机构论坛(IMDRF)的标准。 3. 设计更新标签模板(详细要求见上文) 4. 准备 SIUD 数据(详细要求见上文) 5. 关注Anvisa当局政策发布 对于 2025 年 7 月 10 日之前生产的 IV 类医疗器械,库存产品仍可销售,无需立即返工。制造商应合理安排库存,确保过渡期的平稳过渡。 6. 获取官方指南 Anvisa 将发布 UDI 问答、视频教程及线上研讨会,帮助制造商更好地理解和实施新规。制造商应密切关注 Anvisa 官方网站,及时获取最新信息。 7. 上市后维护 变更管理:在产品版本更新、标签改版或灭菌工艺调整时,及时更新 SIUD 中的信息。 留样管理:每批次留样需与 UDI-PI 关联,便于召回追溯。 巴西 UDI 的实施是提升医疗器械追溯与患者安全的关键一步。对于中国出口企业而言,IV 类器械自 2025 年 7 月 10 日起已无缓冲期,必须立即采取行动。企业需迅速调整生产流程和标签设计,避免货物在巴西海关受阻。同时,密切关注 SIUD 法规进展,为数据上报做好准备。 Anvisa 将在未来几个月内加强宣导,建议企业订阅其官方更新以获取最新动态。合规不仅是成本,更是进入巴西市场的门票。知汇希望所有企业都能顺利应对巴西 UDI 的挑战,抓住巴西市场的机遇。 Wiselink拥有包括原澳大利亚药品监督管理局局长Dr. Derrick Beech为首席顾问的国际专业团队,秉承源于澳洲、扎根中国、服务世界的精神,信守专业、真诚、开放的核心价值观,致力于为医疗器械、化妆品、食品、保健品和中药制造商提供全球合规认证和临床试验服务。