

近年来,越来越多医疗器械制造商选择进军泰国市场。在泰国进行医疗器械注册时,制造商通常希望将相似产品归入一个“系列”,以便共用一个注册证。这不仅可以简化监管流程,还大大降低了注册成本与维护难度。 然而,泰国食品药品监督管理局(TFDA)对“系列”注册有明确要求。哪些产品可以被归入一个系列?哪些变体又必须单独注册?本文知汇将为您详细介绍。 根据泰国FDA依据《东盟医疗器械指令(AMDD)》的法规定义,“系列”指的是一组满足以下条件的医疗器械: 由同一制造商生产; 具有相同的预期用途; 具有相同的设计与工作原理; 存在的差异不影响器械的安全性或基本性能。 医疗器械按照“系列”注册具有以下优势: 多型号产品共用一个许可证; 大幅节省注册成本与时间; 后续变更(如包装或颜色)处理更为简便; 有利于产品快速上市。 泰国食品药品监督管理局已发布详细指南,概述了医疗器系列中可接受的差异。以下变体通常是允许的: 需要注意的是,这些差异被接受的前提是不影响安全性、有效性及预期用途,否则将不被允许作为“系列”注册。 若医疗器械产品之间存在以下任一重大差异,则不能归入同一个系列: 改变预期用途; 更改操作原理或核心功能; 使用了不同的材料,影响生物相容性; 更换灭菌方式; 影响风险等级或产品分类; 软件变更导致功能增强或算法变化; 结构设计发生重大调整。 此类产品必须作为独立产品注册,或者若它们以一个功能单元协同工作,可考虑采用“系统注册”方式。 了解泰国医疗器械“系列”注册规则,不仅能帮助制造商加快注册进度、降低运营成本,更有助于在合规框架内进行产品线的灵活扩展与升级。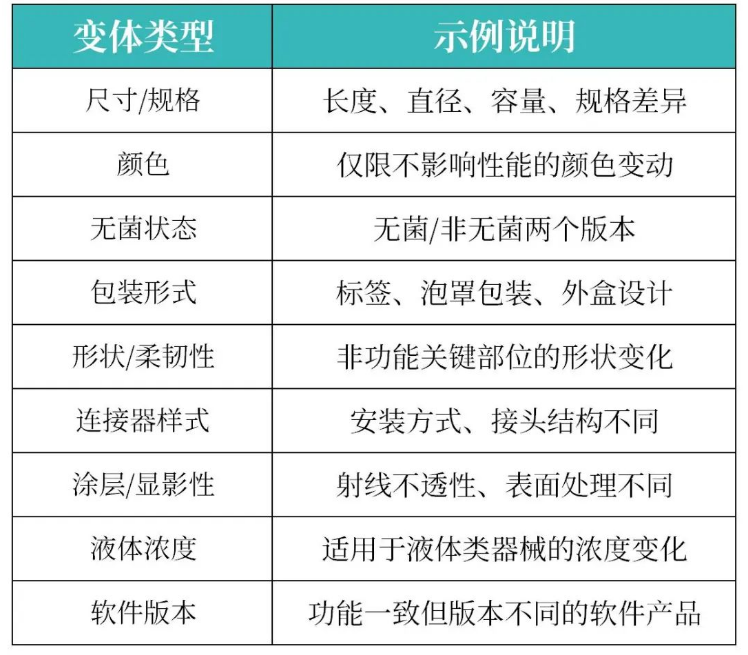
Wiselink拥有包括原澳大利亚药品监督管理局局长Dr. Derrick Beech为首席顾问的国际专业团队,秉承源于澳洲、扎根中国、服务世界的精神,信守专业、真诚、开放的核心价值观,致力于为医疗器械、化妆品、食品、保健品和中药制造商提供全球合规认证和临床试验服务。


