只有CE证书和欧代,医疗器械可以进入意大利市场吗?答案是:不行。通过本篇文章,知汇将为您详细讲解,医疗器械进入意大利市场的相关信息。将医疗器械投放到欧洲市场必须符合欧盟MDR法规(EU)2017/745,虽然该法规适用于欧盟所有成员国,但每个成员国都有自己在国内实施该法规的方式,主要是在该法规中添加法规并制定当地立法。目前意大利是实施这种策略的国家之一,除了要求CE证书和欧代之外,意大利还要求所有进入意大利市场的医疗器械都必须经过医疗器械注册程序。需要注意的是,该程序适用于从低风险到高风险的所有医疗器械类别。以下是意大利医疗器械国家数据库和医疗器械注册的相关信息介绍。

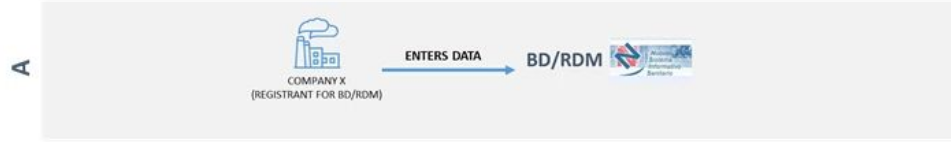
1.数据库(BD/RDM),包括名为“Repertorio”的数据库子集,汇集了以下各方提供的信息:根据第12条第2款开展活动的实体(在《用户手册》医疗器械制造商简介中称为装配商)2.注册人对所提供的信息承担全部责任,包括一般数据和与每个医疗器械(MD)相关的数据。同时数据的公布不构成该部门任何形式的批准。3.根据1997年2月24日第46号法令及其后的修正案,医疗器械和药品服务总局有权随时对申报和注册的医疗器械进行检查。4.在医疗器械数据库中,直接输入数据的实体被视为“注册人”。只有注册者才能更改与其注册的医疗器械有关的信息。系统最初获取的处理状态为“L”的所有信息都必须经过电子签名“验证”才能“公布”。自2014年1月1日起,对处理状态为(“L”)的数据信息进行电子签名验证将有时间限制。系统针对首次录入的数据和更改已有数据有不同的验证时限通知:医疗器械的“首次通知”必须按照现行法律规定的程序完成,在任何情况下都必须在数据输入之日起30日内完成数据的电子签名。超过此期限,如果没有电子签名验证,输入的数据将从BD/RDM系统中删除,包括注册后系统最初分配的渐进编号。医疗器械的“后续通知”由之前输入系统的数据变更引起,必须在“返回处理”之日起7个日历日内通过电子签名完成。超过这一期限,如果没有进行适当的验证,所做的更改将被视为无效,并从系统中删除,而之前的通知在所有效果和目的上仍然有效。如果系统检测到数据库中的通知处于处理状态,则会在相关部分列出:待完成通知(待办事项列表)。除数据库外,医疗设备还可在用户手册医疗设备制造商简介中称为“Repertorio”或“Repertoire”的数据库子集中注册,在“Repertorio”中注册医疗器械不是强制性的。(一)要在BD/RDM中注册医疗器械,必须按照以下两种路径(A和B)访问数据库。直接在BD/RDM中操作的公司被定义为“注册公司”;注册公司可以是以下四种类型:1.第46/97号法令第1条第2款(f)项定义的医疗器械制造商2.第46/97号法令第12条第2款所述的实体(称为装配商)3.第46/97号法令第13条第2款所述由制造商指定的欧盟授权代表
B-通过授权访问医疗器械数据库在BD/RDM中注册器械
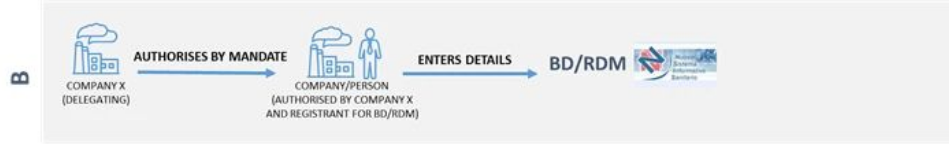
在进行医疗器械注册之前,必须按照上一节“访问BD/RDM”中的说明访问医疗器械数据库。在意大利注册的医疗器械(MD),无论是I类和组装设备的MD,或是IIA类、IIB类、III类和有源植入设备的MD,在数据库中注册都是强制性的。如果您对医疗器械意大利注册有任何疑问或者需求,欢迎咨询Wiselink知汇的专业团队。知汇Wiselink CN拥有包括原澳大利亚药品监督管理局局长Dr. Derrick Beech为首席顾问的国际专业团队,秉承源于澳洲、扎根中国、服务世界的精神,信守专业、真诚、开放的核心价值观,致力于为医疗器械、化妆品、食品、保健品和中药制造商提供全球合规认证和临床试验服务。




