


脉搏血氧仪是一种广泛应用于医疗领域的设备,用于非侵入性地测量动脉血氧饱和度(SpO2)和脉率。然而,近年来的研究表明,脉搏血氧仪的准确性可能受到多种因素的影响,尤其是皮肤色素沉着。
为此,美国食品药品监督管理局(FDA)发布了最新的指南草案。FDA要求在指南草案发布后的60天内对其进行评论。同时FDA将审查和考虑所有意见,然后最终确定本指南,以指导制造商和医疗专业人员更好地使用和评估脉搏血氧仪的性能。本文知汇将为您解读一下指南草案的核心内容。

https://www.fda.gov/media/184896/download
一、指南更新的核心目的 二、新指南与旧指南的主要变化 新指南要求制造商收集更多的临床数据,以评估设备在不同皮肤色素沉着范围内的性能准确性。 临床研究的参与者数量从10人增加到至少150人,以确保样本的多样性和代表性。 引入了主观的Monk Skin Tone Scale和客观的calculation of individual typology angle来评估研究参与者的肤色。 如果设备在新的上市前提交中证明了性能的准确性,需增加显著的标签声明,以帮助用户识别脉搏血氧仪在不同肤色人群中的性能。
三、新指南的适用范围 适用于某些医用脉搏血氧仪,主要用于医院或医生办公室。包括产品代码为DQA、NLF、OLK、QYU和DPZ的血氧仪。(如下图所示) 不适用产品代码为 OCH或PGJ的血氧仪。此外,本指南也不涉及产品代码为 MUD、NMD、QEM或 MMA的血氧仪。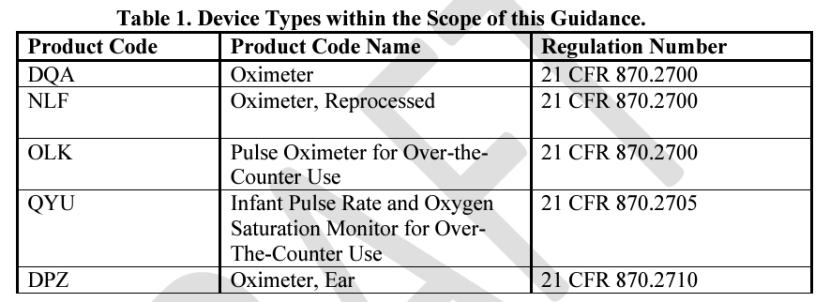

四、新指南关于临床研究的主要变化 受试者数量要求显著增加,至少需要150名参与者,且每个受试者至少提供20对血氧数据,总共至少3000对数据。 对受试者的招募标准更加严格,除了遵循ISO 80601-2-61标准中的入排标准外,还要求通过Monk Skin Tone Scale和比色法对受试者的肤色进行评估,并按MST水平进行分组。 研究要求在不同MST分组和不同血氧饱和度水平(70%至100%)的每个范围内至少有30%的参与者。 对人口统计信息的要求也更为详细,需要包括年龄、性别、BMI和民族等信息。这些变化旨在提高临床研究的代表性和准确性,确保脉搏血氧仪在不同肤色人群中的性能评估更为可靠。(具体要求如下图所示)