



https://www.team-nb.org/wp-content/uploads/2024/12/Team-NB-PositionPaper-MDR-Certification-Process-Consensus-Document-20241218.pdf
一、主要目的和范围:
二、认证流程阶段:
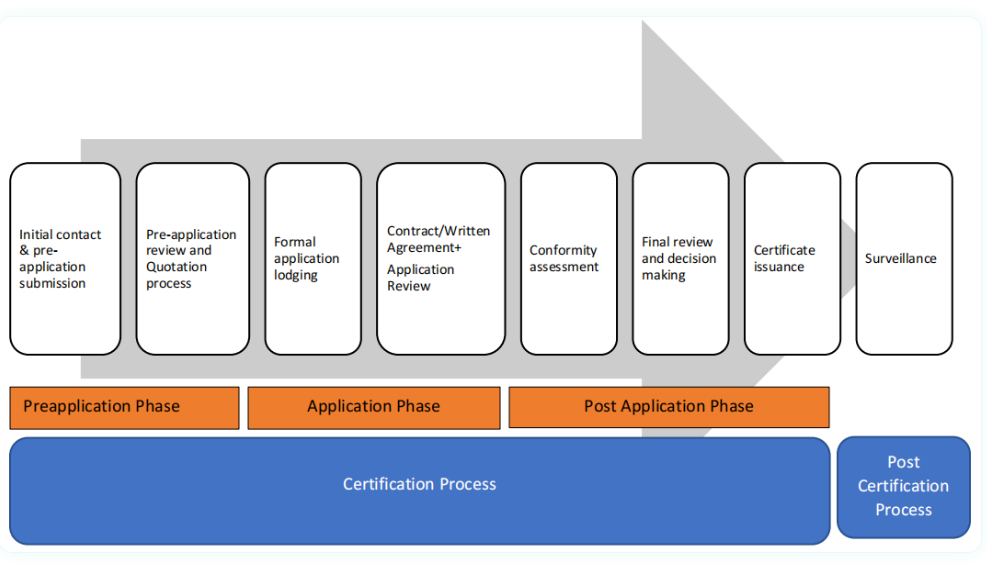
制造商与公告机构NB之间的首次接触,可以是口头或数字形式(如电子邮件、在线表单)。制造商需提交包括产品信息、公司详情等相关信息,以便NB机构进行初步审核并提供符合性评估服务的报价。此阶段,NB将核实产品是否受MDR覆盖,并进行分类。
NB机构将根据制造商提供的信息进行初步审核,确保产品属于MDR范畴并准确分类。基于制造商提供的信息,如工厂、供应商、产品等,NB机构将提供包含成本估算的报价。若预申请信息发生变化或有新信息出现,可能影响原报价,NB机构可能会修改报价。
若制造商对NB机构提供的报价满意,并希望继续申请流程,则可以正式提交申请。此过程需至少提交质量管理体系文件(QMS)、产品技术文档等多项资料。针对个别类型的医疗器械,NB机构可能要求提供完整的技术文档,以验证产品资格、分类及选择的符合性评估程序,并制定评估计划。
申请提交后,NB机构将提供合同文件。双方签署合同后,NB机构将基于制造商提供的文件进行审核申请,包括申请的完整性、产品资格、适用的符合性评估程序等内容的审核,并决定是否接受申请。
接受正式申请后,NB机构将进行审核申请并制定适当的符合性评估活动计划,包括质量管理体系审核、技术文档评估、物理测试、实验室测试等项目。评估活动的选择取决于医疗器械分类和选择的符合性评估程序。NB机构将通知制造商计划进行的符合性评估活动的时间。
完成必要的符合性评估活动后,NB机构将进行最终审核和决策,以决定是否发放证书。这一审核由未参与先前评估的人员执行,确保评估活动报告和支持文件的完整性、以及无未解决的不符合项。审核结果将同时记录在内部参考报告中,作为最终决策依据。
若审核结果通过,NB机构将根据MDR的适用路线生成证书,并将证书发放给制造商,同时提交至EUDAMED系统。
初始认证结束以及证书颁发后,NB将定义必要的监管活动,包括年度QMS审计、PSUR评估、SSCP验证、技术文档评估、监管数据评估和不定期审核等,以确保医疗器械制造商持续符合MDR法规的要求,产品能够顺利进入欧盟市场。
本共识文件未来将继续根据NB机构在MDR法规下获得的进一步经验以及法规的变化、其他相关指导文件(例如MDCG文件)的发展对要求解释的任何变化进行修订。通过这份共识文件,制造商可以获得一个清晰的指导,以便更有效地准备和提交MDR认证申请,确保产品能够持续符合欧盟市场的要求。