

No. 2014-0029号行政命令(《食品经营单位许可和加工食品、其他食品注册及其他目的的规则和条例》)将食品补充剂定义为 "旨在补充膳食的加工食品,带有或含有一种或多种以下膳食成分:维生素、矿物质、草药、氨基酸、草本植物或其他植物、动物、人工或天然膳食物质,以增加每日总摄入量,其数量符合菲律宾最新推荐的能量和营养素摄入量或国际商定的每日最低要求。
它通常以胶囊、片剂、液体、凝胶、粉末或药丸的形式出现,并不代表可用作常规食品或膳食或饮食的唯一项目或药物和药品的替代品"。

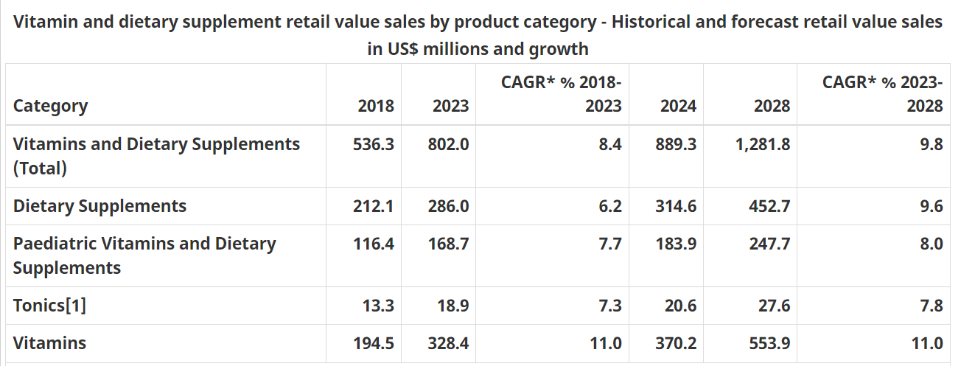
来源:Euromonitor International, 2024
所有加工食品,包括膳食补充剂,都必须在菲律宾FDA当局注册后,方可分销、供应、销售或提供销售及使用,以及进行广告宣传。(第2014-009号行政令第VI节,《加工食品注册准则》)。最初,电子注册仅适用于低风险食品,但 FDA 第 2016-014 号通告已将注册流程扩展至中高风险食品。
一次注册可满足不同包装尺寸的要求,但必须具有相同的品牌和产品名称、相同的配方比例顺序和相同的标签信息。
3.1 原料注册:
特定原材料、添加剂和配料可能需要注册。
3.2 申请人:
制造商和贸易商或分销商(进口商/出口商/批发商)在获得产品注册前,必须获得与其活动有关的经营许可证(LTO)(No. 2014-0029号行政命令第 V 部分和附件)。
3.3 程序:
菲律宾食品与药物管理局将评估适用法规和标准的遵守情况。为此,需要提供以下文件;
①经公证并填写完整的综合申请表;
②缴费证明;
③所有包装尺寸的清晰完整的散装标签或图样,进口膳食补充剂的进口商贴纸;
④所有包装尺寸的产品不同角度的照片;
⑤对于食品补充剂,需提交实际商业展示的实拍图;
⑥证明符合食品法典、国家和其他标准的CoA--物理、化学和微生物分析、成品稳定性数据和安全数据;
⑦宣称功效的证据。
3.4 结果:
①成功注册产品将获得产品注册证书;
②修改产品的标签、包装尺寸、保质期和包装设计必须通知PFDA;
③制造商或再包装商的变更以及成分的改变需要重新注册。
No. 88-Bs. 1984(关于在菲律宾销售的预包装食品标签的规则和条例)对预包装食品的标签进行了规定。然而,2014-0030号行政命令对该行政命令进行了较大程度的修订。
该行政令明确适用于食品补充剂。一般禁止食品标签中的虚假、误导或欺骗性描述。此外,应在标签上用英语和/或菲律宾语注明以下详细信息:
①产品名称;
②品牌名称和/或商标;
③完整的配料表;
④净含量;
⑤允许按体积或数量标注。多件包装应注明总数量和单件数量;
⑥制造商、再包装商、包装商、进口商、贸易商和分销商的名称和地址;
⑦对于进口产品,应提供进口商的完整名称和地址。还必须标明原产国;
⑧批次标识;
⑨储存条件;
⑩有效期;
⑪食品过敏原信息;
⑫使用说明;
⑬营养信息;
⑭产品不是药物的警告声明。
在菲律宾,食品药品管理局(FDA)在确保现有膳食补充剂的安全和质量方面发挥着至关重要的作用。如果您计划引进食品补充剂,则必须从菲律宾食品药品管理局PFDA获得经营许可证(LTO)。以下是流程概述:
5.1 了解 FDA 准则:
在获取膳食补充剂的 LTO 之前,有必要熟悉 PFDA 的指导方针和法规。菲律宾食品和药物管理局网站(www.fda.gov.ph)提供了有关具体要求和程序的详细信息。
5.2 建立合法商业实体:
要申请LTO,您必须在菲律宾有注册的商业实体。确保您的企业符合必要的法律要求,如商业许可证、执照和税务登记。合法经营是获得 PFDA 批准的关键。
5.3 产品注册:
想要成功在PFDA注册您的产品,您必须首先为您的膳食补充剂获得 LTO。这一过程可确保膳食补充剂符合必要的安全和质量标准。为产品注册准备以下文件:
5.3.1 产品信息
完整的产品名称
产品描述
成分和组成
生产工艺
包装细节
功效宣称、建议用法和用量
5.3.2 分析证书(CoA)
从对食品补充剂进行质量分析的符合要求的实验室获取 CoA。CoA 可证明产品的质量、有效性和安全性。
5.3.3 良好生产规范(GMP)认证
获得 GMP 认证,以证明您的生产设施符合 FDA 的良好生产规范指南。
5.3.4 稳定性数据
提供稳定性数据,展示产品在不同储存条件下的质量稳定性和保质期。
5.3.5 标签要求
确保您的产品标签符合 FDA 有关准确产品信息、使用说明、警告和注意事项的规定。
5.4 LTO 申请:
进行LTO申请并成功后,您的产品即可在 PFDA 注册。为申请准备以下文件:
5.4.1 LTO 申请表
从 FDA 网站下载表格,并提供有关您的企业和注册产品的准确信息。
5.4.2 商业文件
提供经营许可证、执照和税务登记的复印件。
5.4.3 GMP 证书
提交生产设施的 GMP 证书。
5.4.3 其他证明文件
根据您的业务性质,可能需要提供其他文件,如所有权证明或生产场地租赁协议。
5.5 提交和处理申请:
向 FDA 办公室提交填写完整的申请和证明文件。支付 FDA 规定的必要费用。FDA 将审查您的申请,如果发现任何不足之处,将通知您予以纠正。
5.6 FDA 检查和合规:
初步审查后,FDA 可能会对您的生产设施进行检查,以确保符合 GMP 标准。请做好相应准备,并及时处理任何不合规问题。
5.7 批准和 LTO 签发:
如果您的申请符合所有要求并通过检查,FDA 将签发 LTO。LTO 的有效期通常为三年。确保在到期前更新,以便继续合法经营。
从菲律宾 FDA 获得食品补充剂的 LTO 是确保产品安全和质量的关键一步,您可以通过了解和遵守 PFDA 的指导方针、注册产品和准备必要的文件,成功地完成这一过程。遵守法规和保持高质量标准将使您的企业受益,并向消费者保证您的食品补充剂的安全性和有效性。
Wiselink拥有包括原澳大利亚药品监督管理局局长Dr. Derrick Beech为首席顾问的国际专业团队,秉承源于澳洲、扎根中国、服务世界的精神,信守专业、真诚、开放的核心价值观,致力于为医疗器械、化妆品、食品、保健品和中药制造商提供全球合规认证和临床试验服务。