

鉴于近期众多客户向知汇咨询关于加拿大医疗器械合规认证的问题,知汇特此准备了一篇专题文章,旨在全面解析加拿大医疗器械认证,以便广大客户更好地理解与掌握。知汇将从以下几点为您逐一介绍。

一. 加拿大医疗器械市场分析
加拿大的医疗器械市场(不包括体外诊断)在2023年的估计价值为92亿美元,约占全球市场的1.8%。2023年,加拿大医疗器械市场的主要领域是:
1. 诊断成像 (21%)
2. 消耗品(15%)
3. 病人辅助工具(16%)
4. 骨科和假肢(10%)
5. 牙科产品(8%)
6. 其他,包括轮椅、眼科仪器、麻醉仪器、透析仪器、血压计、内窥镜仪器、医院家具(30%)
二. 加拿大医疗器械监管机构及法规要求
1. 监管机构:加拿大卫生部(Health Canada,简称 HC)负责帮助加拿大人维持和改善健康,确保提供高质量的医疗服务,并致力于减少健康风险。
2. 法规要求:Medical Devices Regulations(SOR/98-282)。
三. 加拿大医疗器械定义及分类规则
1. 定义
医疗器械是指用于治疗诊断,或预防疾病,或异常身体状况的任何仪器或部件。注意,医疗器械不包括用于动物或兽医目的的医疗器械。
2. 分类
(1)分类规则
加拿大医疗器械分类规则与欧盟医疗器械法规2017/745非常相似,采用法规条款式的分类方法,非目录式。在加拿大,医疗器械根据其使用的相关风险被分为四类,I类器械具有最低的潜在风险(如压舌板) ,IV类器械具有最大的潜在风险(如心脏起搏器) 。II、III和IV类医疗器械必须持有医疗器械许可证才能在加拿大销售。
(2)分类例举
Class I: 绷带、拐杖、手动牙刷
Class II: 电动牙刷、助听器、体温计
Class III: 髋关节植入物、呼吸机
Class IV: 人工心脏,心脏起搏器
如果您对您的医疗器械在加拿大的风险等级分类有疑问,欢迎咨询Wiselink知汇,以便获取准确的风险等级,选择最佳的注册路径。
四. 加拿大医疗器械许可证
加拿大卫生部为医疗器械颁发两种不同类型的许可证:
1. 医疗器械许可证(MDL)——发给制造商的许可证,授权他们在加拿大进口或销售其II、III或IV类医疗器械。
2. 医疗器械设立许可证(MDEL)——向I类制造商以及所有器械类别的进口商或分销商颁发的许可证,允许他们在加拿大进口或分销医疗器械。
需要注意的是,MDL申请是针对医疗器械本身的,而MDEL是针对分销商/进口商或I类医疗器械制造商的许可。MDEL是由加拿大卫生部监管行动和执行处(ROEB)颁发的,基于证明该机构符合加拿大卫生部所有的MDEL监管要求。在加拿大卫生部的检查中,MDEL持有者必须向加拿大卫生部证明他们符合他们所证明的与他们在加拿大制造、进口或分销(销售)的医疗器械有关的监管要求。
生产商必须申请并维护MDEL,以确保符合《食品和药品法》及其《医疗器械条例》。要维护MDEL,必须执行以下操作:
1. 每年4月1日前提交年度许可证审查申请。
2. 如果《医疗器械条例》第45(a)和(b)段中的信息发生变化,则在15个日历日内通知加拿大卫生部。
3. 医疗器械租赁属于“销售”的定义(见《食品和药品法》第2节)。如果您租赁或租赁医疗器械,您必须遵守《医疗器械条例》的要求,包括第44节规定的持有MDEL的要求。
五. 加拿大医疗器械注册流程
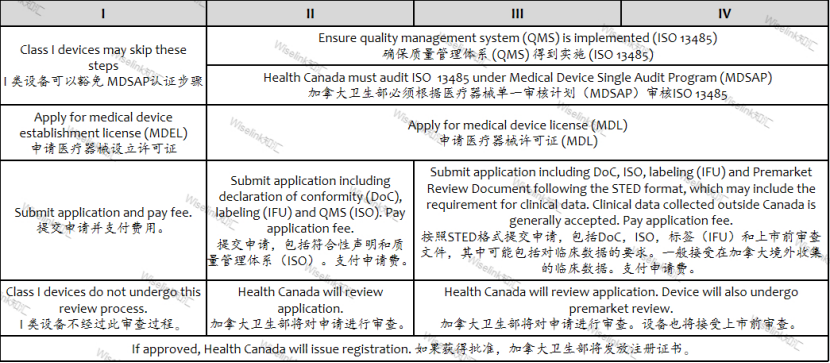
六. 加拿大医疗器械申请所需资料
1. 产品名称(和标签上保持一致)
2. 制造商信息(和标签上保持一致)
3. 注册负责联系人信息
4. 发票信息
5. 质量管理体系证书MDSAP(II、III、IV类强制要求MDSAP)
6. 符合性声明
(一)II类器械
由企业管理者签署声明:
他们有客观证据证明他们符合法规第10条、第11(1)和12(1)款以及第13至20条的规定。
(1)对于装饰性隐形眼睛,有客观证据证明他们符合规例第10条、第11(2)和12(2)款以及第13至17条的规定;
(2)对于IVD产品,声明使用代表为预期患者的人体受试者,并在与预期使用条件相似的条件下使用;
(3)声明不是IVD产品。
(二)III类器械
由企业管理者签署声明,并按照MDR Part1,第32(3)款提供信息和文件。
(三)IV类器械
由企业管理者签署声明,并按照MDR Part1,第32(4)款提供信息和文件。
7. 预期用途
8. 许可申请类型
9. 医疗器械使用地点
10. 包含药物的医疗器械信息
11. 包含受控物质的IVD kit
12. 器械历史
13. 器械的标识
14. 相互依赖设备的兼容性
15. 认可标准符合列表
16.优先审核(III、IV类器械)
如果希望优先审核,则需要提供优先申请,15天内对申请进行审核,申请成功,可以加速上市时间。需要满足以下条件,才可申请优先审核:
(1)目的是诊断或治疗严重的、危及生命的或严重衰弱的疾病或状况的器械;
(2)必须有充分的临床证据证明医疗设备:
A. 提供有效的疾病或状况的治疗或诊断,目前没有医疗设备在加拿大获得许可;
B. 对于在加拿大或其他地区销售的现有产品未能充分管理的疾病或状况,提供比现有治疗或诊断设备显著的风险-效 益改善;
C. 应对未预见或未得到满足的紧急卫生需求(新的)。
七. 加拿大医疗器械标签/包装要求
1. 设备名称
2. 制造商的名称和地址
3. 设备的标识符,包括作为系统、测试套件、医疗设备组、医疗设备系列的一部分的任何医疗设备的标识符
4. 对于III类或IV类装置,控制编号
5. 如果内容物不明显,则说明包装中包含的内容,以适合设备的术语表示,如尺寸、净重、长度、体积或单位数量
6. “无菌”,如果制造商打算在无菌条件下出售器械
7. 设备的有效期
8. 设备制造、销售或代表的医疗条件、目的和用途,以及设备的性能规范(如果这些规范是正确使用所必需的)
9. 使用说明
10. 适用于设备的任何特殊储存条件
八. 加拿大医疗器械注册后管理
制造商、进口商和分销商必须保留任何有关设备性能或安全问题的记录,包括消费者投诉。在设备严重伤害或导致病人死亡的情况下,制造商和进口商都必须向加拿大卫生部提交一份初步和最终报告。初步报告必须包含以下信息:
1. 设备的名称、标识符号以及制造商或进口商的联系信息
2. 有关该医疗器械对病人健康的负面影响的数据,事件发生的日期,以及召回的原因
3. 制造商或进口商对该事件的初步意见
4. 提交初步报告后,制造商和进口商必须提交一份最终报告,其中必须包括以下信息
5. 事件的详细描述
6. 对事故原因的解释以及因事故而采取的行动
7. 关于因调查而采取的任何行动的报告
如果需要召回,制造商和进口商都必须在召回处理之前或期间以及召回完成之后向加拿大卫生部报告,并且必须提供结果和为防止问题再次发生所采取的行动。
如果您对加拿大医疗器械合规认证有更多的疑问,或是了解关于加拿大医疗器械认证的价格周期,欢迎咨询Wiselink知汇的小伙伴。
Wiselink拥有包括原澳大利亚药品监督管理局局长Dr. Derrick Beech为首席顾问的国际专业团队,秉承源于澳洲、扎根中国、服务世界的精神,信守专业、真诚、开放的核心价值观,致力于为医疗器械、化妆品、食品、保健品和中药制造商提供全球合规认证和临床试验服务。