

医疗器械内窥镜是一种用于医学诊断、治疗和检查的设备,通常用于内部器官或组织的视觉检查。内窥镜通常包括光源和相机系统,以便医生能够实时观察身体内部的情况,以诊断疾病、进行治疗或进行手术。这些内窥镜可以用于检查和照明人体内部的各种部位。目前国内的医疗器械内窥镜制造商众多,出口到国外的市场需求也逐渐增大,那今天就来聊一下,内窥镜出口泰国需要怎么做?
国产的内窥镜一般是1-3类风险等级,想要将医疗器械产品出口到国外,都是需要将风险等级分类清楚,风险等级越高,则意味着难度越大。
一、泰国政府中的哪些监管机构负责泰国的医疗器械注册?
泰国食品药品监督管理局(TFDA) 是负责监管泰国医疗器械的政府机构。
医疗器械控制部是TFDA的办公室,专门负责医疗器械事务的监督。
是可以的,但是医疗器械必须先在泰国完成注册才能出售。
三、泰国对医疗器械有哪些不同的监管分类?
为了使泰国的医疗器械法规与东盟医疗器械指令(AMDD)保持一致,泰国公共卫生部发布自2019年12月19日起,医疗器械分为:
(1)体外诊断医疗设备;
(2)非体外诊断医疗器械。
体外诊断医疗器械按对个人和公共健康的危害程度从低到高分类:

泰国其他医疗器械分类:
| 风险等级 | 风险 | 注册途径(注册类型) |
| 一类 | 低风险 | 备案(自我声明) |
| 二类 | 低至中风险 | 通知(CSDT) |
| 三类 | 中等至高风险 | 通知(CSDT) |
| 四类 | 高风险 | 许可证(CSDT) |
1类设备
营业许可证
指定经营者的委托书
设备名称和描述、标签、设备规格、制造信息或产品所有者详细信息和使用说明 (IFU)(如适用)
国外注册记录(如适用)
灭菌测试报告(适用于无菌设备)
校准测试报告(用于测量设备)
制造商或产品所有者的符合性声明 (DoC)
授权书 (LOA)
2-4类设备
TFDA 已发布过渡性规定,允许制造商和进口商在 2024 年 2 月 15 日之前遵循简化要求。但是截止日期之后,2-4类器械提交的技术档案需要满足完整的 CSDT 要求。CSDT 格式要求在东盟医疗器械指令(AMDD)的附件 4 中进行了描述。
营业许可证
指定经营者的委托书
设备名称和描述、标签、制造信息、产品所有者详细信息和执行摘要
废物处理程序(如适用)
质量管理体系认证(ISO/GMP)
制造商或产品所有者的符合性声明 (DoC)
授权书 (LOA)
四、泰国医疗器械注册申请条件有哪些?
五、TFDA申请注册流程是怎样的?
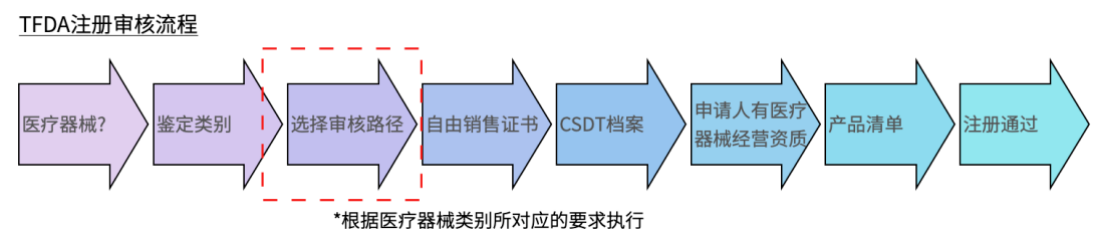
六、泰国Sponsor(泰代LAR):